Umkippen
Umkippen ist eine plötzliche, katastrophale Zustandsveränderung eines Gewässers durch Sauerstoffmangel.
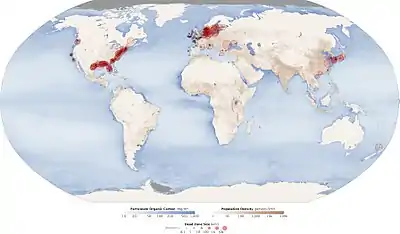
Ein auffälliges Anzeichen ist das Absterben vieler Besiedler, z. B. Fischsterben, und das einseitige Überhandnehmen anderer Besiedler, insbesondere Blaualgen und andere Bakterien. In Abschnitten größerer Gewässer und Meeresbuchten können so tote Zonen entstehen (engl. dead zones).
Die Wirkungskette

Unmittelbarer Auslöser des Umkippens ist immer der drastische Abfall der Sauerstoffkonzentration im Wasser, oft auf Null („Anoxie“), der allen aeroben Organismen die Lebensgrundlage entzieht. Ursache des Sauerstoffschwunds selbst ist in der Regel eine zu hohe Biomasse, insbesondere von einzelligen Algen (Phytoplankton) im freien Wasserkörper, die im Falle ihres natürlichen Absterbens durch mikrobiellen Abbau unter Sauerstoffverbrauch dem Wasser den Sauerstoff entziehen. Die Entstehung dieser zu hohen Algenbiomasse kann ein natürlicher Vorgang sein, wird aber häufig durch vom Menschen verstärkte Anreicherung des Wassers mit Nährstoffen erzeugt, die für das Algenwachstum wesentlich sind, also düngende Wirkung besitzen. Dieser Vorgang wird Eutrophierung des Gewässers genannt. Für das von Menschen verursachte verstärkte Algenwachstum ist dabei derjenige Nährstoff wesentlich, der durch seine vorher zu geringe Konzentration das Wachstum im unbeeinflussten Gewässer am stärksten begrenzt hatte (Minimumgesetz), dies ist in natürlichen Binnengewässern, von seltenen Ausnahmefällen abgesehen, fast immer Phosphat. Zusammengefasst kommt es zum Umkippen eines Gewässers durch die Erhöhung der Phosphatkonzentration im freien Wasserkörper. Die Phosphatanreicherung ist dabei meist ein langsamer, kontinuierlich ablaufender Prozess, der sich zunächst nur in einem immer dichteren Wachstum der Schwebalgen (Phytoplankton) äußert. Zuletzt reicht ein geringfügiger Anstoß, z. B. besonders warme Wetterbedingungen, um die Kettenreaktion in Gang zu setzen. Diese sind aber dann nur der Auslöser, nicht die eigentliche Ursache des Umkippens.
Umkippen eines Gewässers bedeutet nicht nur eine drastische, aus sich selbst irreversible Veränderung seiner Lebensgemeinschaft, sie schränkt auch seine Nutzbarkeit für den Menschen ein. Technische Maßnahmen, die den Zustand des Gewässers wieder in einen brauchbaren Zustand zurückführen sollen, werden als „Seensanierung“ bezeichnet. Wichtigstes Mittel einer Seensanierung muss es immer sein, die Phosphatkonzentration im freien Wasserkörper dauerhaft zu vermindern. Diese Aufgabe ist in der Praxis oft sehr schwierig erreichbar, da Gewässer komplexe Systeme mit zahlreichen internen Regelkreisen und Wechselwirkungen sind. Daher hat eine Absenkung der Phosphateinträge nicht immer einen linearen Abfall der Konzentration im Wasser zur Folge, weil hier komplexe Wechselwirkungen, vor allem mit den Wasserorganismen und dem am Gewässergrund abgelagerten Seensediment bestehen.
Dass es durch Sauerstoffschwund zum Umkippen des Gewässers kommen kann, wird durch verschiedene Umstände begünstigt oder verhindert. Dem Vorgang entgegen wirkt insbesondere die Nachlieferung von Luftsauerstoff in das Gewässer hinein, der den dort verbrauchten Sauerstoff ersetzt und nachliefert. Zum Umkippen kommt es dadurch vor allem in stehenden Gewässern, also in Seen oder kleineren Binnenmeeren sowie Teilen davon, beispielsweise der Ostsee, da die Strömung in Fließgewässern durch die Durchmischung dem Vorgang entgegen wirkt. Auch in sehr flachen stehenden Gewässern kommt es wegen der großen Oberfläche selten zum Umkippen. Tiefe, stehende Gewässer sind außerdem im Jahreslauf zeitweise geschichtet, also nicht völlig durchmischt, wodurch die Sauerstoffnachlieferung in die tiefen Wasserschichten unterbrochen ist. Der Vorgang in flachen Gewässern und Fließgewässern ist aber letztlich derselbe und kann auch hier, wenn auch seltener, zum Umkippen führen.
Rolle des Phosphats
Wie oben dargestellt, beruht übermäßige Eutrophierung von stehenden Gewässern, die bis zum Umkippen führen kann, beinahe ausschließlich auf dem Einfluss eines einzigen Faktors, der Erhöhung des Phosphatgehalts. Erst diese Erkenntnis, die Ende der 1960er Jahre und gegen heftige Widerstände erzielt wurde, ermöglichte die Sanierung belasteter Seen. Der Erkenntnisfortschritt wurde anfangs durch Lobbyarbeit großer Waschmittelkonzerne verzögert, die auf Phosphatzugaben in ihren Produkten nur ungern verzichten wollten.[1] (vergleichbar der heutigen Rolle von Ölkonzernen bei der Unterstützung von Klimawandelleugnern[2]). Überraschend ist der geringe Beitrag von Stickstoffverbindungen, die an Eutrophierungsvorgängen in terrestrischen Ökosystemen und in Meeresküstengewässern (Ästuaren) wesentlich mitbeteiligt oder sogar entscheidend sind. Dass Stickstoff-Überdüngung in Binnengewässern, von wenigen Spezialfällen abgesehen, praktisch keine Rolle spielt, wurde durch Manipulationsexperimente mit ganzen Seen nachgewiesen.[3][4]
Der Phosphatgehalt im Seewasser ergibt sich im Wesentlichen als einfache Funktion seiner Zufuhr aus dem Einzugsgebiet, er wird von Faktoren wie dem Volumen des Sees, dem Verhältnis von dessen Oberfläche zu seiner Tiefe, dem Verhältnis zwischen Seewasservolumen und Zu- und Abflüssen (Verweildauer) und der Alkalinität des Seewassers beeinflusst, so dass einige Seen bei gleicher Phosphatzufuhr resistenter gegen Umkippen sind als andere. Bei der Modellierung der Zusammenhänge stammen die wesentlichen Beiträge vom Program on Lake Eutrophication der OECD[5] unter Leitung von Richard A. Vollenweider,[6] die Modelle werden deshalb meist „OECD-Modelle“ oder „Vollenweider-Modelle“ genannt. Der vom Menschen erzeugte Phosphateintrag in den See wird als „Phosphatlast“ bezeichnet. Erhöhung der Phosphatlast verschiebt das Gewässer in vorhersagbarer Weise mehr oder weniger kontinuierlich vom oligotrophen über den mesotrophen zum eutrophen Zustand, ist die Phosphatlast bekannt, ist damit das weitere Schicksal des Sees vorhersagbar, auch wenn die Veränderung noch nicht eingetreten ist. Verschiebung der Phosphatzufuhr über den Schwellenwert zum eutrophen Zustand, als „kritische Last“ (oder engl. critical load) bezeichnet, führt deshalb vorhersagbar zur Zustandsverschlechterung, letztlich zum Umkippen.
Der Phosphateintrag in Gewässer aus deren Einzugsgebiet (heute nur noch selten aus direkten Einleitungen in einen See) geht in den Industrieländern etwa zur Hälfte auf sogenannte Punktquellen und zur anderen Hälfte auf sogenannte diffuse Quellen zurück. Punktquellen sind Abwassereinleitungen oder Abflüsse von Kläranlagen, die mit Phosphat aus Fäkalien, aus industriellen Abwässern und aus Wasch- und Reinigungsmitteln belastet sind. Dabei wurde der Gehalt an Polyphosphaten in Waschmitteln zur Gewässerschonung stark vermindert, bisher aber nicht in Spülmaschinenmitteln.[7] Diffuse Einträge stammen im Wesentlichen aus landwirtschaftlichem Dünger, der durch direkten Abfluss mit dem Regenwasser oder durch Bodenerosion ins Gewässer gelangt. Auch der natürliche Phosphateintrag erfolgt diffus, er macht aber heute meist nur wenige Prozent des Gesamteintrags aus.
Werden die Phosphateinträge in ein Gewässer später wieder vermindert, tritt nur selten unmittelbar der frühere Zustand wieder ein.[8] Diese Hysterese ist vor allem darauf zurückzuführen, dass ein großer Teil des Phosphats irgendwann am Gewässergrund im Seensediment festgelegt wird und daraus später wieder remobilisiert werden kann, so dass der Phosphatgehalt im freien Wasser zunächst kaum absinkt. Dieser Faktor wird als „interne Last“ (engl. internal load) bezeichnet. Zwar wird im Gleichgewichtsfall immer mehr Phosphat im Sediment abgelagert als von dort mobilisiert wird. Wird aber der Zustrom vermindert, sind Wasser und Sediment nicht mehr im Gleichgewicht. Die Erholung wird dadurch verzögert.
Hintergrund: Phosphatrücklösung
Der einfache Zusammenhang zwischen dem Phosphatgehalt in den Zuläufen und der Konzentration im Wasserkörper eines Gewässers wird durch die Rolle der Seensedimente verkompliziert. Ein Teil des zugeführten Phosphats wird in den Sedimenten festgelegt. Später kann, je nach den Bedingungen am Seengrund, ein mehr oder weniger großer Teil dieses festgelegten Anteils rückgelöst werden. Diese Rücklösung kann lange, unter Umständen Jahrzehnte, nachwirken, wenn die externen Zuflüsse bereits wieder vermindert worden sind.[9] Durch Aufnahme des Phosphors in lebende Organismen, Sedimentation von Biomasse am Gewässergrund und Rücklösung aus dem Sediment bildet sich zudem ein interner Nährstoffzyklus aus, durch den der Zustand des Gewässers sehr lange nachwirkend, möglicherweise in einigen Fällen sogar irreversibel, verschlechtert ist. Viele Forscher gehen dabei von zwei metastabilen Zuständen aus, die je nach Phosphorgehalt „kippen“ können,[10] so dass das Gewässer den neuen Zustand, der dann zum neuen Gleichgewichtszustand würde, ohne drastische Eingriffe von außen kaum jemals wieder verlassen könnte. In diesem Falle wäre das Umkippen des Gewässers und das Umkippen zwischen diesen beiden Zuständen des Sediments mehr oder weniger dasselbe. Andere Forscher gehen von eher graduellen Übergängen zwischen den Zuständen aus.[11][12]
Bedingungen am Gewässergrund eutropher Seen
In Seen bildet sich im Sommer und meist auch im Winter eine temperaturbedingte Dichteschichtung mit dazwischen liegenden Vollzirkulationen im Herbst und im Frühjahr aus. Dadurch kommt es zu einer klaren Trennung von Primärproduktion und dem Abbau von Biomasse. Der Aufbau von Biomasse unter Bindung der anorganischen Nährstoffe und unter Erzeugung von Sauerstoff findet in den lichtreichen Schichten nahe der Oberfläche, also im Epilimnion und oft auch im oberen Metalimnion statt. Dagegen ist die Remineralisation der abgesunkenen Überreste von Biomasse über dem Boden des Sees, je nach Seetiefe im Hypolimnion oder unteren Metalimnion konzentriert. Dort wird Sauerstoff verbraucht und die anorganischen Nährstoffe wieder freigesetzt. Das Wasser des Epilimnions wird durch Wind und Konvektion täglich durchmischt. Dabei wird der Sauerstoffgehalt dem Gleichgewicht mit der Luft angeglichen. Auch findet hier wegen des Lichtangebotes der größte Teil der Sauerstoff produzierenden Photosynthese statt. Das Wasser im Metalimnion und Hypolimnion erhält von außen keinen Sauerstoff. Vielmehr sinken absterbende Algen und Planktontiere sowie deren Kot von oben herab. Beim biologischen Abbau ihrer Substanz wird so viel Sauerstoff verbraucht, wie bei der Entstehung ihrer Biomasse durch Photosynthese im Epilimnion entstanden war. Dadurch wird am Boden eines eutrophen Sees oft der gesamte Sauerstoff verbraucht, das Sediment selbst, oft auch das darüber geschichtete Wasser, wird sauerstofffrei. Auch in Flachseen und Kleingewässern, in denen sich keine thermische Schichtung ausbildet und das Licht den Boden des Gewässers erreichen kann, ist oft zumindest das Sediment selbst durch Biomasse-Abbau anaerob.
Speicherung und Freisetzung des Phosphats
Phosphat kann am Seengrund im Sediment gespeichert werden. Dieser Speicher ist teilweise permanent, teilweise je nach äußeren Bedingungen reversibel, so dass das Phosphat später wieder freigesetzt werden kann. Gesteuert wird diese Freisetzung vor allem über die Alkalinität und das Redoxpotential am Gewässergrund.
In kalkreichen, stark basischen Gewässern kann ein Teil des Phosphors als Calciumphosphat, als Mineralphase Hydroxylapatit genannt, ausfällen. Bedeutender ist die teilweise Einlagerung in ausgefälltes Calciumkarbonat („Seekreide“), als Mineral Calcit genannt. In stark sauren Seen kann ein Teil des Phosphats mit freien Aluminium-Ionen als Aluminiumphosphat ausfällen oder mit Aluminiumhydroxid Al(OH)3 mitgefällt werden.[13] Beide Prozesse spielen aber in den meisten Gewässern keine große Rolle, da sie nur in sehr harten bzw. stark versauerten Gewässern ablaufen.
Bedeutsamer ist die Ausfällung des Phosphats mit Eisenionen. Dabei wird das Phosphat effektiv nur von oxidiertem, dreiwertigem Eisen festgelegt. Beträgt die Masse des dreiwertigen Eisens an der Sedimentoberfläche das fünfzehnfache der Masse des Phosphors, wird das Phosphat sehr effektiv aus dem freien Wasser entfernt.[14] Dieser Mechanismus wird als „Phosphatfalle“ bezeichnet. Das Phosphat wird dabei vor allem an amorphes Eisen(III)-oxidhydroxid (FeO(OH)) gebunden, nur unter besonderen Bedingungen als definiertes Eisenphosphat gefällt.
Unter stärker anaeroben Bedingungen wird im Sediment das dort vorhandene dreiwertige Eisen zu zweiwertigem reduziert:
Da die Verbindungen des zweiwertigen Eisens viel stärker löslich sind, werden dadurch unter reduzierenden Bedingungen die Eisenoxide aufgelöst und das daran gebundene Phosphat wieder freigesetzt. Bei Sauerstoffmangel bleibt deshalb das Phosphat im Wasser gelöst und wird mit der nächsten Zirkulation wieder düngewirksam über den ganzen See verteilt. Diese Reaktion wird allerdings durch weitere Ionen im Seenwasser stark beeinflusst. Ist der Nitrat-Gehalt des Wassers hoch, kann nach Verbrauch des freien Sauerstoffs durch Nitratatmung das Redoxpotential hoch gehalten werden. Hohe Sulfatgehalte werden hingegen durch bakterielle Desulfurikation zu Sulfid reduziert, die mit dem zweiwertigen Eisen als Eisensulfid (als kristalline Mineralphase Pyrit genannt) ausgefällt werden, wodurch das Eisen dauerhaft aus dem freien Wasser entfernt werden kann. Hohe pH-Werte mit Seekreidefällung vermindern die Wirkung der Phosphatfalle, weil ein Teil des Phosphats von Hydroxid-Ionen verdrängt werden kann.[11] Die tatsächliche P-Freisetzung vorherzusagen, ist deshalb äußerst schwierig.
Rolle von Makrophyten in Flachseen
In Flachseen und Weihern, in denen ein großer Teil des Gewässergrunds in der belichteten Zone liegt, kann es anstelle der Massenvermehrung von Algen zu einem verstärkten Wachstum von „höheren“ Wasserpflanzen kommen. Dazu zählen Röhrichtarten und untergetaucht (oder submers) lebende Gefäßpflanzen, aber auch am Boden (benthisch) wachsende, größere Algen wie z. B. die Armleuchteralgen. Die Streu und die Rückstände der Makrophyten sind biologisch schwerer abbaubar als planktonische Algen, deshalb ist ein von Makrophyten dominiertes Gewässer stabiler gegenüber Umkippen. Der makrophytenreiche Zustand könnte ein alternativer (meta-)stabiler Zustand bei gleichem Nährstoffgehalt sein.[1] Schlüsselfaktor für den Übergang zwischen plankton-dominierten und makrophyten-dominierten Zuständen scheint der Fraßdruck des Zooplankton auf die einzelligen Algen zu sein, wobei der Zooplanktonbestand von Fischen reguliert wird („trophische Kaskade“).
Versuche, das Umkippen eutrophierter Seen durch Förderung der Makrophyten zu verhindern, werden als „Biomanipulation“ zusammengefasst.
Einzelnachweise
- David W. Schindler: Recent advances in the understanding and management of eutrophication. In: Limnology and Oceanography. 51, Nr. 1, 2006, S. 356–363
- Paul C. Stern, John H. Perkins, Richard E. Sparks, Robert A. Knox (2016): The challenge of climate change neoskepticism. Science 353 (6300): 653–654. doi:10.1126/science.aaf6675
- D. W. Schindler: Evolution of Phosphorus Limitation in Lakes. In: Science. 195, Nr. 4275, 1977, S. 260–262, doi:10.1126/science.195.4275.260.
- David W. Schindler, R. E. Hecky, D. L. Findlay, M. P. Stainton, B. R. Parker, M. J. Paterson, K. G. Beaty, M. Lyng, S. E. M. Kasian: Eutrophication of lakes cannot be controlled by reducing nitrogen input: Results of a 37-year whole-ecosystem experiment. In: Proceedings of the National Academy of Sciences. 105, Nr. 32, 2008, S. 11254–11258, doi:10.1073/pnas.0805108105, PMID 18667696.
- Eutrophication of Waters (OECD) Monitoring, Assessment and Control
- Richard A. Vollenweider: Input-output models. In: Schweizerische Zeitschrift für Hydrologie. 37, Nr. 1, 1975, S. 53–84, doi:10.1007/BF02505178.
- Brigitte Osterath: Phosphatfrei waschen − phosphatbepackt spülen. In: Nachrichten aus der Chemie. 59, Nr. 9, 2011, S. 828–830, doi:10.1002/nadc.201190015.
- Erik Jeppesen u. a.: Lake responses to reduced nutrient loading – an analysis of contemporary long-term data from 35 case studies. In: Freshwater Biology. 50, Nr. 10, 2005, S. 1747–1771, doi:10.1111/j.1365-2427.2005.01415.x.
- Martin Sondergaard, Peder Jens Jensen, Erik Jeppesen: Retention and Internal Loading of Phosphorus in Shallow, Eutrophic Lakes. In: The Scientific World Journal. 1, 2001, S. 427–442, doi:10.1100/tsw.2001.72, PMID 12806078.
- S. R. Carpenter, D. Ludwig, W. A. Brock: Management of eutrophication for lakes subject to potentially irreversible change. In: Ecological Applications. 9, Nr. 3, 1999, S. 751–771, doi:10.1890/1051-0761(1999)009[0751:MOEFLS]2.0.CO;2.
- Michael Hupfer, Jörg Lewandowski: Oxygen Controls the Phosphorus Release from Lake Sediments – a Long-Lasting Paradigm in Limnology. In: International Review of Hydrobiology. 93, Nr. 4–5, 2008, S. 415–432, doi:10.1002/iroh.200711054.
- René Gächter, Bernhard Wehrli: Ten Years of Artificial Mixing and Oxygenation: No Effect on the Internal Phosphorus Loading of Two Eutrophic Lakes. In: Environmental Science & Technology. 32, Nr. 23, 1998, S. 3659–3665, doi:10.1021/es980418l.
- Jiřı́ Kopáček, Kai-Uwe Ulrich, Josef Hejzlar, Jakub Borovec, Evžen Stuchlı́k: Natural inactivation of phosphorus by aluminum in atmospherically acidified water bodies. In: Water Research. 35, Nr. 16, 2001, S. 3783–3790, doi:10.1016/S0043-1354(01)00112-9.
- H. S. Jensen, P. Kristensen, E. Jeppesen, A. Skytthe: Iron:phosphorus ratio in surface sediment as an indicator of phosphate release from aerobic sediments in shallow lakes. In: Hydrobiologia. 235–236, Nr. 1, 1992, S. 731–743, doi:10.1007/BF00026261.