Styrol-Monooxygenase
Styrol-Monooxygenase (SMO) ist ein Enzym in Bakterien. Es katalysiert die endotherme chemische Reaktion
- Styrol + FADH2 + O2 ↔ (S)-2-Phenyloxiran + FAD + H2O
| Styrol-Monooxygenase (Pseudomonas putida) | ||
|---|---|---|
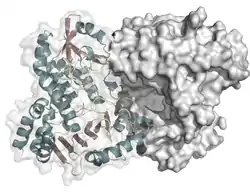
| ||
| 3D-Struktur einer Styrol-Monooxygenase nach PDB 3ihm | ||
| Masse/Länge Primärstruktur | 430 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Dimer | |
| Kofaktor | FADH2 | |
| Bezeichner | ||
| Gen-Name(n) | StyA | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 1.14.14.11, Monooxygenase | |
| Reaktionsart | Epoxydierung | |
| Substrat | Styrol + FADH2 + O2 | |
| Produkte | (S)-Styroloxid + FAD + H2O | |
| Vorkommen | ||
| Übergeordnetes Taxon | manche Bakterien | |
als ersten Schritt des aeroben Styrol-Abbauweges von Bakterien.[1] Das Produkt 2-Phenyloxiran (Styroloxid) kann von einer Styroloxid-Isomerase (SOI) zu Phenylacetaldehyd isomerisiert werden. Letzteres wird durch eine Phenylacetaldehyd-Dehydrogenase (EC 1.2.1.39) zu Phenylessigsäure, einem Schlüsselintermediat, weiter oxidiert.
Entsprechend der EC-Nummer gehört das Enzym (SMO) zur Gruppe der Oxidoreduktasen und ist vom Cofaktor FAD abhängig, so dass es als external flavoprotein monooxygenase klassifiziert wurde (Untergruppe: Typ E)[2][3]. Es bildet ein Zweikomponenten-System mit einer Reduktase (StyB, StyA2B). Die Reduktase nutzt ausschließlich NADH, um FAD zu reduzieren, welches dann zur Oxygenase (StyA, StyA1) transferiert wird. Zwei Typen des Enzymes sind bisher dokumentiert: StyA/StyB (bezeichnet als E1), zuerst in Pseudomonas-Arten beschrieben, und StyA1/StyA2B (bezeichnet als E2), zuerst in Actinobakterien beschrieben. Der E1-Typ scheint häufiger in der Natur vorzukommen und besteht aus einer einzelnen Monooxygenase (StyA), welche durch eine einzelne Reduktase (StyB) unterstützt wird. Der E2-Typ setzt sich jedoch anders zusammen. Er besteht aus einer Haupt-Monooxygenase (StyA1) und einem Fusionsprotein aus Monooxygenase und Reduktase (StyA2B). Letzteres ist die Quelle für reduziertes FAD (Reduktase) und hat zudem etwas Nebenaktivität als Oxygenase. Bisher führen alle Styrol-Monooxygenasen eine enantioselektive Epoxidierung von Styrol und chemisch analogen Verbindungen aus, was sie für biotechnologische Anwendungen interessant macht.[2]
2021 wurden erstmals Styrol-Monooxygenasen beschrieben, welche eine (R)-Selektivität aufweisen.[4][5]
Einzelnachweise
- Mooney, A., P. G. Ward, and K. E. O'Connor. 2006. Microbial degradation of styrene: biochemistry, molecular genetics, and perspectives for biotechnological applications. Appl. Microbiol. Biotechnol. 72:1-10. PMID 16823552
- Montersino, S., D. Tischler, G. T. Gassner, and W. J. H. van Berkel. 2011. Catalytic and structural features of flavoprotein hydroxylases and epoxidases. Adv. Synth. Catal. 353:2301-2319.
- van Berkel, W. J. H., N. M. Kamerbeek, and M. W. Fraaije. 2006. Flavoprotein monooxygenases, a diverse class of oxidative biocatalysts. J. Biotechnol. 124:670-689. PMID 16712999
- Hu Xiao, Shuang Dong, Yan Liu, Xiao-Qiong Pei, Hui Lin: A new clade of styrene monooxygenases for ( R )-selective epoxidation. In: Catalysis Science & Technology. Band 11, Nr. 6, 2021, ISSN 2044-4753, S. 2195–2201, doi:10.1039/D0CY02312D (rsc.org [abgerufen am 3. November 2021]).
- Can Cui, Chao Guo, Hui Lin, Zhao-Yun Ding, Yan Liu: Functional characterization of an (R)-selective styrene monooxygenase from Streptomyces sp. NRRL S-31. In: Enzyme and Microbial Technology. Band 132, 1. Januar 2020, ISSN 0141-0229, S. 109391, doi:10.1016/j.enzmictec.2019.109391 (sciencedirect.com [abgerufen am 3. November 2021]).