Sieden
Sieden, bezeichnet auch als Kochen und Wallen, ist, im Gegensatz zur Verdunstung, ein schnelles Verdampfen, also ein schneller Phasenübergang vom Flüssigen zum Gasförmigen, bei dem der Dampfdruck einer Flüssigkeit den Umgebungsdruck erreicht.[1] Sieden können sowohl Reinstoffe als auch Gemische.

Siedevorgang
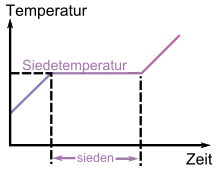
Entspricht der Sättigungsdampfdruck einer Flüssigkeit dem atmosphärischen Druck oder übersteigt diesen, so ist der Siedepunkt erreicht und die Substanz siedet.
Sofern der Druck konstant bleibt, bleibt beim Sieden von Reinstoffen (z. B. Wasser) auch die Temperatur konstant, bis die Flüssigkeit vollständig verdampft ist. Sämtliche zugeführte Wärme wird in den Phasenübergang investiert.[1] Das ist Grundlage der sehr effektiven Siedekühlung von thermisch hoch belasteten Gegenständen.
Bei Gemischen, zum Beispiel mit den Komponenten Wasser und Aceton, ist die Zusammensetzung der flüssigen und der Gasphase in der Regel unterschiedlich, die höhersiedende Komponente reichert sich in der flüssigen Phase an. Daher steigt der Siedepunkt mit fortschreitender Verdampfung. Der Siedevorgang wird am besten durch ein Siedediagramm beschrieben. In diesem Fall liegen die Komponenten in der flüssigen und der gasförmigen Phase in unterschiedlichen Konzentrationen vor. Diesen Umstand macht man sich bei thermischen Trennverfahren wie der Destillation zunutze.[2]
Beispiel Wasser
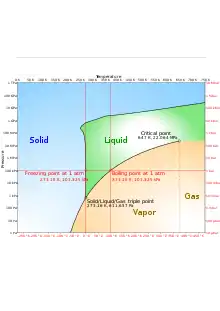
Unter Normalbedingungen, also bei einem Luftdruck von 1013 hPa und einer Temperatur von 20 °C, ist Wasser flüssig. Wird Wasser in einem oben offenen Gefäß von unten durch eine Wärmequelle erhitzt, baut sich ein Temperaturgradient auf. Am Boden ist es am heißesten, die Oberflächentemperatur entspricht noch der Lufttemperatur. Da warmes Wasser eine geringere Dichte als kaltes Wasser hat, steigt es auf, dafür sinkt kälteres Wasser nach unten (Konvektion). Bei langsamer Erwärmung kann das ganze Wasser verdampfen, ohne dass Blasen aufsteigen.
Ist die Temperatur des Bodens höher als die Temperatur des Siedepunkts beim herrschenden hydrostatischen Druck, so verdampft das Wasser. Zunächst bilden sich an kleinen Unebenheiten des Bodens (Keimbildung) Blasen aus, welche nach oben steigen und kühleres Wasser nach unten strömen lassen: das Wasser beginnt zu sieden. Die Blasen enthalten Wasserdampf oder andere Gase, die im kalten Wasser gelöst waren.
Solange Blasen aufsteigen und ein intensiver Wärmeübergang durch die Wand gewährleistet ist, spricht man vom Blasensieden. Bildet sich hingegen eine zusammenhängende Dampfschicht, bezeichnet man dies als Filmsieden.
Beim Übergang vom Blasensieden zum Filmsieden verschlechtert sich der Wärmeübergang zwischen Boden und Wasser sprunghaft. Beim Blasensieden wird das Wasser durch die aufsteigenden Blasen durchgerührt, dies fehlt beim Filmsieden. Dieser Effekt muss beim Kühlen von heißen Objekten (wie z. B. Brennelementen) mit Wasser beachtet werden.
Beim stillen Sieden ist noch nicht im gesamten Gefäß die Siedetemperatur erreicht. Die Blasen kondensieren im kälteren Wasser und brechen zusammen. Durch die aufsteigenden heißen Dampfblasen werden die oberen Schichten des Wassers zusätzlich erwärmt, bis der ganze Wasserkörper gleichmäßig aufgeheizt ist.
Die Erwärmung des Oberflächenwassers führt auch zu einer Erwärmung der darüber befindlichen Dampfphase. Ist die Oberflächentemperatur des Wassers größer als der Siedepunkt beim herrschenden Luftdruck (z. B. größer als 100 °C bei 1013 hPa), verdampft das Wasser unmittelbar entsprechend der Rate, in der die zur Verdampfung benötigte Wärme zugeführt wird.
Siedeverzug
Wasser, Wasserstoffperoxid oder Laugen (zum Beispiel Natronlauge) ohne Staubpartikel oder Gasbläschen lassen sich in reinen Gefäßen auch über die Siedetemperatur hinaus erwärmen, ohne dass es zum Sieden kommt. Kleinste Störungen, wie zum Beispiel Erschütterungen, die eine Durchmischung nach sich ziehen, können zu einer explosionsartigen Trennung der flüssigen von der Dampfphase führen, was man als Siedeverzug bezeichnet. Um das zu vermeiden, fügt man Lösungen Siedesteinchen aus Ton oder Bimsstein zu, die durch die Lösung nicht angegriffen werden, aber durch ihre poröse Struktur die Bildung kleiner Blasen erleichtern, sodass es nicht zum Siedeverzug kommt.
Physikalische Explosion
Die durch Verdampfen starke Volumenzunahme eines Stoffes kann, wenn sehr viel Hitze schlagartig zugeführt wird, zu einer physikalischen Explosion führen.
Siehe auch
Einzelnachweise
- Ernst Doering, Herbert Schedwill, Martin Dehli: Grundlagen der Technischen Thermodynamik. 2008, ISBN 978-3-8351-0149-4 (Seite 96 in der Google-Buchsuche).
- Claus Czeslik, Heiko Seemann, Roland Winter: Basiswissen physikalische Chemie. 2007, ISBN 978-3-8351-0047-3 (Seite 104 in der Google-Buchsuche).