Sepiapterin-Reduktase
Sepiapterin-Reduktase (SPR) ist das Enzym in Eukaryoten, das die Reduktion von Sepiapterin und 6-Pyruvoyl-5,6,7,8-tetrahydropterin katalysiert. Dabei handelt es sich um die letzten Schritte in der Biosynthese der Pterine, die das Grundgerüst für mehrere Vitamine und Cofaktoren bilden. SPR ist im Zytoplasma lokalisiert. Mutationen im SPR-Gen des Menschen können SPR-Mangel, und dieser eine seltene Erbkrankheit verursachen.[1]
| Sepiapterin-Reduktase | ||
|---|---|---|
| ||
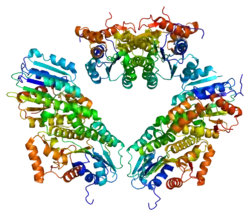
| Bändermodell des SPR-Dimers des Menschen nach 1Z6Z | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 261 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Bezeichner | ||
| Gen-Name | SPR | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 1.1.1.153, Oxidoreduktase | |
| Reaktionsart | Redoxreaktion | |
| Substrat | Sepiapterin + NADPH + H+ | |
| Produkte | 7,8-Dihydrobiopterin + NADP+ | |
| Vorkommen | ||
| Übergeordnetes Taxon | Eukaryoten | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 6697 | 20751 |
| Ensembl | ENSG00000116096 | ENSMUSG00000033735 |
| UniProt | P35270 | Q91XH5 |
| Refseq (mRNA) | NM_003124 | NM_011467 |
| Refseq (Protein) | NP_003115 | NP_035597 |
| Genlocus | Chr 2: 72.89 – 72.89 Mb | Chr 6: 85.13 – 85.14 Mb |
| PubMed-Suche | 6697 | 20751 |
Vorkommen
Aus Extrakten von Rattenlebern wurde in den 1960er Jahren ein Enzym erhalten und gereinigt, welches die Reduktion von Sepiapterin zu Dihydrobiopterin katalysierte.[2] Auch aus Insekten sowie Organen von Mäusen, Menschen und anderen Organismen wurden Sepiapterin-Reduktasen isoliert. Die ergiebigsten Quellen für SPRs sind Erythrocyten, Leber- und Gehirngewebe. Einige SPRs sind kloniert und sequenziert worden.[3] Eine Röntgenstrukturanalyse der SPR aus Mäusen ergab, dass hier ein Homodimer mit 261 Aminosäuren pro Monomer vorliegt.[4]
Eine SPR ist außerdem bei Dictyostelium nachgewiesen.[5]
Funktion
Biochemie
Zusammen mit dem Cofaktor NADPH katalysiert das Enzym die Reduktion (Hydrierung) der Carbonylgruppe des Sepiapterins zu 7,8-Dihydrobiopterin. In der Biosynthese des 5,6,7,8-Tetrahydrobiopterins ist es für die Hydrierung der Vorstufen, u. a. des 6-Pyruvoyl-5,6,7,8-tetrahydropterins verantwortlich.
Stellung im Stoffwechsel
SPR wirkt im Stoffwechsel vieler Eukaryoten an der Synthese von Pigmentfarbstoffen mit.[6]
Im Pterin-Stoffwechsel des Menschen werden unter Beteiligung von SPR Neurotransmitter der Cerebrospinalflüssigkeit produziert.[7]
Defizienz
Ein Mangel an SPR wurde klinisch beschrieben als ein therapierbarer angeborener Mangel des Pterin-Stoffwechsels. Die erfolgreiche Behandlung erfolgte über 2–5-jährige Substitutionstherapie betroffener Jugendlicher.[7]
Einzelnachweise
- UniProt P35270
- Masako Matsubara, Setsuko Katoh, Miki Akino, Seymour Kaufman, Sepiapterin reductase, Biochimica et Biophysica Acta - Enzymology and Biological Oxidation, 122 (2), 202–212 (1966); doi:10.1016/0926-6593(66)90062-2.
- UniProt Eintrag
- Günter Auerbach, Anja Herrmann, Markus Gütlich, Markus Fischer, Uwe Jacob, Adelbert Bacher, Robert Huber, The 1.25 Å crystal structure of sepiapterin reductase reveals its binding mode to pterins and brain neurotransmitters The EMBO Journal 16, 7219–7230 (1997); doi:10.1093/emboj/16.24.7219.
- Y. A. Kim, H. J. Chung u. a.: Characterization of recombinant Dictyostelium discoideum sepiapterin reductase expressed in E. coli. In: Molecules and cells. Band 10, Nummer 4, August 2000, S. 405–410, ISSN 1016-8478. PMID 10987137.
- Braasch, Ingo, Manfred Schartl, Jean-Nicolas Volff: Evolution of pigment synthesis pathways by gene and genome duplication in fish. BMC Evolutionary Biology, Band 7, Nr. 1, 2007, S. 74.
- Echenne, Bernard et al.: Sepiapterin reductase deficiency: clinical presentation and evaluation of long-term therapy. Pediatric Neurology, Band 35, Nr. 5, 2006, S. 308–313.