Saquinavir
Saquinavir (SQV) ist ein Arzneistoff aus der Gruppe der HIV-Proteaseinhibitoren und wird in Kombinationspräparaten zur Therapie von HIV-Infektionen verwendet.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
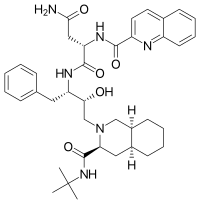 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Saquinavir | |||||||||||||||
| Andere Namen |
N-{1-Benzyl-2-hydroxy-3-[3-(tert-butylcarbamoyl)-1,2,3,4,4a,5,6,7,8,8a-decahydroisochinolin-2-yl]-propyl}-2-[(chinolin-2-yl)formylamino]-butandiamid (IUPAC) | |||||||||||||||
| Summenformel | C38H50N6O5 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code |
J05AE01 | |||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Wirkmechanismus |
Hemmung der HIV-Protease | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 670,84 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Indikation
Der Arzneistoff wird zur Behandlung HIV-1-infizierter Erwachsener eingesetzt. Die Verwendung erfolgt in Kombination mit anderen antiretroviralen Arzneimitteln im Sinne einer sogenannten „highly active antiretroviral therapy“.
Geschichte
Saquinavir wurde von Roche entwickelt und war 1995 der erste HIV-Proteaseinhibitor, der von der amerikanischen Lebens- und Arzneimittelbehörde FDA zugelassen wurde. Da es bei vielen Patienten zu rascher Resistenzentwicklung kam, wurde das Präparat vom Markt genommen und in einer neuen Formulierung und damit höherer Bioverfügbarkeit 1997 neuerlich zugelassen. Die Europäische Kommission erteilte die Zulassung für das Arzneimittel Invirase mit dem Wirkstoff Saquinavir im Oktober 1996.
Wirkungsmechanismus
Saquinavir ist ein HIV-Proteaseinhibitor. Es hemmt die HIV-Protease, ein virales Enzym, das an der Produktion neuer Viruspartikel maßgeblich beteiligt ist. Es ist so in der Lage, die Ausbreitung von HIV im Körper Infizierter zu verlangsamen. Bei der alleinigen Anwendung von Saquinavir zeigten sich sehr geringe Bioverfügbarkeitswerte, was die Wirkung deutlich beeinträchtigt. Grund dafür ist der Abbau von Saquinavir zu unwirksamen Metaboliten durch das Cytochrom P450-System. Deshalb wird dieser Arzneistoff heute in Kombination mit einem anderen HIV-Proteaseinhibitor, Ritonavir, verabreicht, was zu einer besseren Wirksamkeit durch höhere Blutplasmaspiegel führt, da Ritonavir das Cytochrom-P450-Enzymsystem hemmt.
Nebenwirkungen
Häufigste Nebenwirkungen betreffen den Gastrointestinaltrakt, also Durchfall, Übelkeit, Bauchschmerzen. Seltener kommen Kopfschmerzen und periphere Neuropathien vor.
Handelsnamen
Die Zulassung für Fortovase® wurde nach Beantragung durch Roche am 27. Juni 2006 durch die EMA zurückgezogen.[6]
Weblinks
- Öffentlicher Beurteilungsbericht (EPAR) der europäischen Arzneimittelagentur (EMA) zu: Saquinavir
- MEROPS: Saquinavir
Einzelnachweise
- Datenblatt Saquinavir mesylate, ≥98% (HPLC), powder bei Sigma-Aldrich, abgerufen am 25. Februar 2013 (PDF).
- Datenblatt SAQUINAVIR MESILATE CRS (PDF) beim EDQM, abgerufen am 19. April 2010.
- Rote Liste Online, Stand: August 2009.
- Arzneimittelkompendium der Schweiz, Stand: August 2009.
- AGES-PharmMed, Stand: August 2009.
- EMA: Public statement on Fortovase: Withdrawal of the marketing authorisation in the European Union.