Raltegravir
Raltegravir (Handelsname: Isentress; Hersteller: MSD Sharp & Dohme) ist ein Arzneistoff aus der Gruppe der Integraseinhibitoren, der zur Behandlung HIV-infizierter Patienten eingesetzt wird.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
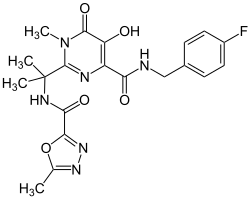 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Raltegravir | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C20H21FN6O5 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
J05AX08 | ||||||||||||||||||
| Wirkstoffklasse | |||||||||||||||||||
| Wirkmechanismus | |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 444,41 g·mol−1 | ||||||||||||||||||
| Löslichkeit |
wasserlöslich[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Isentress ist das erste zugelassene Arzneimittel aus der Gruppe der Integraseinhibitoren. Raltegravir soll im Vergleich zu anderen bei der HAART eingesetzten Arzneimitteln besser verträglich sein; zudem erhofft man sich eine gute Wirksamkeit auch bei Patienten mit multiresistenten Viren.
Geschichte
Isentress wurde am 12. Oktober 2007 in den USA und am 20. Dezember 2007 in der Europäischen Union zugelassen. Raltegravir ist damit der erste Vertreter dieser neuen Wirkstoffklasse der Integraseinhibitoren, der auf den Markt kommt. In der EU wurde zunächst nur eine bedingte Zulassung erteilt, die den Hersteller verpflichtete, im Laufe des Jahres unter anderem weitere Studienergebnisse aus zwei Phase-III-Studien vorzulegen, die in die Bewertung des Nutzen-Risiko-Verhältnis einfließen. Am 14. Juli 2009 wurde die Genehmigung „unter Auflagen“ aufgehoben. Die uneingeschränkte Genehmigung für das Inverkehrbringen gilt fünf Jahre und kann anschließend verlängert werden.[1] Das Bundespatentgericht hat am 31. August 2016 im Weg der einstweiligen Verfügung eine Zwangslizenz an dem Medikament erteilt, die der Bundesgerichtshof mit Urteil vom 11. Juli 2017 bestätigt hat.[3]
Klinische Angaben
Anwendungsgebiete (Indikationen)
Raltegravir ist für die Kombinationstherapie von HIV-infizierten Erwachsenen zugelassen, bei denen es trotz antiretroviraler Therapie zu nachgewiesener HIV-1-Replikation kommt.[1]
Gegenanzeigen (Kontraindikationen)
Überempfindlichkeit gegen den Wirkstoff.
Nebenwirkungen
Die häufigsten (>10 %) unerwünschten Ereignisse während der klinischen Studien waren Diarrhoe, Übelkeit, Kopfschmerzen und Fieber. Die Therapieabbruchrate aufgrund von unerwünschten Ereignissen lag bei mit Raltegravir behandelten Patienten bei zwei Prozent im Vergleich zu 1,4 Prozent bei Placebo.[1] Erfahrungen aus Langzeitbehandlung liegen noch nicht vor.
Pharmakologie
Pharmakodynamik
Raltegravir wirkt als Integraseinhibitor. Die retrovirale Integrase ist ein Schlüsselenzym, das das HI-Virus für die Integration seines Genoms in die Chromosomen der Wirtszelle benötigt. Raltegravir hemmt einen wesentlichen katalytischen Schritt dieses Enzyms, den Strangtransfer, verhindert dadurch die Integration der viralen Nukleinsäure und reduziert in der Folge die Virusreplikation. Eine Reihe weiterer Enzyme, darunter auch retrovirale Reverse Transkriptase, wurden daraufhin getestet, ob sie durch Raltegravir gehemmt würden. Dies konnte nicht beobachtet werden; es gilt als gesichert, dass die antivirale Aktivität ausschließlich auf die Hemmung der Integrase zurückzuführen ist. Körpereigene Enzyme werden nicht beeinflusst.[1]
Pharmakokinetik
Raltegravir wird rasch resorbiert; die Aufnahme wird von Mahlzeiten wenig beeinflusst. Der Arzneistoff wird durch Glucuronidierung metabolisiert. Für die terminale Halbwertszeit werden zirka neun Stunden angegeben.[1]
Toxikologie
Es gibt keine spezifischen Informationen zur Überdosierung bei Patienten. Die Toxizitätsbestimmung wurde an Mäusen, Ratten und Hunden durchgeführt. Dabei war eine einzelne perorale Gabe von Raltegravir in der Maus gut verträglich (LD50 > 2000 mg/kg); bei intravenöser Gabe lag die höchste verträgliche Dosis bei 100 mg/kg/Tag. Bei wiederholter oraler Gabe wurden 50 mg/kg/Tag gut vertragen. In ähnlichen Studien in Ratten wurde ein NOAEL von 120 mg/kg/Tag bestimmt. Beim Hund zeigten sich nach einjähriger oraler Gabe von > 360 mg/kg/Tag keine Schädigungen. In Studien zur Genotoxizität und Reproduktionstoxizität war der Stoff unauffällig. Studien zur Karzinogenität sind noch nicht abgeschlossen.[1]
Einzelnachweise
- Öffentlicher Beurteilungsbericht (EPAR) der europäischen Arzneimittelagentur (EMA) zu: Isentress.
- Registrierungsdossier zu N-[(4-fluorophenyl)methyl]-1,6-dihydro-5-hydroxy-1-methyl-2-[1-methyl-1-[[(5-methyl-1,3,4-oxadiazol-2-yl)carbonyl]amino]ethyl]-6-oxo-4-pyrimidinecarboxamide (Abschnitt GHS) bei der Europäischen Chemikalienagentur (ECHA), abgerufen am 11. Juli 2020.
- Pressemitteilung des Bundesgerichtshofs vom 11. Juli 2017 Nr. 111/17, abgerufen am 11. Juli 2017