Pincer-Ligand
Ein Pincer-Ligand ist ein tridentates Ligandsystem, welches meist an ein Übergangsmetall gebunden ist.
Geschichte
Die ersten Pincer-Komplexe wurden in den 1970er Jahren von B. L. Shaw und C. J. Moulton[1] veröffentlicht. Seither wurden viele unterschiedliche Ligand-Systeme synthetisiert und veröffentlicht.
Eigenschaften
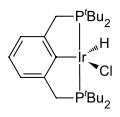
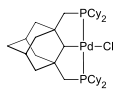
Pincer-Liganden sind so aufgebaut, dass sie mit zwei Donor-Atomen (zum Beispiel Phosphor, Stickstoff oder Schwefel) und einer σ-Bindung an das (Übergangs-)Metall binden können. Oft werden Phosphine als Donatoren verwendet, da sie einfach verändert werden können. So kann beispielsweise die Sterik sehr einfach verändert werden. Wenn der Pincer-Ligand über zwei Phosphor-Donatoren und mit einer Kohlenstoff-Metall σ-Bindung an das Metall gebunden ist, spricht man von einem PCP-Pincer-Liganden. Auch die Bindung mittels einer Stickstoff-Metall σ-Bindung ist möglich (PNP). Des Weiteren sind NCN-(Stickstoff-Kohlenstoff-Stickstoff) und SCS-(Schwefel-Kohlenstoff-Schwefel)-Ligandensysteme häufig. Als Ligandrückgrat dienen meist Phenylsysteme. Allerdings sind auch aliphatische Systeme bekannt.[2] Werden die Liganden an ein Metall gebunden, ergeben sich coplanare Systeme, welche sehr starr sind. Dies führt zu einer erhöhten thermischen Stabilität des Systems.
Anwendungen
Pincer-Liganden können in vielen katalytischen Prozessen eingesetzt werden: Aktivierung von Kohlenstoffdioxid (CO2),[5] Stickstoff (N2),[6] Polymerisation von Alkenen[7][8] und Alkinen,[9] Alkan-Dehydrogenierung[10][11] und Transfer-Hydrierung.[12]
Einzelnachweise
- C. J. Moulton, B. L. Shaw: J. Chem. Soc., Dalton Trans. 1976, S. 1020.
- R. Gerber, O. Blacque, C. M. Frech: ChemCatChem. 1, 2009, S. 393.
- C. J. Moulton, B. L. Shaw: J. Chem. Soc., Dalton Trans. 1976, S. 1020.
- R. Gerber, O. Blacque, C. M. Frech: ChemCatChem. 1, 2009, S. 393.
- D. W. Lee, C. M. Jensen, D. Morales-Morales: Organometallics. 22, 2003, S. 4744–4749.
- A. Vigalok, Y. Ben-David, D. Milstein: Organometallics. 15, 1996, S. 1839–1844.
- D. S. McGuiness, V. C. Gibson, J. W. Steed: Organometallics. 23, 2004, S. 6288–6292.
- D. S. McGuiness, V. C. Gibson, D. D. F. Wass, J. W. Steed: J. Am. Chem. Soc. 125, 2003, S. 12716–12717.
- J. Yao, W. T. Wong, G. Jia: J. Organomet. Chem. 598, 2000, S. 228–234.
- F. Liu, E. B. Pak, B. Singh, C. M. Jensen, A. S. Goldman. J. Am. Chem. Soc. 121, 1999, S. 4086–4087.
- C. Jensen. Chem. Commun. 1999, S. 2443–2449.
- P. Dani, T. Karlen, R. A. Gossage, S. Gladiali, G. van Koten: Angew. Chem., Int. Ed. 39, 2000, S. 743–745.