Pertussisimpfstoff
Ein Pertussisimpfstoff (Synonym: Keuchhustenimpfstoff) ist ein Impfstoff gegen eine Keuchhusten-Erkrankung (Pertussis). Der Pertussisimpfstoff befindet sich auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation.[1] Die Weltgesundheitsorganisation empfiehlt eine Verwendung von Pertussisimpfstoffen in einem Fünffachimpfstoff mit Impfstoffen gegen Diphtherie, Tetanus, Hepatitis B und Haemophilus influenzae b.[2]
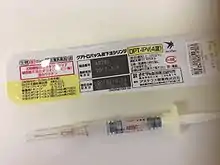
Eigenschaften
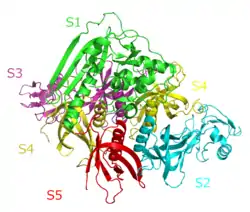
Der in Europa (mit Ausnahme von Polen)[3] und USA verwendete Pertussisimpfstoff ist ein Toxoidimpfstoff, der gegen das Pertussistoxin (PT) und teilweise auch gegen das filamentöse Hämagglutinin (FHA), Pertactin (PRN, ein Porin) und Fimbrien (Agglutinogene) in fixierter Form (FIM) der Typen 2 und 3 immunisiert, in unterschiedlichen Kombinationen und Dosierungen.[3][4][5] Die wirksamen Bestandteile (mit Ausnahme von Polen) verwendeten Pertussisimpfstoffe enthalten keine Erreger-Zellen mehr, sondern sind azellulär (abgekürzt aP). In der Regel wird eine Wirkverstärkung durch Adsorption an ein Adjuvans wie Aluminiumhydroxid und Aluminiumphosphat eingesetzt.
Der Erreger bildet eine Reihe weiterer Toxine und andere Virulenzfaktore, vor allem das ebenfalls humanpathogene Adenylzyklase-Hämolysin[6] und Trachea-Zytotoxin.[7] Aufgrund abnehmender Herdenimmunität und Mutationen des Erregers hat die Anzahl der Infektionen in den letzten Jahren zugenommen.[8]
Einzel-Impfstoffe
Nachdem 1906 eine Methode zur Isolierung von B. pertussis durch die Arbeit von Jules Bordet und Octave Gengou veröffentlicht wurde, begann die Suche nach Impfstoffen.[9] Die ersten Pertussisimpfstoffe – basierend auf abgetöteten Zellen des Erregers (Ganzkeimimpfstoff, auch Ganzzellimpfstoff[10], englisch whole cell Pertussis Vaccine, abgekürzt wP) – wurden 1912 durch Bordet und Gengou, 1913 durch Charles Nicolle und 1914 durch Thorvald Madsen entwickelt.[9] Während einer Keuchhusten-Epidemie auf Färöer (1923/24) wurde ein Ganzkeimimpfstoff getestet. Der Impfstoff konnte zwar die Infektion größtenteils nicht verhindern, jedoch die Sterblichkeit sowie die Schwere der Symptome unter Geimpften erheblich senken.[11] In einer 1926 durchgeführten klinischen Studie wurde beobachtet, dass eine Impfung nicht erst nach, sondern vor Ausbruch der Erkrankung schützt (Impfstoffwirksamkeit etwa 75 %).[11] Mit diesem Wissen konnte einem Keuchhustenausbruch 1929 auf Färöer besser begegnet werden.[11]
Bei einer neuen, zweiten Generation von Impfstoffen wurden abgetötete Erreger zentrifugiert und anschließend teilweise gereinigt.[12] Diese Ganzkeimimpfstoffe wurden erstmals 1933[13] durch die Arbeiten von Madsen vorgestellt.[12] Die Bakteriologin Pearl Kendrick verfeinerte sie und begann in den späten 1930er Jahren und frühen 1940er Jahren klinische Studien an Kindern. Zudem kombinierten sie und ihre Kollegen 1942 einen DTP-Kombinationsimpfstoff,[9] der dann 1948 in den USA zugelassen wurde.[14]
Nach unerwünschten Nebenwirkungen von Ganzkeimimpfstoffen begannen in den 1970er Jahren in Japan die Entwicklung von azelluären Impfstoffen (aP).[9] Zunächst enthielten diese hauptsächlich FHA sowie kleinere Mengen des PT-Toxoids (Takeda-Typ-Vakzine bzw. T-Typ-Impfstoffe, benannt nach dem japanischen Hersteller Takeda), später gleiche Mengen (Biken-Typ-Vakzine bzw. B-Typ-Impfstoffe, benannt nach dem japanischen Hersteller Biken).[3] Ab 1981 wurden aP-Impfstoffe zunächst ausschließlich in Japan eingesetzt.[15][3] Durch den großen Erfolg begannen auch andere Länder mit der Entwicklung azelluärer Impfstoffe, die sich in Hinblick verschiedener Faktoren (Art und Menge Komponenten, Adjuvanzien, Methode der Reinigung oder der Toxininaktivierung) voneinander unterscheiden.
Im Jahr 1975 beschränkte die Ständige Impfkommission (STIKO) ihre Empfehlung für den Einsatz des Ganzkeimimpfstoffs aufgrund gehäufter Nebenwirkungen (vornehmlich starke Lokalreaktionen, Fieberkrämpfe und einzelne Enzephalopathien) auf Kinder mit erhöhtem Risiko.[16] In der DDR wurde der Ganzkeimimpfstoff dagegen unvermindert eingesetzt.[17] Die STIKO erweiterte 1991 die Impfempfehlung wieder.[17] Der DTwP-Impfstoff wurde als Kombinationsimpfung von 1930 bis 1991 verwendet, bis der ebenfalls darin enthaltene Pertussisimpfstoff aufgrund von Schmerzen und Rötung an der Einstichstelle bei 50 % der Geimpften in den USA gegen eine zellfreie Form (azellulärer Pertussisimpfstoff, aP) ausgetauscht wurde, was anschließend als TDaP oder DTaP bezeichnet wurde.[5] Der wP-Impfstoff enthält Endotoxine von B. pertussis, die stärkere Nebenwirkungen auslösen.[18] aP-Impfstoffe wurden erstmals in Deutschland 1995 verfügbar, sowohl monovalent als auch in Kombination mit Diphtherie- und Tetanustoxoid (DTaP).[4][17] Im Jahr 2000 wurde die Impfempfehlung auf ältere Kinder (von 9 bis 17 Jahren) und ab 2009 auf Erwachsene ausgedehnt.[17]
Heutige Impfstoff-Kombinationen
In Deutschland und in den meisten anderen europäischen Staaten sind derzeit Pertussisimpfstoffe ausschließlich in Kombinationspräparaten auf dem Markt. So steht ein Pertussis-Einzelimpfstoff in Deutschland aktuell nicht zur Verfügung,[19] seitdem der letzte (PAC MÉRIEUX von Sanofi Aventis) 2005 vom Markt genommen wurde.[20]
Die Kombinationsimpfstoffe richten sich gegen Keuchhusten, Tetanus und Diphtherie (DTP-Impfstoff) bis zur 6-fach-Impfung zusätzlich gegen Kinderlähmung, Hepatitis B und Haemophilus influenzae Typ b (hexavelenter Impfstoff). Die Komponenten der Kombinationsimpfstoffe werden dabei abgekürzt, beispielsweise Tdap eines 3-fach-Impfstoffes oder DTaP-IPV-Hib-HepB eines 6-fach-Impfstoffes. Diese Kombinationen enthalten neben Bestandteilen von B. pertussis (aP) auch Tetanusimpfstoff gegen das Toxin von Clostridium tetani (T oder t) und Diphtherieimpfstoff gegen das Toxin von Corynebacterium diphtheriae (D oder d). Die kleinen Buchstaben t bzw. d in den Abkürzungen kennzeichnen dabei geringere Konzentrationen der jeweiligen Komponente.[21] DTaP wird meistens zur Immunisierung von Kindern verwendet, während für den Wiederholungsimmunisierung von Erwachsenen sowie die Erstimmunisierung im Erwachsenenalter (bei Personen, die bisher weder an Diphtherie erkrankt waren noch dagegen geimpft wurden) meistens Tdap verwendet wird.[5]
In anderen Gebieten wird weiterhin der Ganzkeimimpfstoff wP verwendet, wie im mittleren Osten, in Afrika und Südamerika.[3]
Immunologie
Nach wiederholter Impfung mit aP-Impfstoff entstehen je nach Impfstoff neutralisierende Antikörper gegen das Pertussistoxin in 71–85 % der Geimpften,[22] beim wP-Impfstoff dagegen in etwa 78 % der Geimpften.[23] Die Wirksamkeitsraten unter wP-Impfstoffen ist aber mit einer erheblichen Streuung (von ca. 40 bis 90 %) verbunden.[23][24] Dies liegt an der komplexen Antigen-Zusammensetzung (mehr als 3000 antigene Strukturen, variabler Fertigungsprozess).[24] Pro Jahr nimmt der Impfschutz zwischen 2 und 10 % ab, mit einer schnelleren Abnahme beim aP-Impfstoff.[23] Durchschnittlich erzeugt also der azelluläre Pertussisimpfstoff eine nur geringfügig geringere und kürzere Immunität als der zellenthaltende Vorgänger wP, hat dafür aber weniger Nebenwirkungen:[22][25]
In Deutschland empfiehlt die STIKO zunächst eine Grundimmunisierung bei Säuglingen durch drei Impfungen im Alter von 2, 4 und 11 Monaten (sogenanntes 2+1-Impfschema). Für Frühgeborene (Geburt vor vollendeten 37. Schwangerschaftswoche) wird zusätzlich eine Impfung im 3. Lebensmonat empfohlen (3+1-Impfschema).[26] Der Impfschutz soll dann verlängert werden durch zwei Auffrischimpfungen im Alter von 5–6 Jahren und 9–17 Jahren. Für Erwachsene soll ein einmaliger Booster (ap) erfolgen; dies soll im Zuge der geplanten Td-Auffrischimpfung durch eine Tdap- oder (je nach Indikation) einer Tdap-IPV-Kombinationsimpfung erfolgen, da kein monovalenter Pertussisimpfstoff zur Verfügung steht.[27]
Für Schwangere ist eine Impfung mit einem Tdap-Kombinationsimpfstoff zu Beginn des 3. Trimenons seit 2020 ausdrücklich empfohlen, da die Impfung die Erkrankungen bei Neugeborenen und jungen Säuglingen reduzieren kann.[27] Diese kann bereits im 2. Trimenon erfolgen, falls eine Frühgeburt wahrscheinlich ist.
Art und Umfang des Impfschutzes
Die mit aP Geimpften sind nach Infektion vor der Erkrankung weitgehend geschützt, können aber vorübergehend mit Bordetellen besiedelt sein und damit als mehr oder weniger asymptomatische Keimträger eine Infektionsquelle darstellen.[28][23] Die Übertragung kann auch über kontaminierte Gegenstände erfolgen, da B. pertussis gegen Austrocknung resistent ist und für einige Tage außerhalb des Organismus überleben kann. Wegen des hohen Kontagionsindex bei nicht-immunen Menschen kann sich B. pertussis in Bevölkerungen mit niedriger Durchseuchungsrate epidemisch ausbreiten. Aber selbst in Regionen mit hoher Impfquote mit dem aP-Impfstoff bleibt der Pertussis-Erreger endemisch, da der Immunitätsnachlass eine Besiedelung erlaubt. Daher ist aus heutiger Sicht mit dem aP-Impfstoff weder der Aufbau einer sicheren Herdenimmunität[29] noch gar eine Eradikation des Erregers möglich.[7] Der Pertussisimpfstoff wirkt nicht gegen die Toxine von B. parapertussis oder B. holmesii, die zwar ebenfalls zu einem keuchhustenähnlichen Krankheitsbild führen, das aber seltener vorkommt und meist leichter und kürzer ist als das durch B. pertussis.[7] Dennoch schützt der aP-Pertussisimpfstoff vor einer Erkrankung, die durch Bordetella parapertussis erzeugt wird.[30] Tendenziell korreliert der Impfschutz stärker mit Antikörpern gegen Protactin und Fimbrien, als mit Antikörpern gegen das Pertussistoxin – allerdings schützen die Antikörper gegen das Pertussistoxin vor den Symptomen des Keuchhustens.[18]
Nebenwirkungen
Unerwünschte Arzneimittelwirkungen bei aP-Impfstoff umfassen Schmerzen, Schwellung und Rötung an der Einstichstelle.[23] Beim wP-Impfstoff treten bei 10 bis 50 % der Geimpften Rötung an der Einstichstelle oder Fieber auf.[23] In 1 % der wP-Geimpften treten Fieberkrämpfe auf.[23] Je jünger der Geimpfte ist, desto weniger ausgeprägt sind die unerwünschten Arzneimittelwirkungen.[23] Der wP-Impfstoff sollte nicht bei Kindern über 7 Jahren verwendet werden.[23]
Handelsnamen
Handelsnamen für Kombinationsimpfstoffe, die auch einen Pertussisimpfstoff enthalten, sind z. B. Boostrix, Covaxis, Hexacima, Hexyon, Pa-Vaccinol, Pac-Mérieux, Acel-P und Infanrix in Europa und in den USA Infanrix und Daptacel für Kinder (DTaP) und Boostrix und Adacel für Erwachsene (Tdap).[31][32][5]
Einzelnachweise
- WHO Model List of EssentialMedicines. In: World Health Organization. Oktober 2013. Abgerufen am 22. April 2014.
- E. S. Bar-On, E. Goldberg, S. Hellmann und L. Leibovici: Combined DTP-HBV-HIB vaccine versus separately administered DTP-HBV and HIB vaccines for primary prevention of diphtheria, tetanus, pertussis, hepatitis B and Haemophilus influenzae B (HIB). In: Cochrane Database Syst Rev. Nr. 4, 2012, S. CD005530. doi:10.1002/14651858.CD005530.pub3. PMID 22513932.
- Kathryn M. Edwards und Michael D. Decker: Pertussis Vaccines. In: Stanley A. Plotkin et al. (Hrsg.): Plotkin's Vaccines. 7. Auflage. Elsevier, Philadelphia 2017, ISBN 978-0-323-35761-6, S. 711 ff., doi:10.1016/B978-0-323-35761-6.00043-2.
- Ulrich Heininger: Pertussis (Keuchhusten). In: Monatsschrift Kinderheilkunde. Band 168, Nr. 8, 1. August 2020, S. 747–759, doi:10.1007/s00112-020-00941-9, PMID 32836397, PMC 7364744 (freier Volltext).
- Centers for Disease Control and Prevention: CDC Pink Book: Pertussis.
- N. H. Carbonetti: Pertussis toxin and adenylate cyclase toxin: key virulence factors of Bordetella pertussis and cell biology tools. In: Future microbiology. Band 5, Nummer 3, März 2010, S. 455–469, doi:10.2217/fmb.09.133, PMID 20210554, PMC 2851156 (freier Volltext).
- Robert Koch-Institut: RKI-Ratgeber Keuchhusten (Pertussis), online Stand: 27. November 2017, Abruf 19. September 2019
- A. A. van der Ark, D. F. Hozbor, C. J. Boog, B. Metz, G. P. van den Dobbelsteen, C. A. van Els: Resurgence of pertussis calls for re-evaluation of pertussis animal models. In: Expert review of vaccines. Band 11, Nummer 9, September 2012, S. 1121–1137, doi:10.1586/erv.12.83, PMID 23151168.
- Institute of Medicine (US) Committee to Review the Adverse Consequences of Pertussis and Rubella Vaccines, Christopher P. Howson, Cynthia J. Howe, Harvey V. Fineberg: Histories of Pertussis and Rubella Vaccines. National Academies Press (US), 1991 (nih.gov [abgerufen am 12. August 2020]).
- Azelluläre Impfstoffe zum Vorbeugen von Keuchhusten (Pertussis) bei Kindern. In: Cochrane. 17. September 2014, abgerufen am 15. Oktober 2021.
- Marta Granström: The History of Pertussis Vaccination: From Whole-Cell to Subunit Vaccines. In: Stanley A. Plotkin (Hrsg.): History of Vaccine Development. Springer, New York 2011, ISBN 978-1-4419-1338-8, S. 73–82, doi:10.1007/978-1-4419-1339-5_10.
- T. Jefferson: Why the MRC randomized trials of whooping cough (pertussis) vaccines remain important more than half a century after they were done. In: Journal of the Royal Society of Medicine. Band 100, Nr. 7, Juli 2007, S. 343–345, PMID 17606757, PMC 1905874 (freier Volltext).
- Thorvald Madsen: VACCINATION AGAINST WHOOPING COUGH. In: Journal of the American Medical Association. Band 101, Nr. 3, 15. Juli 1933, S. 187–188, doi:10.1001/jama.1933.02740280007003.
- Jeffrey P. Baker und Samuel L. Katz: Childhood vaccine development: an overview. In: Pediatric Research. Band 55, Nr. 2, Februar 2004, S. 347–356, doi:10.1203/01.PDR.0000106317.36875.6A, PMID 14630981.
- Y. Sato, M. Kimura, H. Fukumi: Development of a pertussis component vaccine in Japan. In: Lancet (London, England). Band 1, Nr. 8369, 21. Januar 1984, S. 122–126, doi:10.1016/s0140-6736(84)90061-8, PMID 6140441.
- Arbeitsergebnisse der Ständigen Impfkommission des Bundesgesundheitsamtes: Empfehlung der Ständigen Impfkommission des Bundesgesundheitsamtes zur Keuchhusten-Impfung. In: Bundesgesundheitsblatt. Nr. 9, 2. Mai 1975 (rki.de [PDF]).
- Robert Koch-Institut: Epidemiologisches Bulletin 24. Mai 2017 / Nr. 21, S. 188. In: rki.de. Abgerufen am 11. August 2020.
- J. D. Cherry: Pertussis: challenges today and for the future. In: PLoS pathogens. Band 9, Nummer 7, 2013, S. e1003418, doi:10.1371/journal.ppat.1003418, PMID 23935481, PMC 3723573 (freier Volltext).
- Pertussis (Keuchhusten): RKI-Ratgeber für Ärzte
- Letzter monovalenter Pertussis-Impfstoff vom Markt Arznei-Telegramm vom Juli 2005.
- J. D. Cherry: How can we eradicate pertussis. In: Advances in Experimental Medicine and Biology. Band 634, 2009, S. 41–51, doi:10.1007/978-0-387-79838-7_4, PMID 19280847.
- L. Zhang, S. O. Prietsch, I. Axelsson, S. A. Halperin: Acellular vaccines for preventing whooping cough in children.. In: The Cochrane database of systematic reviews. 9, 17. September 2014, S. CD001478. doi:10.1002/14651858.CD001478.pub6. PMID 25228233.
- Weltgesundheitsorganisation (WHO): Pertussis vaccines: WHO position paper - September 2015. In: Releve epidemiologique hebdomadaire. Band 90, Nummer 35, August 2015, S. 433–458, PMID 26320265.
- Fred Zepp, Markus Hufnagel: Impfungen und Reiseimpfungen. In: Georg F. Hoffmann et al. (Hrsg.): Pädiatrie: Grundlagen und Praxis (= Springer Reference Medizin). Springer, Berlin, Heidelberg 2020, ISBN 978-3-662-60300-0, S. 152, doi:10.1007/978-3-662-60300-0_13.
- A. Allen: Public health. The pertussis paradox. In: Science. Band 341, Nummer 6145, August 2013, S. 454–455, doi:10.1126/science.341.6145.454, PMID 23908204.
- Epidemiologisches Bulletin 26/2020. In: RKI. 25. Juni 2020, abgerufen am 29. November 2020.
- Epidemiologisches Bulletin. (PDF) In: RKI. 26. August 2021, S. 22, abgerufen am 8. Oktober 2021.
- Robert Koch-Institut: Schutzimpfung gegen Pertussis: Häufig gestellte Fragen und Antworten, 14. Dezember 2012, abgerufen am 18. September 2019.
- Pertussis Frequently Asked Questions, [Centers for Disease Control and Prevention], online 1. April 2019, Abruf 19. September 2019
- J. Liko, S. G. Robison, P. R. Cieslak: Do Pertussis Vaccines Protect Against Bordetella parapertussis? In: Clinical Infectious Diseases. Band 64, Nummer 12, Juni 2017, S. 1795–1797, doi:10.1093/cid/cix221, PMID 28369240.
- Paul-Ehrlich-Institut: Impfstoffe gegen Pertussis (Keuchhusten) (Memento vom 2. März 2016 im Internet Archive). Abgerufen am 29. Februar 2016.
- Burghard Stück, Burkhard Schneeweiß, Heinz-Josef Schmitt, Carl Heinz Wirsing von König: Neues über Pertussis und Pertussis-Impfstoffe. In: Deutsches Ärzteblatt (1996), Band 93, Heft 49, S. A-3270–3276. (PDF).