Perfluoroctansulfonamid
Perfluoroctansulfonamid (PFOSA) ist eine chemische Verbindung, die zu den per- und polyfluorierten Alkylverbindungen (PFAS) gehört.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
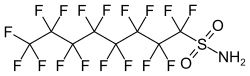 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Perfluoroctansulfonamid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H2F17NO2S | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 499,14 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt |
145–150 °C[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
In der Umwelt kann PFOSA zu Perfluoroctansulfonat (PFOS) umgewandelt werden.[2]
Darstellung
PFOSA kann durch die Reaktion von Perfluoroctansulfonsäurehalogeniden mit flüssigem Ammoniak[2] oder über eine zweistufige Reaktion via Azid, gefolgt von einer Reduktion durch Zn/HCl[3] dargestellt werden.
Verwendung
N-Alkyl-substituierte Perfluoroctansulfonamide werden in photographischen Papieren, in medizinischen Anwendungen sowie Pestiziden eingesetzt.[4] PFOSA reichert sich über die Nahrungskette an (Bioakkumulation).[5] Es wird angenommen, dass PFOSA die biologische aktive Form des Insektizids Sulfluramid (N-Ethylperfluoroctansulfomamid) darstellt.[6] PFOSA kamen bis zum Verbot in der Oberflächenmodifikation als Nebelgasminderer in der Metallverarbeitung und als Korrosionsschutz in der Verchromung zum Einsatz, ebenfalls in der Textilindustrie. Weiteres Anwendungsgebiet war in der chemischen Industrie als Löschschaum, Reinigungsmittel (Shampoo, Teppichreiniger).[7]
Regulierung
Da Perfluoroctansulfonamid unter die Definition „Perfluoroctansulfonsäure und ihre Derivate (PFOS) C8F17SO2X (X = OH, Metallsalze (O–M+), Halogenide, Amide und andere Derivate einschließlich Polymere)“ fällt, unterliegt es in der EU und in der Schweiz einem weitreichenden Verbot.[8][9]
Einzelnachweise
- JK-Scientific: Perfluorooctanesulfonamide (PDF; 132 kB), abgerufen am 27. Dezember 2019.
- HJ Lehmler: Synthesis of environmentally relevant fluorinated surfactants—a review. In: Chemosphere. 58, Nr. 11, 2005, S. 1471–1496. doi:10.1016/j.chemosphere.2004.11.078. PMID 15694468.
- Lehmler HJ, Rama Rao VV, Nauduri D, Vargo JD, Parkin S: Synthesis and Structure of Environmentally Relevant Perfluorinated Sulfonamides. In: J Fluor Chem. 128, Nr. 6, 2007, S. 595–607. doi:10.1016/j.jfluchem.2007.01.013. PMID 18516235. PMC 2394736 (freier Volltext).
- Patentanmeldung EP0021003B1: Verwendung von Perfluoralkansulfonamid-Salzen als Tenside. Angemeldet am 14. Mai 1980, veröffentlicht am 9. Februar 1983, Anmelder: Bayer AG, Erfinder: Karl-Heinz Mitschke, Hans Niederprüm.
- UBA Texte 41/2007: Entwicklung und Validierung einer Methode zur Bestimmung von polyfluorierten organischen Substanzen in Meerwasser, Sedimenten und Biota; Untersuchungen zum Vorkommen dieser Schadstoffe in der Nord- und Ostsee (PDF; 6,4 MB).
- A.A. Starkov, K.B. Wallace: Structural determinants of fluorochemical-induced mitochondrial dysfunction. In: Toxicol. Sci.. 66, Nr. 2, 2002, S. 244–252. doi:10.1093/toxsci/66.2.244. PMID 11896291.
- Janine Kowalczyk: Übergang von Perfluoroctansäure (PFOA) und Perfluoroctansulfonsäure (PFOS) aus kontaminierten Futtermitteln in ausgewählte Gewebe des Mastschweins und der Legehenne. In: Bundesinstitut für Risikobewertung (Hrsg.): Dissertation. 2014, ISSN 1863-852X, S. 129 (bund.de [PDF; abgerufen am 28. Mai 2021]).
- Verordnung (EU) 2019/1021 des Europäischen Parlaments und des Rates vom 20. Juni 2019 über persistente organische Schadstoffe (Neufassung)
- Chemikalien-Risikoreduktions-Verordnung, Anhang 1.16
