Osteogenesis imperfecta
Osteogenesis imperfecta (Abkürzung OI; altgriechisch ὀστέον ostéon, deutsch ‚Knochen‘, γένεσις génesis, deutsch ‚Entstehung‘ und lateinisch imperfecta ‚unvollkommen‘) wird umgangssprachlich auch als Glasknochenkrankheit bezeichnet, da die Knochen leicht zerbrechlich sind und im Röntgenbild eine glasige Struktur aufweisen. Die OI ist eine seltene Erbkrankheit, für die überwiegend autosomal-dominante, seltener auch autosomal-rezessive Erbgänge beschrieben sind. Hauptmerkmal der OI ist das veränderte Kollagen vom Typ I, was zu einer abnorm hohen Knochenbrüchigkeit mit unterschiedlichen Krankheitsbildern führt.
| Klassifikation nach ICD-10 | |
|---|---|
| Q78.0 | Osteogenesis imperfecta |
| ICD-10 online (WHO-Version 2019) | |
Unter Betroffenen wird der Begriff „Glasknochenkrankheit“ tendenziell abgelehnt, da die OI für sie eher eine Behinderung als eine Erkrankung darstellt. Man spricht in diesem Zusammenhang von „Glasknochen haben“.[1]
Ursache der Kollagenfehlbildung und Häufigkeit
Kollagen Typ I ist Hauptbestandteil des Bindegewebes und damit das wichtigste Protein für den Aufbau der Knochenmatrix. Es lagert sich aus drei linksgängigen alpha-Tropokollagenketten zu einer rechtsgängigen Helix zusammen.
Ursache der OI ist eine Punktmutation in der Erbinformation, welche für das Kollagen Typ I codiert und auf den Chromosomen 7 und 17 liegt. Aufgrund des Austausches der wichtigsten Aminosäure des Kollagens (Glycin, das eine relativ geringe Größe besitzt) durch eine andere – größere – Aminosäure wird die Synthese des Kollagens vermindert. Außerdem wird die richtige „Verdrillung“ der Kollagentripelhelix behindert, wodurch es zum Verlust der Stabilität kommt.
Der Erbgang ist überwiegend autosomal dominant. In der Fachliteratur wird für einzelne Formen auch der rezessive Erbgang beschrieben.[2] Ist keiner der Elternteile selbst betroffen, handelt es sich um eine Spontanmutation.
Die Häufigkeit der Erkrankung wird für alle Formen zusammen weltweit auf ca. 4–7 Fälle pro 100.000 Einwohner geschätzt, so dass man in der Bundesrepublik Deutschland von etwa 2500–4500 Betroffenen ausgeht.[3]
Folgen

Da das Kollagen vom Typ I rund 90 % der Knochenmatrix ausmacht, ist das Hauptmerkmal der OI eine abnorm hohe Knochenbrüchigkeit. Das Synonym Glasknochen beschreibt sehr bildhaft sowohl die mechanischen Eigenschaften des wie Glas leicht zerbrechlichen Knochens als auch das Erscheinungsbild der Knochen auf Röntgenaufnahmen. Da bei der OI nur ungenügend schattengebende Knochensubstanz eingelagert ist, erhöht sich die Strahlentransparenz bei der Röntgenaufnahme, so dass der Knochen oftmals als milchglasähnliche, verwaschene Struktur dargestellt wird.
Darüber hinaus kann noch eine ganze Reihe weiterer Symptome auftreten, die nachfolgend aufgeführt sind:
- extreme Knochenbrüchigkeit
- Blaue Skleren
- Schwerhörigkeit
- Kleinwuchs
- skelettale Deformierungen
- Verbiegung der Wirbelsäule (Skoliose und Kyphose)
- überdehnbare Gelenke
- schwache Muskulatur
- Herzklappenfehlbildungen mit Undichtigkeiten (Insuffizienz)
- offene Herzkammerscheidewand (VSD)[4]
- starkes Schwitzen
- Neigung zu Leistenbrüchen
- Kurzsichtigkeit
- Kautschuk-Kopf (weicher Schädel)
- weite Fontanellen (Bindegewebe zwischen den Schädelnähten)
Keine Auswirkungen hat die Glasknochenkrankheit auf kognitive Fähigkeiten.
Historischer Überblick
Medizinisch ist die OI bereits seit Ende des 17. Jahrhunderts bekannt, wenn auch nur grob-anatomisch, wie wir aus Schriften von Malebranche (1684), Bordenave (1763), Henckel (1772) oder Sandifort (1793) wissen.
1833 veröffentlichte der Straßburger Anatom Johann Friedrich Lobstein (1777–1835) in seinem Lehrbuch der pathologischen Anatomie eine Untersuchung zur Knochenbrüchigkeit bei Erwachsenen. Mit der Bezeichnung der „idiopathic osteopsathyrosis“, in die er auch Symptome der altersbedingten Osteoporose einfließen ließ („Die Osteopsathyrose wird besonders an den beiden Grenzmarken des Lebens in der Kindheit nämlich und im Greisenalter beobachtet.“), prägte er fortan den Begriff der „maladie de Lobstein“.
Dem niederländischen Anatomen Willem Vrolik gelang es 1849 mit der Fallbeschreibung eines Neugeborenen mit weichem Schädeldach und zahlreichen alten wie frischen Frakturen, die angeborene Knochenbrüchigkeit von der Rachitis foetalis zu unterscheiden. Er grenzte die Erkrankung erstmals scharf von dem bisherigen Sammelnamen der Rachitis foetalis, zu der in jener Zeit alle foetalen Entwicklungsstörungen der Knochen eingeordnet wurden, ab und gibt ihr den Namen Osteogenesis imperfecta.
Doch noch immer hielt man die verschiedenen Ausprägungen der OI bei Erwachsenen und Neugeborenen für zwei ganz unterschiedliche Erkrankungen, und es brauchte weitere knapp sechzig Jahre, bis Emil Looser 1906 mit seinen Untersuchungen den endgültigen Beweis erbringen konnte, dass es sich bei den verschiedenen Fällen um ein und dasselbe Krankheitsbild mit unterschiedlichen Ausprägungen handelt. Nachdem es Looser gelungen war, diese ätiologische Verwandtschaft herzustellen, führte er daraufhin die Bezeichnungen Osteogenesis imperfecta congenita (ehemals Typ Vrolik) für die ab der Geburt feststellbare Form und Osteogenesis imperfecta tarda (ehemals Typ Lobstein) für die erst im weiteren Lebensverlauf erkennbare Form ein.
Um die Jahrhundertwende erweiterte sich dank des weiteren diagnostischen Fortschritts das Themengebiet in der Beschreibung der OI. Bezogen sich zuvor gemachte Veröffentlichungen allein auf das Knochensystem, so befassten sich mit Beginn des 20. Jahrhunderts die Autoren zunehmend mit Beschreibungen extraskelettaler Besonderheiten, wie dem Auftreten von blauen Skleren (Adair-Dight, 1912; Gutzeit 1921), der Schwerhörigkeit im frühen Erwachsenenalter (Fischer, 1921), Zahnbildungsstörungen bis hin zur Dentinogenesis imperfecta (Biebl, 1924).
Meist beschränkten sich die Autoren bei ihren Publikationen jedoch auf die Beschreibung einzelner Symptome oder Merkmale der Osteogenesis imperfecta. Erst die 1949 veröffentlichte Dissertation des dänischen Arztes Knud Stakemann Seedorff, die über die rein medizinischen Aspekte hinausgeht, setzte einen wissenschaftlichen Meilenstein in der umfangreichen Beschreibung der OI. Neben einem medizinisch ausführlichen anamnestischen Teil, den er mit radiologischen Abbildungen ergänzte, beschrieb Seedorff vor allem auch den beruflich-sozialen Hintergrund der von ihm untersuchten 180 OI-Betroffenen sehr umfangreich. Erstmals machte er auch eine Angabe über die Häufigkeit der OI: „In diesem Land wird jedes Jahr ein Kind mit dieser Erkrankung geboren.“.
Verlaufsformen
Die 1979 eingeführte 4-Typen-Klassifizierung des australischen Arztes und Genetikers David Sillence wurde im Jahre 2000 durch die Montrealer Wissenschaftsgruppe um Francis H. Glorieux um die OI-Typen V, VI und VII erweitert. Aufgrund der hohen Ausprägungsvariabilität lassen sich jedoch die Betroffenen nicht immer klar einem dieser OI-Typen nach der erweiterten Sillence-Klassifikation zuordnen.
OI Typ I (ehemals Osteogenesis imperfecta tarda, Typ Lobstein)
Synonyme: Adair-Dighton-Syndrom; Milde Osteogenesis imperfecta; Nicht-deformierende Osteogenesis imperfecta; Van der Hoeve-Syndrom[5]
Dies ist die mildeste Form der OI. Sie wird daher häufig erst erkannt, wenn das Kind laufen lernt und sich hierbei Frakturen zuzieht. Häufig wird die OI bei diesen Betroffenen aber auch erst Mitte der dritten Lebensdekade diagnostiziert, wenn beispielsweise der behandelnde Arzt aufgrund degenerativer Beschwerden eine Knochendichtemessung veranlasst oder wenn bei einem Säugling mit OI die Mutter mit untersucht wird. Der Körperbau ist meist normal und Knochenverformungen sind minimal oder fehlen gänzlich. Die Muskelkraft ist gemindert und die Muskulatur nicht selten hypoton. Durch die schwachen Bänder neigen die Gelenke oftmals zur Überstreckbarkeit. Die Sklera kann von weiß über bläulich zu tief blau variieren. Ab dem 20. Lebensjahr können vermehrt Hörprobleme auftreten, welche durch Verkalkung des Steigbügels entstehen. Eine Stapes-Plastik behebt die Schwerhörigkeit nahezu vollständig. Die schwerste Zeit ist wohl die Pubertät (meist zwischen dem 13. und 18. Lebensjahr), mit Beginn des 20. Lebensjahres werden die Knochen aber meist stabiler.
OI Typ II
Sie ist die schwerste Form der OI. Auch wenn dieser OI-Typ durch die unterentwickelte Lungenfunktion, eine hohe Frakturanfälligkeit und seine starken Deformierungen in der Literatur bislang als letal, also nicht überlebensfähig, beschrieben wurde, hat sich die Prognose dank der medizinischen Entwicklung in den letzten Jahren stark verbessert.
OI Typ III (ehemals Osteogenesis imperfecta congenita, Typ Vrolik, oder auch Vrolik-Syndrom)
Die Betroffenen dieses Typs sind kleinwüchsig. Mit der geringsten Körpergröße und der höchsten Neigung zu Deformierungen und Brüchen der Knochen gehören sie in der Typisierung nach dem Typ II zur Extremform unter den OI-Betroffenen, was häufig den Gebrauch eines Rollstuhls erforderlich macht. Neben den Extremitäten können der Schädel, der Brustkorb und die Wirbelsäule in unterschiedlicher Ausprägung verformt sein, weshalb es auch zu Problemen beim Atmen kommen kann.
OI Typ IV
Betroffene dieses Typs sind ebenfalls kleinwüchsig, meist jedoch leichter betroffen als bei dem Typ III und somit häufiger Fußgänger. Die Skleren sind normal bis leicht bläulich. Die Neigung zu Frakturen und Verformungen der Knochen ist häufig geringer als bei Typ III. Es ist nicht zwingend ein Rollstuhl notwendig.
OI Typ V
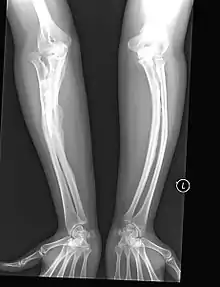
Betroffene dieses Typs neigen zum seltenen Phänomen des sogenannten hyperplastischen Kallus (Callus luxurians), einer spontan überschießenden Kallusbildung ohne eine hierfür übliche Fraktur mit anschließender Verknöcherung. Durch Einlagerung von Calciumsalzen in die bindegewebigen Strukturen (Syndesmosen) zwischen den beiden Unterarmknochen Elle und Speiche sowie den Unterschenkelknochen Schien- und Wadenbein (Calcifizierung der Membranae interosseae antebrachii et cruris) ist die Ein- und Auswärtsdrehung (Pronation/Supination) des Unterarms bzw. des Unterschenkels der Betroffenen erheblich blockiert, was zur klinischen Differentialdiagnose hilfreich ist, sofern die Bewegungseinschränkungen nicht auf Deformierungen der entsprechenden Knochen oder Gelenke beruhen.
OI Typ VI
Obwohl Betroffene dieses OI-Typs klassische klinische Symptome der OI zeigen, konnte bislang keinerlei Mutation auf den hierfür bekannten Kollagen-Genen nachgewiesen werden. Die Skleren sind normal bis leicht bläulich. Keine Dentinogenesis imperfecta. Der Blutspiegel der alkalischen Phosphatase (ein Enzym, das die Osteoblastenaktivität beschreibt) ist leicht erhöht.
OI Typ VII
Beim OI-Typ VII liegt eine Verkürzung der proximalen Extremitäten, also der Oberarme und -schenkel, im Verhältnis zu den distalen Extremitäten (Unterarme und -schenkel) vor. Diese als Rhizomelie bezeichnete Besonderheit ist bislang nur bei OI-Betroffenen aus einer Gruppe von Angehörigen der First Nations in Québec aufgetreten.
Behandlungsmethoden
Da die OI eine genetisch bedingte Störung ist, beschränken sich die möglichen Therapieformen auf rein symptomatische Behandlungsmethoden.
Zu diesen gehören insbesondere:
- die Marknagelung
- die Physiotherapie
- die Bisphosphonattherapie
Marknagelung
Bei der Marknagelung wird der gebogene Knochen zunächst mehrfach osteotomiert, um dann die einzelnen Knochensegmente wieder perlenschnurartig auf den Marknagel aufzufädeln. Anfangs wurden hierfür starre Nägel verwendet. Im wachsenden Knochen mussten diese Nägel allerdings immer wieder ausgetauscht werden, da der Knochen irgendwann länger als der Nagel wurde und der Nagel dadurch den Knochen nicht mehr stützen konnte. Die Folge waren Frakturen in diesen ungeschützten Bereichen. Darum konstruierten 1963 die beiden Orthopäden Bailey und Dubrow einen Teleskopmarknagel. Beim Knochenwachstum ziehen sich die beiden Nagelsegmente teleskopartig auseinander und „wachsen“ so quasi mit.
- Indikationen für eine Marknagelung sind neben häufigen Frakturen an ein und demselben Knochen Pseudarthrosen und mittelgradige bis schwere Fehlstellungen mit funktioneller Beeinträchtigung der Gliedmaßen.
- Kontraindikationen sind unter anderem ein schlechter Allgemeinzustand, eine kardiorespiratorische Insuffizienz oder das Fehlen von Verankerungsmöglichkeiten des Nagels im Knochen aufgrund mangelnder Knochensubstanz.
Physiotherapie
Etwa seit Anfang der siebziger Jahre wurde der Physiotherapie in der OI-Behandlung eine immer größere Rolle zugeschrieben. Hatte man in den Jahren zuvor durch Ruhigstellung (Immobilisierung) versucht, möglichst keine Frakturen zu provozieren, wusste man nun, dass eine Immobilisierung zum vermehrten Knochenabbau führt. Auch die Behandlungsmethoden für OI-Betroffene wurden in den darauf folgenden Jahren, wenn auch langsam, dieser Erkenntnis angepasst und die Betroffenen zu mehr Aktivität aufgefordert. Ein einheitliches physiotherapeutisches Behandlungskonzept für die OI gibt es bislang nicht. Um hier den Betroffenen als auch den Therapeuten eine Hilfe an die Hand zu geben, veröffentlichte die Deutsche Gesellschaft für Osteogenesis imperfecta Betroffene 1997 das von Willy Hagelstein entwickelte Bewegungsprogramm Glasfit.
Bisphosphonattherapie
Die jüngste der drei Therapiesäulen bildet die Säule der medikamentösen Behandlung mit Bisphosphonaten. Erste Publikationen über die Therapie von OI-Betroffenen mit Bisphosphonaten wurden auf der 6. Internationalen wissenschaftlichen Konferenz zur OI in Holland im Jahr 1996 veröffentlicht. Alle Wissenschaftsgruppen konnten zwar einen wesentlichen Knochenzuwachs messen, offen blieb aber die Frage, ob mit der erhöhten Knochendichte auch eine verringerte Frakturrate einhergehen würde. In einer sehr umfangreichen Studie gelang es 1998 dann dem Montrealer Arzt und Wissenschaftler Francis H. Glorieux und seinen Mitarbeitern, den Zusammenhang zwischen Knochendichteerhöhung und Abnahme der Frakturrate aufzuzeigen. Mittlerweile gehört die medikamentöse Therapie mit Bisphosphonaten zum Stand der Wissenschaft bei der Behandlung der OI.
Differentialdiagnose
Abzugrenzen sind die seltene Idiopathische juvenile Osteoporose, ferner die Achondrogenesie Typ II gegen den Typ II sowie auch die Achondrogenesie Typ IA und die Achondrogenesie Typ IB sowie das Osteoporose-Pseudoglioma-Syndrom.[6]
Osteogenesis imperfecta bei Tieren
Die Glasknochenkrankheit wurde bislang bei Hunden, Katzen, Schafen und Rindern beschrieben. Genetisch handelt es sich um eine variable Erkrankung, die Pathophysiologie gleicht jedoch der Osteogenesis imperfecta des Menschen. Bei Dackeln liegt meist eine Mutation im SERPINH1-Gen zugrunde, bei einem Retriever und einem Beagle wurde dagegen jeweils eine COL1A1-Genmutation nachgewiesen.[7]
Siehe auch
Quellen
- F. H. Glorieux, F. Rauch, H. Plotkin, L. Ward, R. Travers, P. Roughley, L. Lalic, D. F. Glorieux, F. Fassier, N. J. Bishop: Typ V osteogenesis imperfecta: a new form of brittle bone disease. In: J Bone Miner Res. 2000; 15, S. 1650–1658.
- F. H. Glorieux, N. J. Bishop, H. Plotkin, G. Chabot, G. Lanoue, R. Travers: Cyclic administration of Pamidronate in Children with severe Osteogenesis imperfecta. In: The New England Journal of Medicine. 1998, Volume 339, S. 947–952.
- F. H. Glorieux, L. M. Ward, F. Rauch, L. Lalic, P. J. Roughley, R. Travers: Osteogenesis imperfecta type VI: a form of brittle bone disease with a mineralization defect. In: J Bone Miner Res. 2002 Jan;17(1), S. 30–38.
- Willy Hagelstein, Hartwig Lehmann, Renate Mücke, Angela Stadtlander: Glasfit – Ein Bewegungsprogramm für Osteogenesis Imperfecta Betroffene. Hrsg.: Deutsche Gesellschaft für Osteogenesis Imperfecta Betroffene e. V., 1997.
- Willy Hagelstein, Kerstin Neumann: Glasfit² – mit dem Theraband und im Wasser. Hrsg.: Deutsche Gesellschaft für Osteogenesis Imperfecta Betroffene e. V., 2001.
- Knud Stakemann Seedorff: Osteogenesis imperfecta. Dissertation. Aarhus Stiftsbogtrykkerie, 1949.
- David O. Sillence u. a.: Genetic heterogeneity in osteogenesis imperfecta. In: Journal of Medical Genetics. 16(2) (1979), S. 101–116.
- Hartmut Stöß: Pathologische Anatomie der Osteogenesis imperfecta. Gustav Fischer Verlag, Stuttgart 1990, ISBN 3-437-11282-1, S. 5.
Weblinks
Einzelnachweise
- Gesundipedia: Osteogenesis imperfecta
- Heike Hoyer Kuhn, Oliver Semler: Osteogenesis imperfecta: Neues zur Pathogenese und Therapie. In: pädiatrie hautnah, 2013, 25 (1) S. 28–32, oi-gesellschaft.de (PDF; 1,2 MB).
- H. Stöß: Pathologische Anatomie der Osteogenesis imperfecta. Gustav Fischer Verlag, Stuttgart 1990, ISBN 3-437-11282-1, S. 5.
- V. Ewerbeck, C.-J. Wirth: Orthopäde. Springer Verlag, Heft Nr. 87; ISSN 0085-4530
- Osteogenesis imperfecta Typ 1. In: Orphanet (Datenbank für seltene Krankheiten).
- Osteoporose-Pseudoglioma-Syndrom. In: Orphanet (Datenbank für seltene Krankheiten).
- Ekkehard Schütz u. a.: Osteogenesis imperfecta beim Dackel. In: Kleintierpraxis. 57 (2012), S. 57–62.