Nitroethan
Nitroethan ist eine gesundheitsschädliche chemische Verbindung, die bei Raumtemperatur als farblose Flüssigkeit vorliegt. Sie besitzt eine Zündtemperatur von 410 °C und einen Flammpunkt von 28 °C.[2]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
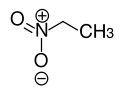 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Nitroethan | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C2H5NO2 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit angenehmem Geruch[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 75,07 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
1,05 g·cm−3 (20 °C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
115 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| pKS-Wert |
8,46 (25 °C)[3] | |||||||||||||||
| Löslichkeit |
löslich in Wasser (45 g·l−1 bei 20 °C)[2] | |||||||||||||||
| Brechungsindex |
1,3917 (20 °C)[4] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−143,9 kJ/mol[7] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Verwendung
Nitroethan wird in der organischen Chemie zur Synthese verschiedenster Stoffe benötigt, da das an die Nitrogruppe gebundene Kohlenstoffatom durch die Mesomeriestabilisierung des Anions einen aciden Charakter besitzt. So bilden Nitroalkane mit Basen Salze. Eine der wichtigsten Reaktionen ist hierbei die Henry-Reaktion; je nach Bedingungen lassen sich Nitroalkene oder Nitroalkohole bilden. Diese Reaktion ist eine wichtige Möglichkeit zur Knüpfung von C–C-Bindungen. Zudem eignet sich Nitroethan als Speziallösemittel. Im Nageldesign findet Nitroethan als Feilhilfe Verwendung.
Einzelnachweise
- Eintrag zu NITROETHANE in der CosIng-Datenbank der EU-Kommission, abgerufen am 23. Oktober 2021.
- Eintrag zu Nitroethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Dissociation Constants of Organic Acids and Bases, S. 8-42.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-390.
- Eintrag zu Nitroethane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 79-24-3 bzw. Nitroethan), abgerufen am 2. November 2015.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-22.

