Nefazodon
Nefazodon ist ein zur Klasse der dualserotonergen Antidepressiva (DSA) gehörendes Antidepressivum. Es ist ein Phenylpiperazin-Derivat, das strukturell und teilweise auch in seiner Wirkungsweise dem schon länger bekannten Antidepressivum Trazodon ähnelt.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
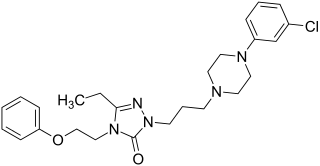 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Nefazodon | |||||||||||||||
| Andere Namen |
1-{3-[4-(3-Chlorphenyl)piperazin-1-yl]propyl}-3-ethyl-4-(2-phenoxyethyl)-4,5-dihydro-1,2,4-triazol-5-on | |||||||||||||||
| Summenformel | C25H32ClN5O2 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code |
N06AX06 | |||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Wirkmechanismus | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 470,01 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Wirkungsweise
Die antidepressive Wirkung des Nefazodon erfolgt über zwei Mechanismen. Es blockiert einerseits den Serotonin-5-HT2A-Rezeptor und andererseits, in geringem Ausmaß, auch die präsynaptische Wiederaufnahme von Serotonin.
Nefazodon hat keine signifikante Affinität zu α- oder β-Adrenozeptoren sowie Histamin-, Dopamin- und Acetylcholin-Rezeptoren.
Geschichte
In Deutschland wurde es ab 1997 von Bristol-Myers Squibb unter der Bezeichnung Nefadar vertrieben, in den USA war es unter der Bezeichnung Serzone erhältlich.
Wegen einiger Fälle von schwerem Leberversagen wurde das Medikament 2003 wieder vom Markt genommen.
Einzelnachweise
- Eintrag zu Nefazodon. In: Römpp Online. Georg Thieme Verlag, abgerufen am 22. Dezember 2014.
- Datenblatt Nefazodone hydrochloride bei Sigma-Aldrich, abgerufen am 15. Juni 2011 (PDF).