Pyridoxal
Pyridoxal ist eine feste, wasserlösliche chemische Verbindung, die als lebensnotwendige Verbindung zu den Vitaminen zählt.
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
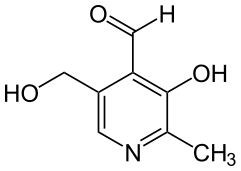 | |||||||
| Allgemeines | |||||||
| Trivialname | Pyridoxal | ||||||
| Andere Namen |
| ||||||
| Summenformel | C8H9NO3 | ||||||
| CAS-Nummer | |||||||
| PubChem | 1050 | ||||||
| DrugBank | DB00147 | ||||||
| Kurzbeschreibung | weißer Feststoff (Hydrochlorid)[1] | ||||||
| Vorkommen | ubiquitär | ||||||
| Physiologie | |||||||
| Funktion | Coenzym bei verschiedenen enzymatischen Reaktionen, vor allem mit Aldehydfunktionen | ||||||
| Täglicher Bedarf | 1,6–1,8 mg | ||||||
| Folgen bei Mangel | Durchfall und Erbrechen, Dermatitis, Krampfzustände, neurologische Störungen, Epileptische Anfälle | ||||||
| Überdosis | >500 mg·d−1 | ||||||
| Eigenschaften | |||||||
| Molare Masse | 167,16 g·mol−1 | ||||||
| Aggregatzustand | fest[1] | ||||||
| Schmelzpunkt | |||||||
| Löslichkeit | 500 g/L[2] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Zusammen mit Pyridoxin und Pyridoxamin sowie deren phosphorylierte Derivate, die in vivo leicht ineinander umgewandelt werden, bilden sie die Gruppe Vitamin B6. Die aktive Form der Vitamin-B6-Gruppe heißt Pyridoxalphosphat.
Pyridoxal wurde erstmals 1944 von Karl August Folkers, der auch wesentlich an der Strukturaufklärung mitgewirkt hatte, synthetisiert.[3]
Biologische Bedeutung
Pyridoxal ist besonders im tierischen Gewebe enthalten.[4]
Einige medizinisch relevante Bakterien benötigen Pyridoxal zum wachsen. Dieses ernährungsbedingte Verlangen kann zur Folge haben, dass einige Bakterien nur in der Nähe anderer Bakterienstämme leben können, welche Pyridoxal produzieren.
Pyridoxal war an der Großen Sauerstoffkatastrophe beteiligt, welche den Tod zahlreicher anaerobischer Lebewesen bedeutete.[5]
Weblinks
Einzelnachweise
- Datenblatt Pyridoxal hydrochloride, ≥99% (HPLC) bei Sigma-Aldrich, abgerufen am 26. Mai 2019 (PDF).
- COFFEN,DL (1978)
- R. E. Olson: Karl August Folkers (1906–1997). In: Journal of Nutrition. 131, Nr. 9, 1. September 2001, S. 2227–2230. PMID 11533258.
- Ermin Welzl: Biochemie der Ernährung. Walter de Gruyter, 1985, ISBN 978-3-11-085431-2, S. 231 (eingeschränkte Vorschau in der Google-Buchsuche).
- Kyung Mo Kim et al.: Protein domain structure uncovers the origin of aerobic metabolism and the rise of planetary oxygen. In: Structure (London, England: 1993). Band 20, Nr. 1, 11. Januar 2012, S. 67–76, doi:10.1016/j.str.2011.11.003, PMID 22244756.