Marschalk-Reaktion
Die Marschalk-Reaktion ist eine Namensreaktion der organischen Chemie, die 1936 von Charles Henri Marschalk (1885–1968) entdeckt wurde.[1] Es handelt sich um die Reaktion eines phenolischen Anthrachinons zu einem substituierten phenolischen Anthrachinon.[2]
Übersichtsreaktion
Die Marschalk-Reaktion erfolgt in mehreren Reaktionsschritten. Dabei wird ein phenolisches Anthrachinon durch ein Aldehyd in der ortho-Position zu der phenolischen Hydroxygruppe substituiert:[3]
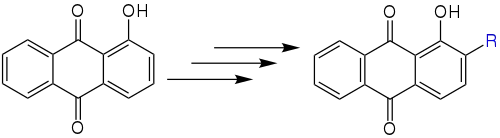
Anstelle der Hydroxygruppe kann es sich auch um ein Anthrachinon mit einer Aminogruppe handeln:[3]
.svg.png.webp)
Reaktionsmechanismus
Im vorgeschlagenen Reaktionsmechanismus steht zunächst das Anthrachinon 1 im Redoxgleichgewicht zu seinem Anthrachinol 2. Dieses Molekül wird nun durch ein Hydroxyd-Ion deprotoniert. Das gebildete Enolat-Ion 3 greift jetzt wie in einer Aldoladdition den Aldehyd nucleophil an. Es bildet sich das Alkoholat 4, welches protoniert wird. Dadurch entsteht das Aldol 5. Es folgt nach einer Aldolkondensation die Deprotonierung des aciden Wasserstoffatoms durch eine Base. Es bildet sich eine C-C-Doppelbindung aus und ein Hydroxid-Ion geht als Fluchtgruppe ab. Zum Schluss wird das Zwischenprodukt 6 zum Anthrachinon reoxidiert und es entsteht das substituierte Produkt 7.[3]

Beispielreaktion
Das Ausgangs-Anthrachinon kann ggf. zusätzlich substituiert sein. Die Marschalk-Reaktion läuft mit verschiedenen Aldehyden ab. Dies ist zum Beispiel bei der folgenden Reaktion mit Formaldehyd der Fall:[4]
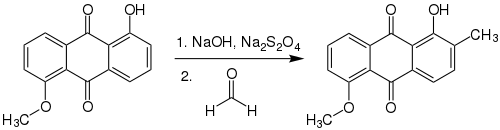
Modifikation
Die Marschalk-Reaktion kann auch zweimal an einem Molekül durchgeführt werden, sodass zwei verschiedene Seitenketten hinzugefügt werden. Dafür müssen die Seitenketten jedoch in richtiger Reihenfolge hinzugefügt werden, da unter normalen Reaktionsbedingungen kein höherer aliphatischer oder aromatischer Aldehyd als zweite vicinale Alkylgruppe mehr eingeführt werden kann. Dadurch ist mit der Marschalk-Reaktion auch eine selektive Monoalkylierung möglich.[1][5]
Die Verwendung verschiedener Aldehyde wurde untersucht, um zu prüfen ob die sterische Hinderung bei der Marschalk-Reaktion eine Rolle spielt. So konnten Unterschiede bei gleichen Reaktionsbedingungen festgestellt werden, jedoch konnte die sterische Hinderung z. B. bei Pivalaldehyd durch eine höhere Reaktionstempereratur überwunden werden.[4]
Anwendung
Die Marschalk-Reaktion kann angewandt werden um Derivate wie 4-Demethoxydaunomycinon herzustellen, welche für die Chemotherapie von Krebs benötigt werden.[6]
Einzelnachweise
- L. A. Mitscher, Tzay-Shiang Wu, Ish Khanna: A useful extension of the Marschalk reaction directed toward synthesis of 11-deoxydoxorubicin antitumor antibiotics. In: Tetrahedron Letters. Band 24, Nr. 44, 1. Januar 1983, S. 4809–4812, doi:10.1016/S0040-4039(00)94013-9 (sciencedirect.com [abgerufen am 22. Mai 2019]).
- C. Marschalk et al., Bulletin de la Société Chimique de France 3, 1545 (1936)
- Ellerd, Michael G., Favaloro, Frank G.: Name reactions and reagents in organic synthesis. 2nd ed Auflage. Wiley, Hoboken, N.J. 2005, ISBN 0-471-22854-0, S. 410.
- Karsten Krohn, Wolfgang Baltus: Synthesis of rac- and ent-fridamycin E. In: Tetrahedron. Band 44, Nr. 1, 1. Januar 1988, S. 49–54, doi:10.1016/S0040-4020(01)85091-2 (sciencedirect.com [abgerufen am 28. Mai 2019]).
- K. Krohn: Synthesis of anthracyclinones by electrophilic and nucleophilic addition to anthraquinones. In: Tetrahedron. Band 46, Nr. 2, 1. Januar 1990, S. 219–318, doi:10.1016/S0040-4020(01)85414-4 (sciencedirect.com [abgerufen am 28. Mai 2019]).
- A. B. Argade, A. R. Mehendale, N. R. Ayyangar: Marschalk reaction approach for a simple synthesis of (±)4-demethoxydaunomycinone. In: Tetrahedron Letters. Band 27, Nr. 30, 1. Januar 1986, S. 3529–3532, doi:10.1016/S0040-4039(00)84841-8 (sciencedirect.com [abgerufen am 28. Mai 2019]).