Magnesiumsilicid
Magnesiumsilicid ist eine anorganische chemische Verbindung des Magnesiums aus der Gruppe der Silicide.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
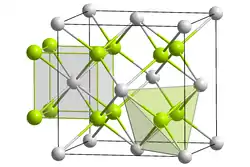 | ||||||||||||||||
| _ Mg2+ _ Si4− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Magnesiumsilicid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | Mg2Si | |||||||||||||||
| Kurzbeschreibung |
schieferblauer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 76,70 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Dichte |
1,94 g·cm−3[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
reagiert heftig mit Wasser[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Magnesiumsilicid kann durch Reaktion von Magnesium mit Silicium gewonnen werden.[5]
Ebenfalls möglich ist die Darstellung durch Reaktion von Siliciumdioxid mit Magnesium.[1]
Phasenreines Magnesiumsilicid kann aus Magnesiumhydrid und Silicium mit Hilfe des SPS-Verfahrens erzeugt werden.[4]
Eigenschaften
Magnesiumsilicid ist ein Feststoff mit harten und sehr spröden, schieferblauen Kristallen.[1] Es stellt eine Zintl-Phase dar und wurde erstmals 1858 von Friedrich Wöhler erwähnt. Genauer wurde die Verbindung erstmals von Paul Lebeau und Robert Bossuet im Jahre 1908 untersucht, denen die Reinstdarstellung von Magnesiumsilicid gelang.[6] Mit Wasser reagiert es heftig unter Bildung hochentzündlicher Gase.[2] Über 723 K reagiert die Verbindung an Luft mit Sauerstoff zu Magnesiumoxid und Silicium.[7] Es besitzt eine Kristallstruktur vom Antifluorit-Typ (a=6,39 Å) mit der Raumgruppe Fm3m (Raumgruppen-Nr. 225) und ist ein n-Halbleiter (genauer ein Eigenhalbleiter), der den Verbindungshalbleitern zugeordnet wird. Unterhalb von 230 °C zeigt Magnesiumsilicid ein sprödes Materialverhalten, darüber wird es plastisch. Die Bruchfestigkeit der Einkristalle sinkt mit steigender Temperatur von 100 MPa bei Raumtemperatur auf 10 MPa bei 630 °C.[4] Es ist gegen Laugen beständig, Säuren dagegen zersetzen es unter Bildung von Siliciumwasserstoffen (Silane) und Wasserstoff. So bildet sich bei Kontakt mit Salzsäure Magnesiumchlorid und Monosilan.[1][8]
Verwendung
Magnesiumsilicid wird zur Herstellung von Silanen sowie zur Eigenschaftsverbesserung von Magnesium- und Aluminium-Legierungen verwendet.[4][9] In Aluminiumlegierungen erhöhen sie die Festigkeit durch Ausscheidungshärtung; sie können also zunächst im weichen Zustand bearbeitet werden und erst anschließend durch eine Wärmebehandlung gehärtet werden. Die wichtigsten Legierungsgruppen sind die Aluminium-Silicium-Legierungen und die Aluminium-Magnesium-Silicium-Legierungen.
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 916.
- Datenblatt Magnesium silicide, ≥99% trace metals basis, −20 mesh bei Sigma-Aldrich, abgerufen am 7. November 2021 (PDF).
- americanelements: Magnesium Silicide
- Nikolaus Reinfried; Modifizierung der Werkstoffe auf Basis von Magnesiumsilicid mit Hilfe der Spark-Plasma-Synthese, 15. März 2006, urn:nbn:de:swb:14-1176195464803-87414
- Kevin Hutchings: Classic Chemistry Experiments. Royal Society of Chemistry, 2000, ISBN 0-85404-919-3, S. 181 (eingeschränkte Vorschau in der Google-Buchsuche).
- Inorganic chemistry. In: Journal of the Chemical Society, Abstracts. 94, 1908, S. B172–B200, doi:10.1039/CA9089405172, hier: S. B184.
- J. Tani, M. Takahashi, H. Kido: Thermoelectric properties and oxidation behaviour of Magnesium Silicide. In: IOP Conference Series: Materials Science and Engineering. 18, 2011, S. 142013, doi:10.1088/1757-899X/18/14/142013.
- Seilnacht: Periodensystem: Silicium
- Edward Ghali: Corrosion Resistance of Aluminum and Magnesium Alloys: Understanding ... John Wiley & Sons, 2010, ISBN 0-470-53176-2, S. 139 (eingeschränkte Vorschau in der Google-Buchsuche).
