Lithiummolybdat
Lithiummolybdat, Li2MoO4 ist eine chemische Verbindung des Lithiums aus der Gruppe der Molybdate.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
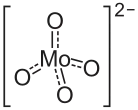 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Lithiummolybdat | ||||||||||||||||||
| Andere Namen |
Dilithiummolybdat | ||||||||||||||||||
| Summenformel | Li2MoO4 | ||||||||||||||||||
| Kurzbeschreibung |
gebrochen-weißes Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 173,82 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,66 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt |
705 °C[1] | ||||||||||||||||||
| Löslichkeit |
Löslich in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Gelöstes Lithiumhydroxid reagiert mit Molybdän(VI)-oxid zu Lithiummolybdat.
Die Reaktion kann nicht mit ungelöstem Lithiumhydroxid erfolgen.[3]
Verwendung
Die Verbindung wird zur Stahlbeschichtung und als Erdöl-Crackkatalysator verwendet.[4]
Eigenschaften
Der Schmelzpunkt des Salzes liegt bei 705 °C und die Dichte bei 2,66 g·cm−3.[1][2] Es besitzt eine Phenakit-ähnliche Struktur.[3]
Sicherheitshinweise
Das Salz kann die Haut, die Atemwege und die Augen teils schwer reizen.[1][2]
Lithiummolybdat reagiert mit starken Säuren und Basen heftig.[1]
Literatur
- P.A.G.O'Hare, Kenneth J. Jensen, H. R. Hoekstra: Thermochemistry of molybdates IV. Standard enthalpy of formation of lithium molybdate, thermodynamic properties of the aqueous molybdate ion, and thermodynamic stabilities of the alkali-metal molybdates. Elsevier, Juli 1974, doi:10.1016/0021-9614(74)90118-9.
Einzelnachweise
- Datenblatt Lithium molybdenum oxide bei AlfaAesar, abgerufen am 15. März 2019 (PDF) (JavaScript erforderlich).
- Datenblatt Lithium molybdate bei Sigma-Aldrich, abgerufen am 15. März 2019 (PDF).
- Thomas W. S. Yip, Edmund J. Cussen, Claire Wilson: Spontaneous formation of crystalline lithium molybdate from solid reagents at room temperature. In: Dalton Transactions. 2010, doi:10.1039/b908266b.
- Dale L. Perry: Handbook of Inorganic Compounds. Hrsg.: Sidney L. Phillips. CRC Press, 1995, ISBN 0-8493-8671-3, S. 227.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.
