Lindlar-Katalysator
Ein Lindlar-Katalysator ist ein Katalysator zur stereospezifischen Hydrierung von Alkinen zu Alkenen. Beim Lindlar-Katalysator wird Palladium als Katalysator und Calciumcarbonat als Trägerstoff eingesetzt. Der Wasserstoff wird gasförmig in den Reaktor gegeben. Um die weitere Hydrierung zum Alkan zu verhindern, wird Bleiacetat (oder Blei(II)-oxid) als Katalysatorgift eingesetzt. Dadurch wird die Reaktivität soweit gemindert, dass das Alken nicht weiter reagiert. Der Katalysator ist nach Herbert Lindlar (Hoffmann-La Roche) benannt.
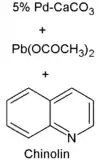
Herstellung
Nach der Beschreibung des Erfinders[1][2] wird der Katalysator durch Reduktion von Palladium(II)-chlorid in einer Anschlämmung von Calciumcarbonat hergestellt. Eine erste Deaktivierung erfolgt durch Zugabe von Bleiacetat, danach wird mit Chinolin weiter deaktiviert, was die Selektivität nochmals steigert. Die selektive Hydrierung eines Alkins zu einem Styrolderivat ist beschrieben.[1]
Eigenschaften
Der Lindlar-Katalysator (auch als Palladium auf Calciumcarbonat, vergiftet bezeichnet) ist ein dunkelgrauer Feststoff.[3] Bei der Hydrierung von Alkinen mit Lindlar-Katalysatoren entstehen stets cis-Alkene, da im ersten Reaktionsschritt das Alkin an dem metallischen Palladium gebunden wird. Danach wird im zweiten Schritt ein H2-Molekül direkt an die Dreifachbindung in einer elektrophilen Additionsreaktion gebunden. Dadurch werden beide Wasserstoffatome gleichzeitig und auf derselben Seite der Doppelbindung addiert. Anschließend löst sich das entstandene Alken vom Palladium.[4]
Verwendung
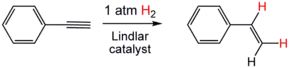
Beispiele sind die Reaktion von Phenylacetylen zu Styrol oder auch die Synthese von Vitamin A, bei der eine Dreifachbindung mit einem Lindlar-Katalysator selektiv zu einem (Z)-Alken hydriert wird.
Recycling
Das Recyclen dieses Katalysators gestaltet sich mitunter schwierig, weil er thermisch aufbereitet werden muss. Die dabei entstehenden Abgase enthalten teilweise giftige Bleioxide, die manche Wäschersysteme nicht zurückhalten können. Daher müssen zusätzliche Chemikalien in den Wäscherkreislauf geführt werden, die Schwermetalle (z. B. Blei oder Quecksilber) ausfällen können.
Literatur
- Jan Bülle, Aloys Hüttermann: Das Basiswissen der organischen Chemie die wichtigsten organischen Reaktionen im Labor und in der Natur. Thieme, Stuttgart 2000, ISBN 978-3-527-30847-7, S. 466.
Einzelnachweise
- Lindlar, H.; Dubuis, R.: Palladium Catalyst for Partial Reduction of Acetylenes In: Organic Syntheses. 46, 1966, S. 89, doi:10.15227/orgsyn.046.0089; Coll. Vol. 5, 1973, S. 880 (PDF).
- Lindlar, H. Ein neuer Katalysator für selektive Hydrierungen. In: Helv Chim Acta 1952, 35, S. 446–450. doi:10.1002/hlca.19520350205.
- Datenblatt Lindlar-Katalysator bei Sigma-Aldrich, abgerufen am 14. Juni 2011 (PDF).
- Overman, L. E.; Brown, M. J.; McCann, S. F.: (Z)-4-(Trimethylsilyl)-3-Buten-1-ol In: Organic Syntheses. 68, 1990, S. 182, doi:10.15227/orgsyn.068.0182; Coll. Vol. 8, 1993, S. 609 (PDF).