Kupferwolframat
Kupferwolframat ist eine anorganische chemische Verbindung des Kupfers aus der Gruppe der Wolframate.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
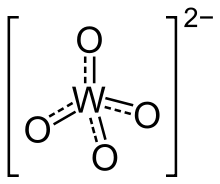 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Kupferwolframat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | CuWO4 | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 311,38 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
7,5 g·cm−3[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Kupferwolframat kann durch Reaktion von Kupfernitrat mit Natriumwolframat in wässriger Lösung gewonnen werden.[6]
Es kann auch durch Reaktion von Kupfer(II)-oxid mit Wolfram(VI)-oxid bei 600 bis 800 °C dargestellt werden.[4]
Eigenschaften
Kupferwolframat ist ein geruchloser gelbbrauner Feststoff, der praktisch unlöslich in Wasser ist.[1] Das Dihydrat ist grünlich und ändert seine Farbe auf braun bis grau-gelb bei Erhitzung über 340 °C unter Kristallwasserabgabe.[4] Das Anhydrat besitzt eine trikline Kristallstruktur, die einer verzerrten Wolframitstruktur ähnelt mit der Raumgruppe P1 (Raumgruppen-Nr. 2) und a = 0,47026 nm, b = 0,58389 nm, c = 0,48784 nm, α = 91,788°, β = 92,469°, γ = 82,805°, Z = 2.[7][8] Das Anhydrat besitzt zwei Hochdruckmodifikationen, die ab etwa 9 und 18 GPa auftreten. Das monokline Dihydrat (Wolframitstruktur) behält seine Kristallstruktur bis mindestens 40 GPa.[9]
Verwendung
Kupferwolframat-Nanopulver wird für Superkondensatoren und als Anodenmaterial in Lithiumionenakkumulatoren (Lithiumchlorat und Lithiumphosphoroxynitrid) eingesetzt. Dünne Schichten aus Kupferwolframat werden für Stickstoffmonoxid-Messungen verwendet.[1] Es wird auch in Atomreaktoren und als Katalysator in der Polyesterherstellung eingesetzt.[3] Es wird auch als Photokatalysator (es ist ein n-Halbleiter mit einer Bandlücke von 2,25 eV) verwendet.[10]
Einzelnachweise
- Datenblatt Copper(II) tungsten oxide, 99.5% (metals basis) bei AlfaAesar, abgerufen am 17. Juni 2016 (PDF) (JavaScript erforderlich).
- William M. Haynes: CRC Handbook of Chemistry and Physics, 94th Edition. CRC Press, 2016, ISBN 978-1-4665-7115-0 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. CRC Press, 2016, ISBN 978-1-4398-1462-8 (eingeschränkte Vorschau in der Google-Buchsuche).
- Gmelin-Institut für Anorganische Chemie und Grenzg: Kupfer: Teil B — Lieferung 3: Verbindungen Kupfer-Lithium bis Kupfer-Eisen Reaktionen der Kupfer-Ionen. Springer-Verlag, 2013, ISBN 978-3-662-13328-6 (eingeschränkte Vorschau in der Google-Buchsuche).
- Felix Machatschki: Spezielle Mineralogie auf geochemischer Grundlage. Springer-Verlag, 2013, ISBN 978-3-7091-8006-8 (eingeschränkte Vorschau in der Google-Buchsuche).
- F. Kosek, J. Horák, J. Kašpar: Leitfähigkeit von Kupferwolframat. In: Collection of Czechoslovak Chemical Communications. Band 24, Nr. 6, 1. Januar 1959, ISSN 1212-6950, S. 2034–2037, doi:10.1135/cccc19592034.
- Kihlborg L., Gebert E.: CuWO4, a distorted Wolframite-type structure. In: Acta Crystallographica Section B: Structural Crystallography and Crystal Chemistry. Band 26, Nr. 7, 15. Juli 1970, doi:10.1107/S0567740870003515.
- formatex.info: Structural refinement and photocatalytic properties of CuWO4 crystals, E.L.S. Souza1, C.J. Dalmaschio2, M.G.R. Filho1, G.E. Luz Jr.1, R.S. Santos1, E. Longo3 and L.S. Cavalcante, 28. August 2014, abgerufen am 17. Juni 2016
- Li Wang, Feng Ke, Qinglin Wang, Jiejuan Yan, Cailong Liu, Xizhe Liu, Yanchun Li, Yonghao Han, Yanzhang Ma, Chunxiao Gao: Effect of crystallization water on the structural and electrical properties of CuWO4 under high pressure. In: Applied Physics Letters. Band 107, Nr. 20, 16. November 2015, S. 201603, doi:10.1063/1.4935978.
- Juan Carlos Colmenares, Yi-Jun Xu: Heterogeneous Photocatalysis: From Fundamentals to Green Applications. Springer, 2016, ISBN 978-3-662-48719-8 (eingeschränkte Vorschau in der Google-Buchsuche).
