Iridium(III)-bromid
Iridium(III)-bromid ist eine anorganische chemische Verbindung des Iridiums aus der Gruppe der Bromide. Neben diesem sind auch ein Iridium(I)-bromid, Iridium(II)-bromid und basische Iridium(III)-bromid-hydrate (Ir(OH)Br3·3H2O) bekannt.[1]
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
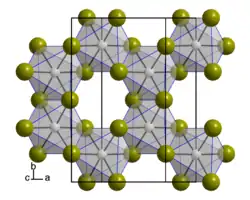 | ||||||||||
| _ Ir3+ _ Br− | ||||||||||
| Allgemeines | ||||||||||
| Name | Iridium(III)-bromid | |||||||||
| Andere Namen |
Iridiumtribromid | |||||||||
| Verhältnisformel | IrBr3 | |||||||||
| Kurzbeschreibung |
dunkelrotbrauner Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 449,94 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
6,82 g·cm−3[2] | |||||||||
| Löslichkeit |
sehr schwer löslich in Wasser, Säuren und Alkalien[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gewinnung und Darstellung
Iridium(III)-bromid kann durch Reaktion von Iridium(II)-bromid mit Brom gewonnen werden. Das Tetrahydrat kann durch Reaktion von Iridium(IV)-oxid-dihydrat mit einer Bromwasserstofflösung.[1] Es kann auch aus den Elementen bei 8 atm und 570 °C dargestellt werden.[4]
Eigenschaften
Iridium(III)-bromid ist ein dunkelrotbrauner Feststoff, der sehr schwer löslich in Wasser, Säuren und Alkalien ist und sich beim Erhitzen in Iridium(II)-bromid zersetzt.[1] Es kristallisiert in einer stark fehlgeordneten Schichtstruktur des Aluminium(III)-chlorid-bzw. Chrom(III)-chlorid-Typs, wobei die monokline Elementarzelle vier Formeleinheiten enthält. Die Fehlordnung ist ebenso wie beim Rhenium(III)-chlorid, Rhenium(III)-bromid, α-Iridium(III)-chlorid und α-Ruthenium(III)-chlorid auf die unterschiedliche Stapelung der Metallschichten zurückzuführen.[5] Das hellolivgrüne Tetrahydrat ist leicht löslich in Wasser, aber unlöslich in Ethanol und Ether. Bei Erwärmung auf 100 °C färbt es sich unter Wasserabgabe dunkelbraun und zersetzt sich bei höheren Temperaturen zu Iridium und Brom.[1]
Einzelnachweise
- H. J. Kandiner: Iridium. Springer-Verlag, 2013, ISBN 978-3-662-12128-3 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. CRC Press, 2016, ISBN 978-1-4398-1462-8, S. 213 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Stanley E. Livingstone: The Chemistry of Ruthenium, Rhodium, Palladium, Osmium, Iridium and Platinum Pergamon Texts in Inorganic Chemistry. Elsevier, 2017, ISBN 978-1-4831-5840-2, S. 1257 (eingeschränkte Vorschau in der Google-Buchsuche).
- K. Brodersen, G. Thiele, H. Ohnsorge, I. Recke, F. Moers: Die Struktur des IrBr3 und über die Ursachen der Fehlordnungserscheinungen bei den in Schichtenstrukturen kristallisierenden Edelmetalltrihalogeniden. In: Journal of the Less Common Metals. 15, 1968, S. 347, doi:10.1016/0022-5088(68)90194-X.