Epimer
In der Chemie werden als Epimere besondere Stereoisomere mit mindestens zwei Stereozentren bezeichnet, die sich in der Konfiguration an nur einem Stereozentrum, mit Ausnahme des letzten asymmetrischen, unterscheiden. Alle anderen Stereozentren in den Molekülen sind, sofern vorhanden, jeweils gleich. Das Anomer ist ein Spezialfall des Epimers, bei dem sich die Konfiguration am anomeren C-Atom ändert (Mutarotation).
In der Nomenklatur wird einem der epimeren Paare das Präfix „epi-“, zum Beispiel bei Chinin und epi-Chinin, hinzugefügt. Wenn es sich bei den Paaren um Enantiomere handelt, wird das Präfix „ent-“ verwendet.
Beispiele
Die Zucker Glucose und Mannose sind Epimere. So unterscheiden sich β-D-Glucopyranose und β-D-Mannopyranose, weil sie nur stereochemisch an der C-2-Position eine unterschiedliche Konfiguration besitzen. Die Hydroxygruppe der β-D-Glucopyranose befindet sich in äquatorialer Position (in der „Ebene“ des Rings), die C-2-Hydroxygruppe der β-D-Mannopyranose hingegen in axialer Position (aus der „Ebene“ des Rings heraus). Da sich die Bilder jedoch nicht spiegeln, handelt es sich hier nicht um Enantiomere, sondern um Epimere:[1]
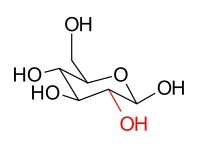 |  |
| β-D-Glucopyranose [enthält fünf Stereozentren, davon ein anomeres Zentrum (rechts)] |
β-D-Mannopyranose |
Ebenso sind D-Erythrose und D-Threose Epimere. Auch cis-Dekalon und trans-Dekalon sind Epimere, wobei letzteres stabiler ist:
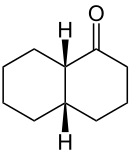 |  |
| cis-Dekalon (enthält zwei Stereozentren) |
trans-Dekalon |
Doxorubicin und Epirubicin sind zwei eng verwandte Arzneistoffe und Epimere:
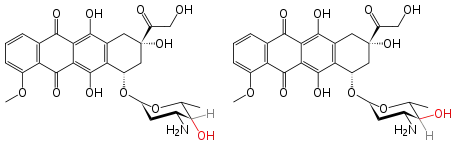 |
| Vergleich von Doxorubicin und Epirubicin |
Andere derartige Verbindungen sind epi-Inositol und Inositol:
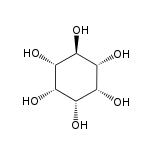 | 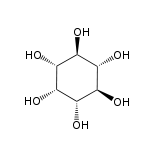 |
| epi-Inositol (enthält sechs Stereozentren) |
Inositol (enthält sechs Stereozentren) |
Weitere Epimere sind Lipoxin und epi-Lipoxin:
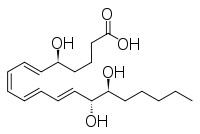 | 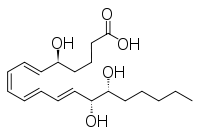 |
| Lipoxin | epi-Lipoxin |
Testosteron und 17-epi-Testosteron sind ebenfalls Epimere:
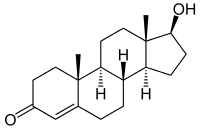 | 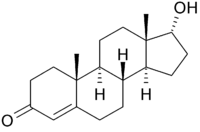 |
| Testosteron (enthält sechs Stereozentren) |
17-epi-Testosteron (enthält sechs Stereozentren) |
Epimerisierung
Epimerisierung ist ein chemischer Prozess, bei dem ein Epimer in sein chirales Gegenstück umgewandelt wird. Ein Beispiel hierfür wäre die kondensierte Tannin-Depolymerisation. Epimerisierung kann spontan sein (im Allgemeinen ein langsamer Prozess) oder durch Enzyme katalysiert werden. Letzteres geschieht bei der Epimerisierung zwischen dem Zucker N-Acetylglucosamin und N-Acetylmannosamin, die durch RENBP, ein Renin-bindenes Protein, katalysiert wird.
Einzelnachweise
- Joachim Buddrus, Bernd Schmidt: Grundlagen der Organischen Chemie. 5. Auflage, de Gruyter Verlag, Berlin 2015, ISBN 978-3-11-030559-3, S. 760–761.