Epimerisierung
Unter Epimerisierung versteht man die Konfigurationsumkehr an einem asymmetrischen Kohlenstoffatom eines Moleküls, das zwei oder mehr asymmetrische Kohlenstoffatome aufweist, wobei die Konfiguration der anderen asymmetrischen Kohlenstoffatome erhalten bleibt. Epimere sind Diastereomere, die sich in der Konfiguration von nur einem Stereozentrum unterscheiden.
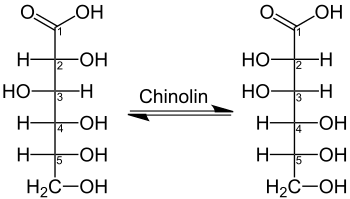
Epimerisierung von D-Gluconsäure (links) in die diastereomere D-Mannonsäure (rechts) unter dem Einfluss von Chinolin. Die beiden epimeren Onsäuren bilden ein Gleichgewicht. D-Mannonsäure geht zum Teil in D-Gluconsäure über und umgekehrt.[1]
cis-Dekalon und trans-Dekalon sind Epimere, wobei letzteres stabiler ist. Die Epimerisierung erfolgt in der α-Position zur Carbonylgruppe.[2]
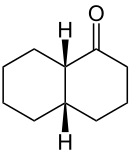 |  |
| cis-Dekalon | trans-Dekalon |
Die Epimerisierung wurde 1890 von Emil Fischer beim Erhitzen von D-Gluconsäure mit Chinolin beobachtet. Als Reaktionsprodukt wurde die am C2-Kohlenstoff epimerisierte D-Mannonsäure erhalten.[3]
Einzelnachweise
- Hans Beyer, Wolfgang Walter: Organische Chemie. S. Hirzel Verlag, Stuttgart, 1984, ISBN 3-7776-0406-2, S. 401.
- Michael B. Smith: March's advanced organic chemistry. John Wiley & Sons, 7. Auflage, 2013, ISBN 978-0-470-46259-1, S. 667.
- Emil Fischer: Ueber die optischen Isomeren des Traubenzuckers, der Gluconsäure und der Zuckersäure. In: Berichte der deutschen chemischen Gesellschaft. Band 23, Nr. 2, 1. Juni 1890, S. 2611–2624, doi:10.1002/cber.189002302157.
Weblinks
- Eintrag zu epimerization. In: IUPAC (Hrsg.): Compendium of Chemical Terminology. The “Gold Book”. doi:10.1351/goldbook.E02166 – Version: 2.3.3.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.