Donnan-Gleichgewicht
Das Donnan-Gleichgewicht beschreibt in der Physikalischen Chemie die ungleiche Verteilung von gelösten geladenen Teilchen (Ionen), die sich einstellt, wenn eine semipermeable Membran für das Lösungsmittel und einige, nicht aber alle in der Lösung vorhandenen Ionen durchlässig ist. In diesem Fall verteilen sich die passierenden Ionen auf beiden Seiten der Membran in unterschiedlicher Konzentration. Diese Ungleichverteilung führt zu einer Potentialdifferenz (Donnan-Potential oder besser: Donnan-Spannung) und einer Differenz des osmotischen Drucks (Donnan-Druck). Das Ausmaß der Abweichung wird durch den Donnan-Koeffizient angegeben.
Benannt ist dieser Effekt nach dem Chemiker Frederick George Donnan, der 1911 eine Theorie zur Erklärung solcher Membrangleichgewichte aufgestellt hat. Die Konzentrationsverteilung wird daher als Donnan-Gleichgewicht (auch Gibbs-Donnan-Gleichgewicht), der zugrundeliegende Vorgang als Gibbs-Donnan-Effekt oder Donnan-Gesetz bezeichnet.
Der Donnan-Effekt ist insbesondere für lebende Zellen aber auch für technische Systeme von Bedeutung.
Grundlagen
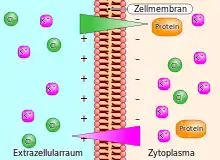
Voraussetzung für das Auftreten des Gibbs-Donnan-Effekts ist die Anwesenheit einer Ionensorte, die von der semipermeablen Membran nicht durchgelassen wird. Dies ist regelmäßig bei Makromolekülen wie löslichen Proteinen oder Nukleinsäuren in biologischen Zellen der Fall. Bei entsprechender Membranbeschaffenheit kann dies aber auch für eine Ionensorte eines niedermolekularen Salzes zutreffen. So ist bei gelöstem Natriumchlorid (Kochsalz) der Durchmesser des hydratisierten Cl−-Ions erheblich größer als der des kleineren Na+-Ions.[1] Zum Donnan-Effekt kommt es auch, wenn Ionen durch Verankerung an einer Grenzfläche nicht frei diffundieren können, wie dies bei Membranproteinen oder geladenen Polymermolekülen (siehe Ionentauscher) der Fall ist.
Ein osmotisches System ist im Gleichgewicht, wenn die chemischen Potentiale des Lösungsmittels und der anderen durchgelassenen Stoffe auf beiden Seiten der Membran jeweils gleich sind. Bei Anwesenheit von Ladungsträgern muss zusätzlich auf beiden Seiten im Volumen (abseits der Doppelschicht) jeweils die Summe der Äquivalentkonzentrationen ausgeglichen sein, denn das Innere eines Leiters ist (im Gleichgewicht) feldfrei und damit frei von Nettoladung. Ist nun auf einer Seite der Membran eine nicht permeierende Ionensorte stärker konzentriert, muss das durch permeierende Ionen kompensiert werden. Deren Konzentration ist daher im Gleichgewicht auf beiden Seiten unterschiedlich. Mit dieser Ungleichverteilung ist eine Potentialdifferenz im Bereich einiger Millivolt (mV) verbunden. Führt die Ungleichverteilung zu einer Differenz der Aktivität des Wassers, entsteht ein osmotischer Druck.
Donnan-Koeffizient
Der (Gibbs-)Donnan-Koeffizient rD, eine dimensionslose Zahl, gibt für die permeablen Ionen an, wie sich die Konzentrationsverhältnisse aufgrund der Potentialdifferenz verändern. Sind z. B. auf beiden Seiten der Membran (Indizes a, i für außen, innen) die permeablen, einwertigen Ionen K+ (Kalium) und Cl− (Chlorid) vorhanden sowie innen ein Makromolekül mit z Ladungen Pz+, so werden Cl− nach innen gezogen und K+ nach außen gedrängt:
wobei die Gleichheit gilt, weil die Potentialdifferenz gleichermaßen, aber in entgegengesetzter Richtung auf die beiden Ionen wirkt.
rD lässt sich unter Ausnutzung der Neutralitätsbedingungen
- und
auch als Funktion der Konzentration des geladenen Makromoleküls angeben:
wobei die Näherung für verdünnte Lösungen gilt.[2] Die permeablen Ionen sind also umso ungleicher verteilt, je höher Konzentration und Ladungszahl des Makromoleküls sind. Letztere ist oft über den Dissoziationsgrad vom pH-Wert abhängig.
Donnan-Potential
Das Donnan-Potential ist die Galvani-Potentialdifferenz zwischen zwei Lösungen, welche durch eine für Ionen permeable Membran getrennt sind[3].
Der Zusammenhang zwischen Membranpotential und Donnan-Koeffizient ergibt sich aus der Nernst-Gleichung:
ΔΦ ist die Differenz des elektrischen Potentials, R die universelle Gaskonstante, T die absolute Temperatur in K und F die Faraday-Konstante.
Die nachfolgende Tabelle mit Beispielen zeigt, dass die Anwesenheit eines nicht permeablen Ions zu großen Konzentrationsunterschieden bei den durchgelassenen Ionen führen kann. Gleichzeitig können beträchtliche Donnan-Potentiale auftreten,[2] zitiert nach:[4]
| z·[Pz+]i | [K+]a = [Cl−]a | [K+]i | [Cl−]i | rD | ΔΦ (mV) |
|---|---|---|---|---|---|
| 0,002 | 0,0010 | 0,00041 | 0,00241 | 2,44 | 22,90 |
| 0,0100 | 0,00905 | 0,01105 | 1,10 | 2,56 | |
| 0,1000 | 0,0990 | 0,1010 | 1,01 | 2,58 | |
| 0,02 | 0,0010 | 0,00005 | 0,02005 | 20,05 | 76,96 |
| 0,0100 | 0,00414 | 0,02414 | 2,41 | 22,65 | |
| 0,1000 | 0,0905 | 0,1105 | 1,10 | 2,56 | |
(alle Konzentrationsangaben in mol·l−1, Temperatur: 298 K). Die Höhe des Membranpotentials hängt vom Verhältnis des geladenen Makromoleküls zu den beweglichen Ionen ab. Sind solche Ionen in hoher Konzentration vorhanden, wirkt sich die Anwesenheit des unbeweglichen Ions nur geringfügig aus.
Osmotischer Druck
Im Gleichgewicht ergibt sich der osmotische Druck aus dem Verhältnis der Aktivitäten der Lösungsmittel auf beiden Seiten der Membran:
Dabei sind: das Molvolumen des Lösungsmittels, R die universelle Gaskonstante und T die absolute Temperatur in K.
Siehe auch
Literatur
- Walter J. Moore, Dieter O. Hummel: Physikalische Chemie. Walter de Gruyter, Berlin 1986, ISBN 3-11-010979-4.
Weblinks
- Vorlesungsskript Biophysik. (PDF; 302 kB) Uni Rostock
- Membranpotential. Universität Hamburg: Botanik online
Einzelnachweise
- Sehon Hannes. Physikalische Chemie. Verlag Herder Freiburg. i. Brsg. 1976, ISBN 3-451-16411-6
- Moore Walter J., Hummel Dieter O.: Physikalische Chemie, S. 650f. Walter de Gruyter, Berlin 1986, ISBN 3-11-010979-4.
- Allen J. Bard, György Inzelt, Fritz Scholz: Electrochemical Dictionary. Springer Science & Business Media, 2008, ISBN 978-3-540-74598-3, S. 167 (google.com).
- Charles Tanford: Physical Chemistry of Macromolecules. John Wiley, New York 1961.