Dantrolen
Dantrolen ist ein Hydantoin-Derivat aus der Gruppe der Muskelrelaxantien und wird als Arzneistoff, oral in Kapselform zur Behandlung spastischer Syndrome mit krankhaft gesteigerter Muskelspannung und intravenös bei der Malignen Hyperthermie und beim malignen neuroleptischen Syndrom eingesetzt. Hergestellt wird der Arzneistoff (als Dantrolen-Natrium) etwa von den Firmen Röhm-Pharma in Wien, Boehringer Mannheim in Rotkreuz[4] und Norgine in Wettenberg.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
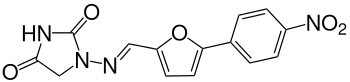 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Dantrolen | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C14H10N4O5 | |||||||||||||||||||||
| Kurzbeschreibung |
orangefarbenes Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
M03CA01 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 314,25 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
7,5[1] | |||||||||||||||||||||
| Löslichkeit |
wenig in Wasser (146 mg·l−1 bei 25 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Die klinische Einführung des von Snyder und seinen Mitarbeitern 1967 synthetisierten[5] und von Gaisford Harrison zur Therapie der Malignen Hyperthermie vorgeschlagenen Dantrolens erfolgte 1979.[6]
Klinische Angaben
Dantrolen hemmt die Freisetzung von Calcium-Ionen (Ca2+) aus dem sarkoplasmatischen Retikulum (ohne die Ca2+-Wiederaufnahme zu beeinflussen)[7] wahrscheinlich über eine Hemmung des Ryanodin-Rezeptors und kann so die unkontrolliert ablaufenden Kontraktionen der gesamten Skelettmuskulatur durchbrechen.[8] Die Maligne Hyperthermie ist eine seltene, aber lebensbedrohende Narkosekomplikation. Triggersubstanzen sind volatile Inhalationsanästhetika und depolarisierende Muskelrelaxantien wie Suxamethonium. Eine für die Erkrankung disponierende Ursache ist häufig eine Mutation des für einen Ryanodin-Rezeptor kodierenden RYR1-Gens. Ein ausreichender Vorrat an Dantrolen zur Notfalltherapie ist in operativen Kliniken und auch in anästhesiologischen Praxen, die Patienten ambulant in Allgemeinanästhesie versorgen, unerlässlich.
Eine weitere Einsatzmöglichkeit ist die Behandlung des malignen neuroleptischen Syndroms. Es gibt Hinweise, dass Dantrolen auch bei der Therapie der bei Intoxikationen mit MDMA (Ecstasy) nicht selten auftretenden Hyperthermie hilfreich sein könnte.[9]
Eine Injektionsflasche enthält 20 mg Dantrolen-Natrium sowie 3 g Mannitol als Trockensubstanz (Pulver). Zur Herstellung einer Infusionslösung wird der Inhalt einer Flasche mit 60 ml Wasser für Injektionszwecke aufgelöst (zur Vermeidung eines Mitaufziehens nicht gelöster Dantrolen-Kristalle – mit dem Risiko für Reaktionen an der Injektionsstelle von einer Rötung bis zur Gewebsnekrose – muss unter Umständen eine Filtrationsvorrichtung (Filternadel bzw. Filterkanüle) benutzt werden[10]). Der pH-Wert beträgt dann 9,5. Zur Behandlung einer Malignen Hyperthermie werden beim erwachsenen Menschen 2,5 bis 10 mg/kg und mehr, etwa 200 mg (10 Injektionsflaschen) bis 800 mg, benötigt.[11]
Unerwünschte Wirkungen
Da Dantrolen auch in Ruhe die intrazelluläre Calciumionenkonzentration senkt und somit gering muskelrelaxierend wirkt, kann nach der Anwendung eine überwachungsbedürftige Atemschwäche während der klinischen Wirkdauer von 5 bis 8 Stunden auftreten. Bei längerer Behandlungsdauer sollte das alkalische Dantrolen über einen zentralvenösen Katheter verabreicht werden, da bei versehentlicher Injektion ins Gewebe Nekrosen drohen. Weitere Nebenwirkungen können Übelkeit, Erbrechen, Kopfschmerzen, Schwindel, Durchfall und allergische Reaktionen sein.[12] Dantrolen wurde auch kausal mit Pleuraerguss in Verbindung gebracht.[13]
Handelsnamen
Monopräparate: Dantamacrin (D, CH), Dantrolen i. v. (D, CH)
Weblinks
- Beverley A. Britt: Dantrolene. In: Canadian Anaesthetists’ Society Journal. Band 31, Nr. 1, 1984, S. 61, doi:10.1007/BF03011484.
Einzelnachweise
- Eintrag zu Dantrolen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. November 2014.
- Eintrag zu Dantrolene in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Datenblatt Dantrolene sodium salt bei Sigma-Aldrich, abgerufen am 25. Mai 2011 (PDF).
- Bei maligner Hyperthermie. In: Anästhesie Intensivtherapie Notfallmedizin- Band 20, Nr. 2, 1985. S. XXV (Röhm Pharma GmbH Wetterstadt).
- H. R. Snyder Jr., C. S. Davis, R. K. Bickerton, R. P. Halliday: l-[(5-Arylfurfurylidine)]amino hydantoins. A new class of muscle relaxants. In: J Med Chem. Band 10, 1967, S. 807–810.
- Michael Heck, Michael Fresenius: Repetitorium Anaesthesiologie. Vorbereitung auf die anästhesiologische Facharztprüfung und das Europäische Diplom für Anästhesiologie. 3., vollständig überarbeitete Auflage. Springer, Berlin/Heidelberg/ New York u. a. 2001, ISBN 3-540-67331-8, S. 804.
- Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin, Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin: S1-Leitlinie: Therapie der malignen Hyperthermie. Erarbeitet von Werner Klingler, Norbert Roewer, Frank Schuster und Frank Wappler. In: Anästh Intensivmed. Band 59, 2018, S. 204–208, hier: S. 207.
- Krause et al.: Dantrolene – A review of its pharmacology, therapeutic use and new developments. Anaesthesia, 2004, Bd. 59, S. 364–373, PMID 15023108 (Übersichtsarbeit).
- Hall & Henry: Acute toxic effects of 'Ecstasy' (MDMA) and related compounds: overview of pathophysiology and clinical management. Br. J. Anaesth, 2006, Bd. 96, S. 678–685, PMID 16595612.
- ifap Service-Institut für Ärzte und Apotheker GmbH: Dantrolen-Kristalle vor Verabreichung ausfiltern.
- Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin, Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin: S1-Leitlinie: Therapie der malignen Hyperthermie. Erarbeitet von Werner Klingler, Norbert Roewer, Frank Schuster und Frank Wappler. In: Anästh Intensivmed. Band 59, 2018, S. 204–208, hier: S. 205.
- S1-Leitlinie: Therapie der malignen Hyperthermie. 2018, S. 207.
- Berthold Jany, Tobias Welte: Pleuraerguss des Erwachsenen – Ursachen, Diagnostik und Therapie. In: Deutsches Ärzteblatt. Band 116, Nr. 21, (Mai) 2019, S. 377–385, hier: S. 380.