Carvacrol
Das Carvacrol ist ein terpenoider Naturstoff, der unter verschiedenen Namen bekannt ist. Der systematische Name (IUPAC) des Carvacrol ist 2-Methyl-5-(1-methylethyl)-phenol. Die Verbindung stellt ein Strukturisomer (Konstitutionsisomer) zum Thymol dar.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
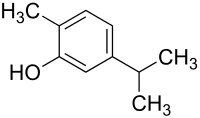 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Carvacrol | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C10H14O | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 150,22 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt |
~ 0 °C[4] | ||||||||||||||||||
| Siedepunkt |
237–238 °C[4] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex |
1,5230 (20 °C)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Vorkommen

Carvacrol kommt unter anderen in Thymian (Thymus), Winter-Bohnenkraut (Satureja montana), Sommer-Bohnenkraut (Satureja hortensis), Oregano (Origanum), Echter Katzenminze (Nepeta cataria) und Gänsefüßen (z. B. Chenopodium ambrosioides)[10] vor. Öle, die von diesen Pflanzenarten gewonnen werden, können bis zu 85 % Carvacrol enthalten. Zwei Pflanzen mit besonders hohem Carvacrol-Gehalt sind auch der Griechische Bergtee (Sideritis scardia) und Kretische Bergtee Malotira (Sideritis syriaca).
Eigenschaften und Aufbau
Das Carvacrol ist ein höheres Homolog des o-Kresols.[11] Gesetzliche Regelungen bezüglich des Carvacrols gehen im Allgemeinen von der Unbedenklichkeit des Thymols aus.[12]
Carvacrol gibt mit Eisen(III)-chlorid eine olivgrüne Färbung.[13]
Biologische Bedeutung
Carvacrol findet vielseitige Verwendung, hauptsächlich als Biozid. So zeigt es Wirkung als Antimykotikum, Insektizid, Antibiotikum und als Anthelminthikum.[14][15] Zudem inhibiert Carvacrol das Entzündungsreaktionen vermittelnde Enzym Cyclooxygenase-2 und entspricht in seiner Wirkung daher den entzündungshemmenden Arzneistoffen Celecoxib und Etoricoxib, die u. a. gegen Rheuma und Gicht eingesetzt werden.[16]
Einzelnachweise
- Eintrag zu CARVACROL in der CosIng-Datenbank der EU-Kommission, abgerufen am 21. März 2020.
- Eintrag zu Carvacrol. In: Römpp Online. Georg Thieme Verlag, abgerufen am 19. Juni 2014.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-316.
- The Merck Index Twelfth Edition. Merck Research Laboratories, 1996, ISBN 0-911910-12-3, Eintrag 1923.
- Datenblatt Carvacrol bei Sigma-Aldrich, abgerufen am 7. Juni 2017 (PDF).
- Eintrag zu Carvacrol in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- P. M. Jenner, E. C. Hagan, Jean M. Taylor, E. L. Cook, O. G. Fitzhugh: Food flavourings and compounds of related structure I. Acute oral toxicity. In: Food and Cosmetics Toxicology. Vol. 2, 1964, S. 327.
- G. S. B. Viana, F. F. Matos, W. L. Araujo, F. J. A. Matos, A. A. Craveiro: Essential Oil of Lippia grata: Pharmacological Effects and Main Constituents. In: Quarterly Journal of Crude Drug Research. Vol. 19, 1981, S. 1.
- Roger James, John B. Glen: Synthesis, biological evaluation, and preliminary structure-activity considerations of a series of alkylphenols as intravenous anesthetic agents. In: Journal of Medicinal Chemistry. Vol. 23, 1980, S. 1350.
- M. S. Owolabi, L. Lajide, M. O. Oladimeij, W. N. Setzer, M. C. Palazzo, R. A. Olowu, A. Ogundajo: Volatile constituents and antibacterial screening of the essential oil of Chenopodium ambrosioides L. growing in Nigeria. In: Nat. Prod. Commun. Band 4, Nr. 7, 2009, S. 989–992, PMID 19731609.
- H. Beyer, W. Walter: Lehrbuch der organischen Chemie. S. Hirzel Verlag, Stuttgart 1981, ISBN 3-7776-0356-2, S. 643.
- Thymol; Exemption from the Requirement of a Tolerance. In: Federal Register. 71 (11), 2006, S. 2889–2895.
- Harry Auterhoff, Joachim Knabe, Hans-Dieter Höltje: Lehrbuch der pharmazeutischen Chemie. Wissenschaftliche Verlagsgesellschaft, Stuttgart 1999, ISBN 3-8047-1645-8.
- S. Kordali, A. Cakir, H. Ozer, R. Cakmakci, M. Kesdek, E. Mete: Antifungal, phytotoxic and insecticidal properties of essential oil isolated from Turkish Origanum acutidens and its three components, carvacrol, thymol and p-cymene. In: J. Bior. Tech. Band 99, Nr. 18, 2008, S. 8788–8795, doi:10.1016/j.biortech.2008.04.048, PMID 18513954.
- M. M. Obaidat, J. F. Frank: Inactivation of Escherichia coli O157:H7 on the Intact and Damaged Portions of Lettuce and Spinach Leaves by Using Allyl Isothiocyanate, Carvacrol, and Cinnamaldehyde in Vapor Phase. In: J. Food Prot. Band 72, Nr. 10, 2009, S. 2046–2055, PMID 19833026.
- M. Hotta, R. Nakata, M. Katsukawa, K. Hori, S. Takahashi, H. J. Inoue: Carvacrol, a component of thyme oil, activates PPARalpha and gamma and suppresses COX-2 expression. In: Lipid Res. 51(1), Jan 2010, S. 132–139. PMID 19578162.

