CLAW-Hypothese
Nach der CLAW-Hypothese gibt es eine negative Rückkopplung (Gegenkopplung) im Klimasystem der Erde über eine schwefelhaltige Substanz, die von bestimmten Arten des Phytoplanktons abgegeben wird und in der Atmosphäre Aerosole bildet, die wiederum Schatten spendende Wolken fördern. Letzteres ist, bezogen auf die nötigen Mengen an Schwefel, sehr effizient. Das ist allgemein akzeptierte Lehrmeinung. Unklar ist, ob die so verminderte Einstrahlung und Temperatur die Emission der Substanz fördert oder hemmt. Im Falle einer Hemmung würde sich ein Thermostat ergeben, der die Temperatur stabilisiert, gegenüber der langsamen Zunahme der Leuchtkraft der Sonne und Schwankungen im Kohlenstoffzyklus, siehe Paradoxon der schwachen jungen Sonne und Paläoklimatologie. Allgemein abgelehnt wird die Gaia-Hypothese, zu der die CLAW-Hypothese einen Baustein beitragen soll.
Die Hypothese wurde von Glenn Shaw (1983) geäußert und von Robert Charlson, James Lovelock, Meinrat O. Andreae und Stephen Warren ausgearbeitet („CLAW“ sind deren Initialen, Charlson/Lovelock/Andreae/Warren-Hypothese).[1]
Details der Wirkkette
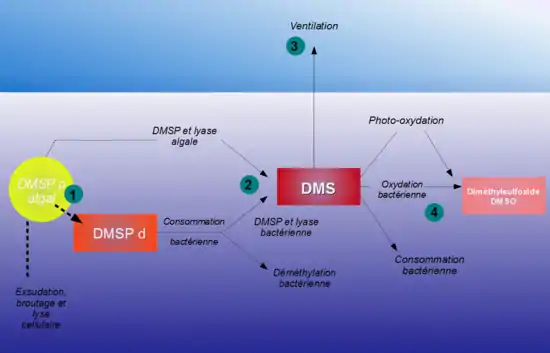
Zu den Emittenten zählen z. B. Coccolithophoren, die Dimethylsulfoniumpropionat (DMSP) zur Erhöhung ihres osmotischen Druckes produzieren. Wenn sie absterben oder gefressen werden, wird DMSP in Methanthiol und Dimethylsulfid (CH3SCH3; DMS) frei. Während Methanthiol schnell bakteriell umgesetzt wird (teilweise zu schwefelhaltigen Aminosäuren) gelangt DMS in die Atmosphäre. Dort wird es photochemisch abgebaut.
Das erste stabile Zwischenprodukt ist Dimethylsulfoxid (CH3S(=O)CH3) :
Die weiteren Wege sind vielfältig, zum Teil heterogen, aber das wesentliche Endprodukt ist Schwefelsäure (H2SO4). Diese und auch das leidlich stabile Zwischenprodukt Methansulfonsäure (CH3SO3H) haben einen sehr geringen Sättigungsdampfdruck, sodass sich die Moleküle zu zahlreichen Kondensationskeimen zusammenlagern. Das bewirkt, dass sich Wolken bei geringerer Übersättigung bilden bzw. bei größerer Feuchte aus zahlreicheren, kleineren Tropfen bestehen, die weniger schnell abregnen. Durch die hygroskopische Wirkung von Sulfataerosolen entsteht unterhalb 100 % r.F. ausgedehnter Dunst, der wie Wolken die Einstrahlung vermindert, siehe Strahlungsbilanz der Erde. Nur in Reinluftgebieten kann dieser Mechanismus bedeutend sein, da es sonst genug andere Kondensationskeime gibt. In höheren, stürmischeren Breiten dominieren aus Gischt gebildete Salzpartikel den Dunst.
Zur Rückwirkung auf die DMS-Emission tragen verschiedene Effekte bei. Eine höhere Einstrahlung und Temperatur führt in mittleren Breiten zu Vermehrung des Planktons, in höheren Breiten gar zu einer längeren Wachstumssaison. In niedrigen Breiten dagegen ist die Primärproduktion oft limitiert durch das Nährstoffangebot, das bei steigender Oberflächentemperatur knapper wird, denn dann ist die Schichtung der oberen 100 bis 200 Meter Wassersäule stabiler, was den Aufstieg nährstoffreichen Tiefenwassers vermindert. Das Plankton reagiert unter Nahrungsstress mit höherer Ausschüttung von DMS, die Population könnte sich zu DMSP-produzierenden Arten verschieben oder aber stark abnehmen. Nicht zuletzt wird DMS mit steigender Wassertemperatur rascher ausgasen.
Literatur
- Glenn E. Shaw (1983): Bio-controlled thermostasis involving the sulphur cycle. Climate Change 5, S. 297–303, doi:10.1007/BF02423524.
- R. Charlson, J. Lovelock, M. Andreae and S. Warren (1987): Oceanic phytoplankton, atmospheric sulphur, cloud albedo and climate. Nature 326, S. 655–661.
- D. Harvey: Climat and global environmental change. Understanding Global Environmental change. Prentice Hall, 2000, ISBN 9780582322615, S. 28ff.
- S. Rahmstorf und K. Richardson: Wie bedroht sind die Ozeane? Biologische und physikalische Aspekte. Fischer, 2007, ISBN 9783104000695, S. 100ff.
- Albert J. Gabric et al.: Global simulations of the impact on contemporary climate of a perturbation to the sea-to-air flux of dimethylsulfide. Australian Meteorological and Oceanographic Journal 63, 2013, S. 365–376, (online).
- M Galí, R Simó: A meta‐analysis of oceanic DMS and DMSP cycling processes: Disentangling the summer paradox. Global Biogeochemical Cycles, 2015, doi:10.1002/2014GB004940 (Zusatzinfo frei).
Weblinks
- Seite über die CLAW-Hypothese
- Johann Feichter: Aerosole und das Klimasystem, aus: Physik in unserer Zeit 2003 (PDF; 447 kB)
- CLAW hypothesis von Charlson et al. (1986; Nature 326, 655-661).
- Ein Schema der anti-CLAW hypothesis vorgestellt von James Lovelock (2006, The Revenge of Gaia) in Antwort auf Charlson et al. (1986; Nature 326, 655-661).
Einzelnachweise
- Robert J. Charlson, James E. Lovelock, Meinrat O. Andreae, Stephen G. Warren: Oceanic phytoplankton, atmospheric sulphur, cloud albedo and climate. In: Nature. 326, 1987, S. 655–661, doi:10.1038/326655a0.