Bisphenol F
Bisphenol F (kurz BPF) ist eine aromatische organische Verbindung aus der Gruppe der Diphenylmethan-Derivate und eines der Bisphenole. In BPF sind die beiden aromatischen Ringe durch eine Methylengruppe (CH2) verbunden.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
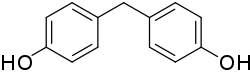 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bisphenol F | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C13H12O2 | ||||||||||||||||||
| Kurzbeschreibung |
rötlich-kristalliner Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 200,20 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Verwendung
BPF wird zur Herstellung von Epoxidharzen und -beschichtungen verwendet, die in der Industrie eingesetzt werden, um die Dicke und Haltbarkeit von Materialien zu erhöhen, wie in:[2][2][3]
- Tank- und Rohrauskleidungen
- Industrieböden
- Straßenbelägen
- Strukturklebstoffen
- Fugenmassen.
BPF-Epoxidharze werden auch für verschiedene Verbraucherprodukte eingesetzt:[2]
- Beschichtungen
- Lacke
- Lebensmittelverpackungen, beispielsweise Beschichtungen von Getränke- und Konservendosen
Im zahnmedizinischen Bereich werden BPF-Epoxidharze in oder für Dentalmaterialien verwendet: als Restaurationsmaterial, für Auskleidungen, als Klebstoff, zur Herstellung von Prothesen und Gewebeersatzstoffen.[2]
Verstoffwechselung und Toxizität
Studien haben gezeigt, dass BPF primär in Phase-II-Biotransformationsreaktionen glucoronidiert und sulfatiert wird,[3][4][5] wobei die Art der Verstoffwechselung jeweils vom Zelltyp abhängig ist. In Zellmodellen entstanden in einer humanen Hepatomzelllinie (HepG2) hauptsächlich die entsprechenden Sulfate, wohingegen in Hepatozyten sowohl Sulfate als auch Glucuronide gebildet wurden.[5] Darüber hinaus entstehen in Phase-I-Biotransformationsreaktionen verschiedene hydroxylierte BPF-Metaboliten, darunter hauptsächlich meta-hydroxyliertes BPF, ortho-hydroxyliertes BPF und 2,4-Dihydroxybenzophenon (DHB).[4][6] Diese Stoffwechselwege sind P450-abhängig.[4]
In einer an Ratten durchgeführten Studie wurden BPF und seinen Metaboliten innerhalb von 96 Stunden zu 43–54 % der Dosis über den Urin und 15–20 % über den Kot ausgeschieden; der Rest der verabreichten Dosis verblieb in verschiedenen Organen der Ratte und wurde hauptsächlich im Lumen des Verdauungstrakts und in der Leber wiedergefunden. Bei trächtigen Ratten wurde BPF auch in Gebärmutter, Plazenta, Fruchtwasser und Feten gefunden, was darauf hinweist, dass BPF die Plazentaschranke zu passieren vermag.[3] Eine weitere Ratten-Studie zeigte als hauptsächlichen Effekt eine Lebertoxizität.[7]
Eine Übersichtsarbeit zur hormonellen Aktivität der Bisphenole A, S und F fand in vier von fünf in-vivo-Studien Berichte über estrogene, androgene und thyroidogene Wirkungen für BPF.[2] In-vitro-Studien zu BPF zeigten Effekte wie Zytotoxizität, zelluläre Dysfunktion, DNA-Schädigung und Chromosomenaberration.[2]
Vorkommen und Freisetzung
BPF konnte in der Umwelt und in Lebensmittelkontaktmaterialien nachgewiesen werden.[8]
BPF kommt in Senf vor, es entsteht dort als Abbauprodukt des natürlich vorkommenden Glucosinalbin.[9] Das Bundesamt für Risikobewertung schätzt mögliche gesundheitliche Beeinträchtigungen durch die daraus resultierende Exposition als unwahrscheinlich ein.[8] Weiterhin kommt BPF in den Knollen bestimmter Orchideenarten vor.[10]
Weblinks
- Bisphenol F – Informationen des Bundesamts für Lebensmittelsicherheit und Veterinärwesen
Einzelnachweise
- Datenblatt Bis(4-hydroxyphenyl)methane bei Sigma-Aldrich, abgerufen am 11. April 2020 (PDF).
- Johanna Ruth Rochester, Ashley Louise Bolden: Bisphenol S and F: A Systematic Review and Comparison of the Hormonal Activity of Bisphenol A Substitutes. In: Environmental Health Perspectives. 123, Nr. 7, 2015, S. 643–50. doi:10.1289/ehp.1408989. PMID 25775505. PMC 4492270 (freier Volltext).
- Nicolas Cabaton, Marie-Christine Chagnon, Jean-Claude Lhuguenot, Jean-Pierre Cravedi, Daniel Zalko: Disposition and metabolic profiling of bisphenol F in pregnant and nonpregnant rats. In: Journal of Agricultural and Food Chemistry. 54, Nr. 26, 27. Dezember 2006, S. 10307–10314. doi:10.1021/jf062250q. PMID 17177575.
- Nicolas Cabaton, Daniel Zalko, Estelle Rathahao, Cécile Canlet, Georges Delous, Marie-Christine Chagnon, Jean-Pierre Cravedi, Elisabeth Perdu: Biotransformation of bisphenol F by human and rat liver subcellular fractions. In: Toxicology in Vitro. 22, Nr. 7, 1. Oktober 2008, S. 1697–1704. doi:10.1016/j.tiv.2008.07.004. PMID 18672047.
- Coralie Dumont, Elisabeth Perdu, Georges de Sousa, Laurent Debrauwer, Roger Rahmani, Jean-Pierre Cravedi, Marie-Christine Chagnon: Bis(hydroxyphenyl)methane—bisphenol F—metabolism by the HepG2 human hepatoma cell line and cryopreserved human hepatocytes. In: Drug and Chemical Toxicology. 34, Nr. 4, 1. Oktober 2011, S. 445–453. doi:10.3109/01480545.2011.585651. PMID 21770713.
- Marc Audebert, L. Dolo, E. Perdu, J.-P. Cravedi, D. Zalko: Use of the γH2AX assay for assessing the genotoxicity of bisphenol A and bisphenol F in human cell lines. In: Archives of Toxicology. 85, Nr. 11, 9. Juni 2011, S. 1463–1473. doi:10.1007/s00204-011-0721-2. PMID 21656223.
- Nobuhiko Higashihara, Keiji Shiraishi, Katusi Miyata, Yutaka Oshima, Yasushi Minobe, Kanji Yamasaki: Subacute oral toxicity study of bisphenol F based on the draft protocol for the "Enhanced OECD Test Guideline no. 407". In: Archives of Toxicology. 81, Nr. 12, 1. Dezember 2007, S. 825–832. doi:10.1007/s00204-007-0223-4. PMID 17628788.
- Bisphenol F in Senf: das Auftreten von unerwünschten Wirkungen auf die Gesundheit durch gemessene BPF-Gehalte ist unwahrscheinlich. In: Bundesamt für Risikobewertung. Abgerufen am 7. Februar 2021.
- O. Zoller, B. J. Brüschweiler, R. Magnin, H. Reinhard, P. Rhyn, H. Rupp, S. Zeltner, R. Felleisen: Natural occurrence of bisphenol F in mustard. In: Food Additives & Contaminants: Part A. 33, Nr. 1, 23. November 2015, S. 137–146. doi:10.1080/19440049.2015.1110623. PMID 26555822.
- Dr. Nina Zänglein: Bisphenole. In: Bayerisches Landesamt für Gesundheit und Lebensmittelsicherheit. Abgerufen am 7. Februar 2020.
