Benary-Reaktion
Die Bénary-Reaktion ist eine Namensreaktion der Organischen Chemie, die erstmals 1909[1] von Erich Bénary (1881–1941) beschrieben wurde. Dabei werden Ketone von Enaminen mit Grignard-Verbindungen umgesetzt. Es entstehen α,β-ungesättigte Ketone, Aldehyde oder Ester.
Übersichtsreaktion
Ein Enaminoketon reagiert mit einer Grignard-Verbindung zu einem α,β-ungesättigten Keton:[2][3]

Der blaue Rest R ist dabei ein organischer Alkylrest, zum Beispiel ein Ethylrest.
Reaktionsmechanismus
Zerong Wang schlägt zwei Mechanismen vor. Im Folgenden werden beide dargestellt, wobei der 1,4-Additions-Eliminierungs-Mechanismus für wahrscheinlicher gehalten wird.
1,4-Additions-Eliminierungs-Mechanismus
Im ersten Schritt wird der blaue Alkylrest der Grignard-Verbindung an das positiv polarisierte Kohlenstoffatom des Enaminoketons 1 addiert, wodurch das Magnesium-Enolat 2 entsteht.
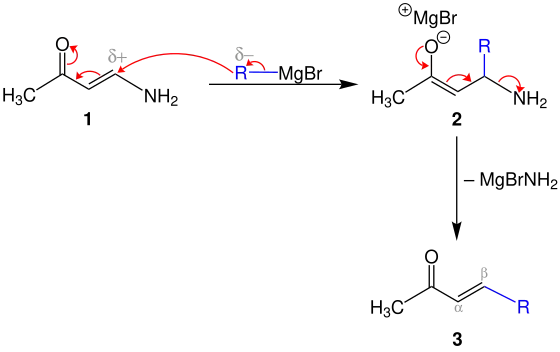
Durch die Eliminierung von MgBrNH2 entsteht das α,β-ungesättigte Keton 3.
1,2-Additions-Mechanismus
In diesem Fall wird der Alkylrest der Grignard-Verbindung an das positiv polarisierte Carbonylkohlenstoffatom von 1 addiert. Das entstehende Magnesium-Enolat 4 wird anschließend mit Wasser behandelt. Die Protonierung der Hydroxygruppe des entstandenen Aminoenolats 5 ergibt die Bildung des Kations 6.
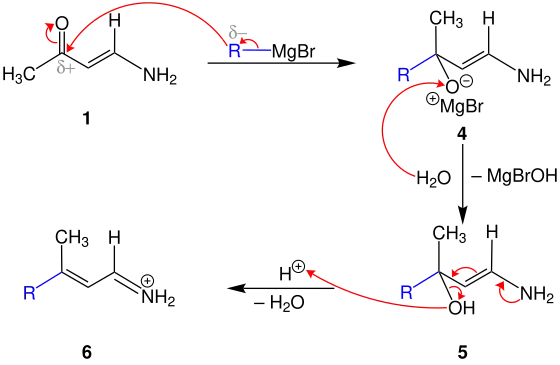
Auch 6 wird durch Wasser protoniert, wodurch das Oxoniumion 7 entsteht.

Durch anschließende 1,3-Wasserstoffverschiebung entsteht das Kation 8. Zuletzt wird ein Ammoniumkation eliminiert. Dadurch entsteht ein α,β-ungesättigter Aldehyd 9.[4]
Literatur
- Z. Wang: Comprehensive Organic Name Reactions and Reagents, Vol 1. John Wiley & Sons, Hoboken, New Jersey 2009, S. 311–314, ISBN 978-0-471-70450-8.
Einzelnachweise
- Erich Bénary: Über die Acylierung des β‐Amino‐crotonsäureesters und verwandter Verbindungen, Berichte der deutschen chemischen Gesellschaft 1909, 42(3), 3912–3925, doi:10.1002/cber.190904203147.
- Erich Bénary: Über eine Bildungsweise ungesättigter Ketone aus substituierten Amino-methylenketonen, Berichte der deutschen chemischen Gesellschaft 1931, 64(9), 2543–2545, doi:10.1002/cber.19270600539.
- Erich Bénary: Über die Einwirkung von Ammoniak und Aminen auf einige aliphatische und aromatische Oxymethylen‐ketone, Berichte der deutschen chemischen Gesellschaft 1930, 63(6), 1573–1577, doi:10.1002/cber.19300630641.
- Ferdinand Näf, René Decorzant: A Stereospecific Synthesis of (E, Z)-α, β-γ, δ-Diunsaturated Aldehydes, Ketones, and Esters Using the Benary Reaction, Helvetica Chimica Acta 1974, 57(5), 1309–1317, doi:10.1002/hlca.19740570507.