Bariummanganat
Bariummanganat, BaMnO4, ist das Bariumsalz aus der Gruppe der Manganate. Im Gegensatz zu Bariumpermanganat besitzt das Mangan in Bariummanganat die Oxidationsstufe +VI.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
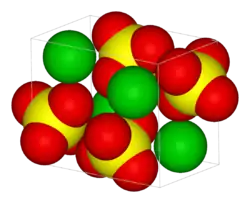 | |||||||||||||||||||
| _ Ba2+ _ Mn6+ _ O2− | |||||||||||||||||||
| Kristallsystem | |||||||||||||||||||
| Raumgruppe |
I41/a (Nr. 88) | ||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bariummanganat | ||||||||||||||||||
| Andere Namen |
Bariummanganat(VI) | ||||||||||||||||||
| Verhältnisformel | BaMnO4 | ||||||||||||||||||
| Kurzbeschreibung |
dunkelgraues Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 256,26 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
4,85 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Löslichkeit |
Unlöslich in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Bariummanganat kann durch die Reaktion der beiden Salze Kaliummanganat und Bariumchlorid gewonnen werden.
Das Erhitzen von Mangan(IV)-oxid mit Bariumcarbonat oder Bariumnitrat lässt auch das Salz entstehen.[3]
Eigenschaften
Physikalische Eigenschaften
Das Salz besitzt bei Normalbedingungen eine Scheelit-ähnliche Struktur. Es kristallisiert in einem tetragonalem Kristallsystem mit der Raumgruppe I41/a (Raumgruppen-Nr. 88). Analog zu Bariumwolframat transformiert es bei einem Druck von 5,8 GPa zu einer monoklinen Fergusonit-Struktur der Raumgruppe I2/a (Raumgruppen-Nr. 15, Stellung 7).[2]
Chemische Eigenschaften
Die Herstellung der Permangansäure ist mit Bariummanganat und Schwefelsäure möglich.
Verwendung
Bariummanganat wurde in der organischen Chemie zur Oxidation von primären Alkoholen zu Aldehyden und Carbonsäuren verwendet.[2]
Einzelnachweise
- Datenblatt Barium manganate bei Sigma-Aldrich, abgerufen am 26. Juli 2019 (PDF).
- Richard C. Ropp: Encyclopedia of the Alkaline Earth Compounds. Newnes, 2012, ISBN 0-444-59553-8, S. 895.
- Nicholas Eastaugh, Valentine Walsh, Tracey Chaplin, Ruth Siddall: Pigment Compendium. Routledge, 2008, ISBN 1-136-37392-6, S. 43–44.

