Azelastin
Azelastin ist ein Arzneistoff. Es ist ein selektives Antihistaminikum vom Typ der H1-Blocker der zweiten Generation. Es wird bei leichter, mittelschwerer und schwerer saisonaler und bei leichter ganzjähriger allergischer Rhinitis (z. B. Heuschnupfen) eingesetzt.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
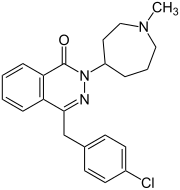 | ||||||||||||||||||||||
| Strukturformel ohne Stereochemie | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Azelastin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Kurzbeschreibung | ||||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Azelastin gibt es als Nasenspray (0,1-prozentige und in USA auch als 0,15-prozentige Lösung) und als Augentropfen (0,05-prozentige Lösung). In einigen Ländern sind das Nasenspray und die Augentropfen auch rezeptfrei in den Apotheken erhältlich.
Azelastin ist chiral. Azelastin wird meist als racemisches [1:1-Gemisch der (R)-Form und der (S)-Form] Hydrochlorid eingesetzt.[1]
Das Hydrochlorid ist eine farblose, nahezu geruchsneutrale Substanz mit einem bitteren Geschmack.
Pharmakokinetik und Metabolismus
Die systemische Bioverfügbarkeit von Azelastin beträgt bei Verabreichung in die Nase etwa 40 %. Maximale Konzentrationen im Blutplasma werden innerhalb von 2 bis 3 Stunden beobachtet. Die Eliminationshalbwertszeit liegt bei 22 h, die konstante Verteilungskonzentration beträgt 14,5 l/kg und die Rate der Entfernung aus dem Blutplasma (Plasmaclearance) ist 0,5 l/h/kg (basierend auf Daten bei intravenöser und oraler Verabreichung). Azelastin wird von der Cytochrom P450 Familie oxidativ in Desmethylazelastin als aktiven Metaboliten und in zwei inaktive Carbonsäuremetaboliten verstoffwechselt. Etwa 75 % einer oralen Dosis werden mit dem Kot ausgeschieden. Die pharmakokinetischen Eigenschaften von oral verabreichtem Azelastin werden durch Alter und Geschlecht nicht beeinflusst[5] und beeinträchtigen die Leberfunktion nicht.
Wirkung
Azelastin wirkt in dreifacher Weise:[5]
Die Wirkung von Azelastin setzt schnell ein: 15 Minuten nach Anwendung des Nasensprays[6] und 3 Minuten nach Einträufeln der Augentropfen.[7] Die Wirkung hält bis zu 12 Stunden an.[8]
Anwendungsgebiete
Als Nasenspray wird Azelastin bei Erwachsenen und Kindern ab 6 Jahren zur lokalen Behandlung von Symptomen der saisonalen allergischen Rhinitis (Heuschnupfen) und perennialen allergischen Rhinitis (ganzjähriger allergischer Schnupfen) eingesetzt, zu denen eine laufende Nase (Rhinorrhoe), häufiges Niesen und Nasenjucken zählen.[9] In einigen Ländern wird Azelastin auch zur Behandlung von nicht-allergischem Schnupfen (vasomotorische Rhinitis) bei Erwachsenen und Kindern ab 12 Jahren eingesetzt.[9] Azelastin Augentropfen werden zur lokalen Behandlung von saisonaler und ganzjähriger allergischer Bindehautentzündung (Konjunktivitis) verwendet.[10]
Im Gegensatz zu Cromoglicinsäure, die nur vorbeugend antiallergisch wirkt und kaum vom Körper aufgenommen wird,[11] kann Azelastin auch akut eingesetzt werden und wirkt teilweise systemisch.
Sicherheit und Verträglichkeit
Azelastin Nasenspray ist sicher in der Anwendung und wird von Erwachsenen und Kindern ab 6 Jahren, die unter allergischer Rhinitis leiden, gut vertragen.[12][13] Die am häufigsten genannten unerwünschten Wirkungen sind bitterer Geschmack, Kopfschmerzen, Nasenbrennen und Somnolenz (Müdigkeit und Benommenheit). In den Verschreibungsempfehlungen in den USA wird vor einem gleichzeitigen Konsum von Alkohol und/oder anderen Medikamenten gewarnt, die dämpfend auf das zentrale Nervensystem wirken. In einer Studie[14] wurde ein ähnlich geringer Grad von Somnolenz wie bei der Placebogruppe (ca. 2 %) beobachtet, während für frühere Studien höhere Werte angegeben werden.[15] Das Problem mit dem bitteren Geschmack wird in manchen Präparaten durch Zusatz von Süßstoff gemildert.
Handelsnamen
Als Nasenspray ist Azelastin in mehr als 60 Ländern zugelassen und wird als Monopräparat unter verschiedenen Markennamen vertrieben: Allergodil (DE), Astelin (USA), Astepro (USA), Pollival (DE, BE, LU), Rhinolast (GB), Vividrin Akut (DE), Afluon (ES). Als Kombinationspräparat mit Fluticason: Dymista (DE, USA, LT).
Die Augentropfen werden in mehr als 30 Ländern vertrieben: Allergodil (DE, A), Optilast (Großbritannien), Optivar (USA), Pollival (DE, BE, IT, NL, LU, RS), Afluon (ES), Vividrin Akut (DE).
Literatur
- Jan L. Brożek, Jean Bousquet u. a.: Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines—2016 revision. In: Journal of Allergy and Clinical Immunology. 140, 2017, S. 950–958, PMID 28602936. doi:10.1016/j.jaci.2017.03.050.
Einzelnachweise
- The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals, 14. Auflage (Merck & Co., Inc.), Whitehouse Station, NJ, USA, 2006; S. 153, ISBN 978-0-911910-00-1.
- Eintrag zu Azelastin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. November 2014.
- Datenblatt Azelastine hydrochloride bei Sigma-Aldrich, abgerufen am 21. März 2011 (PDF).
- Eintrag zu Azelastine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 17. August 2021.
- F Horak, UP. Zieglmayer: Azelastine nasal spray for the treatment of allergic and non-allergic rhinitis. In: Expert Rev Clin Immunol, 2009, 5, S. 659–669.
- Horak F et al.: Azelastine nasal spray and desloratadine tablets in pollen-induced seasonal allergic rhinitis: a pharmacodynamic study of onset of action and efficacy. In: Curr Med Res Opin, 2006, 22, S. 151–157.
- Friedlaender MH et al.: Evaluation of the onset and duration of effect of azelastine eye drops (0.05%) versus placebo in patients with allergic conjunctivitis using an allergen challenge model. In: Opthalmology, 2000, 107, S. 2152–2157.
- Greiff F et al.: Topical azelastine has a 12-hour duration of action as assessed by histamine challenge-induced exudation of alpha 2-macroglobulin into human nasal airways. In: Clin Exp Allergy, 1997, 27, S. 438–444.
- Rhinolast® nasal spray Summary of Product Characteristics, Astelin® FDA prescribing information.
- Optilast® eye drops Summary of Product Characteristics, Optivar® eye drops FDA prescribing information.
- onmeda.de Chromoglicinsäure-Beschreibung, abgerufen am 6. Juni 2018.
- Ratner PH et al.: A double –blind, controlled trial to assess the safety and efficacy of azelastine nasal spray in seasonal allergic rhinitis. In: J Allergy Clin Immunol, 1994, 94, S. 818–825.
- LaForce C et al.: Safety and efficacy of azelastine nasal spray (astelin NS) for seasonal allergic rhinitis. In: Ann Allergy Asthma Immunol, 1996, 76, S. 181–188.
- Berger W et al.: Impact of azelastine nasal spray on symptoms and quality of life compared with cetirizine oral tablets in patients with seasonal allergic rhinitis. In: Ann Allergy Asthma Immunol, 2006, 97, S. 375–381.
- Friedrich Horak: Effectiveness of twice daily azelastine nasal spray in patients with seasonal allergic rhinitis. In: Therapeutics and Clinical Risk Management Jg. 5 (2008) Heft 4 (Oktober), S. 1009–1022, PMC 2621402 (freier Volltext).
-Azelastine_Enantiomers_Structural_Formulae_V.1.svg.png.webp)