Pseudomonas fluorescens
Pseudomonas fluorescens ist ein gramnegatives, oxidasepositives, stäbchenförmiges Bakterium der Gattung Pseudomonas mit polständigem Geißelbüschel. P. fluorescens sondert, wie auch andere Pseudomonaden, Siderophore namens Pyoverdine (= bakterielles Fluorescein) ab, die unter UV-Licht fluoreszieren. Das Bakterium ist aerob und kommt im Boden, im Wasser und auf Pflanzen vor.
P. fluorescens gehört zu den selten isolierten, humanmedizinisch bedeutsamen Pseudomonasarten.[1][2]
Größere Bedeutung als in der Medizin hat P. fluorescens jedoch in der Bodenbiologie und beim Verderb von Nahrungsmitteln.
| Pseudomonas fluorescens | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
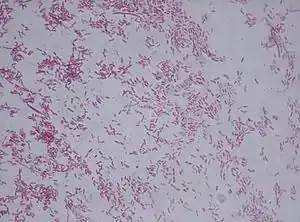
Pseudomonas fluorescens in Gram-Färbung | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Pseudomonas fluorescens | ||||||||||||
| Migula 1895 |
Bodenbiologie
Manche Stämme von P. fluorescens sind wichtige Bodenorganismen, da sie in der Lage sind, eine Reihe von pflanzenpathogenen Keimen zu unterdrücken. Auf diese Weise können natürliche suppressive Böden entstehen. Dieser Effekt ist darauf zurückzuführen, dass diese Stämme von P. fluorescens als Sekundärmetaboliten Antibiotika produzieren, sodass es durch die Besiedelung der Wurzeln durch solche Stämme zu einer induzierten systemischen Resistenz der Pflanze kommt bzw. sodass solche Stämme oft sehr spezifische Antagonisten bestimmter Pathogene sind.[3]
Antibiotika
Das Genom des Stammes Pf-5 wurde vollständig sequenziert. Dabei wurden 4 bereits bekannte Genkomplexe gefunden, die für Pilze oder Eipilze giftige Sekundärmetaboliten kodieren. Hierbei handelte es sich um Pyoluteorin, 2,4-Diacetylphloroglucinol, Pyrrolnitrin und Cyanwasserstoff. Außerdem wurden drei bislang unbekannte Genkomplexe entdeckt, die möglicherweise ebenfalls Sekundärmetaboliten kodieren. Es wurden auch Genkomplexe zur nicht-ribosomalen Erstellung und zur Aufnahme der Pyoverdin-Siderophore gefunden (Position und Orientierung weichen allerdings von denen bereits bekannter Genkomplexe in anderen Mikroorganismen ab).
Da Pyoverdine sehr stark wirksame Siderophore sind, kann es in pH-neutralen bis basischen Böden (Fe3+-Ionen sind schlecht löslich) zu einer Hemmung von phytopathogenen Bakterien kommen, weil diese zu wenig Fe3+-Ionen aufnehmen können. Hier verschwimmen allerdings die Grenzen, denn die Antibiotika sind Sekundärmetaboliten, während das Eisen im primären Stoffwechsel benötigt wird. Dennoch wirkt hier der Primärstoffwechsel hemmend auf das Wachstum phytopathogener Keime ein.
Ähnlich dürfte es sich mit Pyochelin verhalten. Die Genkomplexe zu seiner Erzeugung wurden ebenfalls im Stamm Pf-5 nachgewiesen. Pyochelin ist ein starker Cu2+- und Zn2+-Chelator und könnte so durch Entzug dieser Ionen hemmend auf das Pilzwachstum einwirken.[3][4]
Induzierte systemische Resistenz
Es ist nicht genau bekannt, wie Bakterien an den Wurzeln mit einer Pflanze interagieren, sodass es zu einer induzierten systemischen Resistenz kommt. Die Produktion des Sekundärmetaboliten 2,4-Diacetylphloroglucinol scheint dabei jedoch eine wichtige Rolle zu spielen.[5] Zudem kann P. fluorescens die pflanzliche Resistenz durch die Produktion des Pflanzenhormons Cytokinin steigern.[6]
Verderb von Nahrungsmitteln
P. fluorescens kann proteolytische und lipolytische Enzyme ausscheiden und lebt aerob und psychrotroph. Deshalb ist P. fluorescens zusammen mit Pseudomonas fragi und Pseudomonas putida einer der häufigsten gramnegativen, psychrotoleranten Keime, die am Verderb von Milch beteiligt sind.[7] Die abgesonderten Enzyme sind hitzestabil und bleiben auch nach dem Pasteurisieren und Ultrahocherhitzen noch aktiv.[8]
Ein anderes Problem bei der Verarbeitung von Milch ist die Besiedelung durch P. fluorescens nach der Pasteurisierung. Als Quelle solcher Besiedelungen kommt die Verarbeitungsumgebung in Frage.[9]
Medizinische Bedeutung
P. fluorescens wird häufig in Blutprodukten gefunden. Das hängt mit der Fähigkeit des Bakteriums zusammen, auch bei 4 °C weiter zu wachsen (Psychrophilie). Somit ist dieser Keim einer der zwei häufigsten Verursacher einer Sepsis nach einer Transfusion mit keimverseuchtem Blut.[10][11]
Einzelnachweise
- Michael T. Madigan, John M. Martinko: Brock Mikrobiologie. Aus dem Englischen von Dr. Thomas Lazar und Freya Thomm-Reitz. 11. aktualisierte Auflage. Pearson Studium, München 2009, ISBN 978-3-8273-7358-8, S. 373–391
- Ina Tammer, Alexandra Clarici, Frank Thies, Brigitte König, Wolfgang König: Nonfermenter: Pseudomonas spp. und verwandte Spezies. In: Birgid Neumeister (Hrsg.), Heinrich K. Geiss (Hrsg.), Rüdiger W. Braun (Hrsg.), Peter Kimmig (Hrsg.), u. a.: Mikrobiologische Diagnostik. Bakteriologie - Mykologie - Virologie - Parasitologie. 2. vollständig überarbeitete Auflage. Georg Thieme Verlag, Stuttgart 2009, ISBN 978-3-13-743602-7, S. 476–481
- Dieter Haas, Geneviève Défago: Biological control of soil-born pathogens by fluorescent pseudomonads. In: Nature Reviews Microbiology. Advance Online Publication, 10. März 2005 doi:10.1038/nrmicro1129, S. 1–13
- Ian T. Paulsen, Caroline M Press, u. a.: Complete genome sequence of the plant comensal Pseudomonas fluorescens Pf-5. In: Nature Biotechnology. Jg. 23, Nr. 7, 2006 doi:10.1038/nbt1110, S. 873–878
- Annalisa Iavicoli, Emmanuel Boutet, Antony Buchala, and Jean-Pierre Métraux: Induced Systemic Resistance in Arabidopsis thaliana in Response to Root Inoculation with Pseudomonas fluorescens CHA0. In: Molecular Plant-Microbe Interactions. Jg. 16, Nr. 7, 2003, S. 851–858
- Großkinsky DK, Tafner R, Moreno MV, Stenglein SA, García de Salamone IE, Nelson LM, Novák O, Strnad M, van der Graaff E, Roitsch T: Cytokinin production by Pseudomonas fluorescens G20-18 determines biocontrol activity against Pseudomonas syringae in Arabidopsis. In: Scientific Reports. 6, März 2016. doi:10.1038/srep23310. PMID 26984671. PMC 4794740 (freier Volltext).
- Martin Wiedmann, Denise Weilmeier, Sean S. Dineen, Robert Ralyea, Kathryn J. Boor: Molecular and Phenotypic Characterization of Pseudomonas spp. isolated from Milk. In: Applied and Environmental Microbiology. Jg. 66 Nr. 5, 2000 doi:10.1128/AEM.66.5.2085-2095.2000, S. 2085–2095
- S. Rajmohan, C.E.R. Dodd, W.M. Waites: Enzymes from isolates of Pseudomonas fluorescens involved in food spoilage. In: Journal of Applied Microbiology. Jg. 93 Nr. 2, 2000 doi:10.1046/j.1365-2672.2002.01674.x, S. 205–213
- Belgin Dogan, Kathryn J. Boor: Genetic Diversity and Spoilage Potentials among Pseudomonas spp. Isolated from Fluid Milk Products and Dairy Processing Plants. In: APPLIED AND ENVIRONMENTAL MICROBIOLOGY. Jg. 69 Nr. 1, 2003 doi:10.1128/AEM.69.1.130-138.2003, S. 130–138
- Gabriel Morduchowicz, Silvio D. Pitlik, David Huminer, Michael Alkan, Moshe Drucker, Joseph B. Rosenfeld, Colin S. Block: Transfusion Reactions Due to Bacterial Contamination of Blood and Blood Products. In: Reviews of Infectious Diseases. Jg. 13 Nr. 2, 1991, S. 307–314
- A. P. Gibb, K. M. Martin, G. A. Davidson, B. Walker, W. G. Murphy: Rate of growth of Pseudomonas fluorescens in donated blood. In: Journal of Clinical Pathology. Jg. 48 Nr. 8, 1995, S. 717–718