Anethol
Anethol ist eine organisch-chemische Verbindung, die aufgrund ihres Biosyntheseweges zu den Phenylpropanoiden gezählt wird. Es ist ein Bestandteil von verschiedenen ätherischen Ölen z. B. Anisöl und kommt in verschiedenen Pflanzen wie Fenchel, Anis und Sternanis sowie in Syzygium anisatum und Clausena anisata vor. Anethol ist ein flüchtiger Aromastoff in Honig.[6] In der Natur kommen beide Isomere vor, allerdings liegt mehr trans-Anethol vor.[2] Der Geruch von Anethol ist ursächlich für das typische Anisaroma.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
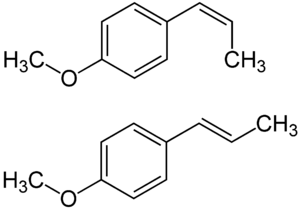 | |||||||||||||||||||
| cis-Anethol (oben) und trans-Anethol (unten) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Anethol | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C10H12O | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 148,22 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
| ||||||||||||||||||
| Dichte |
0,99 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Isomerie
Wegen der in Anethol enthaltenen Doppelbindung existieren zwei Isomere: cis- und trans-Anethol. Beide Isomere haben unterschiedliche physikalische Eigenschaften.
| Isomere von Anethol | ||
| Name | cis-Anethol | trans-Anethol |
| Andere Namen | (Z)-Anethol | (E)-Anethol |
| CAS-Nummer | 25679-28-1 | 4180-23-8 |
| 104-46-1 (undefiniert) | ||
| EG-Nummer | 247-181-4 | 224-052-0 |
| 203-205-5 (undefiniert) | ||
| ECHA-Infocard | 100.042.878 | 100.021.866 |
| 100.002.914 (undefiniert) | ||
| PubChem | 1549040 | 637563 |
| 7703 (undefiniert) | ||
| Wikidata | Q27147814 | Q255564 |
| Q27105777 (undefiniert) | ||
Ein Strukturisomer von Anethol ist Estragol.
Eigenschaften
In 1 l Ethanol sind 500 ml Anethol löslich. Dagegen ist es nur sehr schlecht in Wasser löslich. Der Flammpunkt liegt bei 90 °C. trans-Anethol ist ein weißer, kristalliner, süß schmeckender Feststoff, der bei 21,4 °C zu einer farblosen, öligen Flüssigkeit schmilzt. Das cis-Anethol ist flüssig und erstarrt bei −22 °C.
Physiologie
Anethol wirkt in der Lunge schleimlösend (sekretolytisch, sekretomotorisch) und schwach antibakteriell. Gleichzeitig zeigt es eine spasmolytische Wirkung, weswegen es als Expektorans und Karminativum eingesetzt werden kann.

Verwendung
Anethol kommt als Duft- und Aromastoff vor allem in Seifen und Mundpflegemitteln zum Einsatz. Wichtig ist daneben die Verwendung in der Spirituosenfabrikation als Aromatiseur für Spirituosen (Anisée, Anisette, Ouzo, Pernod, Rakı) und in der Lebensmitteltechnologie als Bestandteil von Aromen, hauptsächlich in Fruchtaromamischungen mit der Geschmacksrichtung Himbeere und Erdbeere.
Weblinks
- Riechstofflexikon: Anethol
Einzelnachweise
- Eintrag zu ANETHOLE in der CosIng-Datenbank der EU-Kommission, abgerufen am 1. November 2021.
- Eintrag zu Anethol. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. November 2014.
- Datenblatt trans-Anethole bei Sigma-Aldrich, abgerufen am 25. Januar 2020 (PDF).
- Datenblatt Anethol (PDF) bei Carl Roth, abgerufen am 19. Februar 2010.
- Eintrag zu Anethol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- Vojtěch Kružík, Adéla Grégrová, Aleš Rajchl, Helena Čížková: Study on Honey Quality Evaluation and Detection of Adulteration by Analysis of Volatile Compounds. In: Journal of Apicultural Science. Band 61, Nr. 1, 16. Juni 2017, S. 17–27, doi:10.1515/jas-2017-0002.
- Albert Gossauer: Struktur und Reaktivität der Biomoleküle, Verlag Helvetica Chimica Acta, Zürich, 2006, S. 210, ISBN 978-3-906390-29-1.
