Anandamid
Arachidonylethanolamid, auch Anandamid genannt, ist das Ethanolamin-Derivat der Arachidonsäure, einer vierfach ungesättigten Fettsäure, die besonders häufig im zentralen Nervensystem vorkommt. Anandamid wird vom Körper selbst gebildet (sofern Linolsäure vorliegt[2]) und ist somit eine endogene Substanz.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
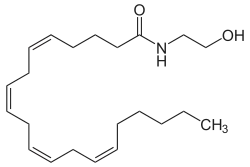 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Anandamid | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C22H37NO2 | ||||||||||||
| Kurzbeschreibung |
hellgelbe, ölige Flüssigkeit[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 347,53 g·mol−1 | ||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||
| Dichte |
0,92 g·cm−3[1] | ||||||||||||
| Löslichkeit | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Wirkung
Anandamid (von Sanskrit Ananda: Freude oder reines Glück) bindet an die Rezeptoren des Endocannabinoid-Systems, an denen auch das THC der Cannabis-Pflanze andockt. Es ist bei ausreichender Dosierung auch in der Lage, THC und weitere Cannabinoide zu verdrängen. Es bindet auch an Vanilloid-TRPV1-Rezeptoren.[3]
Die hauptsächlich interagierenden Regionen des Gehirnes scheinen diejenigen zu sein, die mit der Wahrnehmung und Gedankenverarbeitung bzw. den Bewegungsabläufen beschäftigt sind.
Anandamid kann durch die Cyclooxygenase-2 (nicht aber durch die Cyclooxygenase-1) zu Prostanoiden verstoffwechselt werden, deren Funktion noch unbekannt ist. Arachidonylethanolamid wird jedoch größtenteils durch Fettsäureamid-Hydrolase (FAAH) durch Spaltung zu Arachidonsäure und Ethanolamin abgebaut.
Im März 2008 veröffentlichten britische Wissenschaftler von der Universität Leicester im Journal of the American Medical Association einen Artikel, in dem sie die Vermutung aufstellen, eine erhöhte Anandamidkonzentration im Blut schwangerer Frauen könne ein Anzeichen für ein erhöhtes Fehlgeburtsrisiko sein.[4]
Struktur
Strukturchemisch gibt es zwischen Anandamid und THC signifikante Unterschiede. Die ausgeprägte Lipophilie (Fettlöslichkeit) hingegen ist beiden Verbindungen gemein. Detaillierte Untersuchungen ergaben jedoch, dass THC und Anandamid eine sehr ähnliche dreidimensionale Struktur besitzen.[5] Pharmakokinetisch wird Anandamid deutlich schneller abgebaut (nach ca. 30 Minuten kein Effekt mehr messbar) als THC, das einige Stunden wirksam bleibt.
Analytik
Zur zuverlässigen qualitativen und quantitativen Bestimmung in biologischem Untersuchungsmaterial kommen nach angemessener Probenvorbereitung die Kopplung der HPLC oder Kapillargaschromatographie mit der Massenspektrometrie in Frage.[6][7][8]
Vorkommen
Anandamid sowie die Ethanolamide zweier anderer ungesättigter Fettsäuren (Oleoyl- und Linoleoylethanolamid) wurden in Schokolade und Kakaopulver nachgewiesen.[9]
Entdeckung
Anandamid wurde 1992 vom tschechischen Chemiker Lumír Ondřej Hanuš und dem amerikanischen Molekularpharmakologen William Anthony Devane entdeckt;[10] kurz danach wurden seine pharmakologischen Wirkungen beschrieben.
Literatur
- R. Mechoulam, E. Fride: The unpaved road to the endogenous brain cannabinoid ligands, the anandamides. In: R. Pertwee (Hrsg.): Cannabinoid Receptors. Academic Press, London 1995, ISBN 0-12-551460-3, S. 233–258.
Einzelnachweise
- Datenblatt Arachidonylethanolamide bei Sigma-Aldrich, abgerufen am 16. Juni 2011 (PDF).
- DocCheck Medical Services GmbH: Arachidonsäure - DocCheck Flexikon. Abgerufen am 15. August 2018.
- R. A. Ross: Anandamide and vanilloid TRPV1 receptors. In: Br. J. Pharmacol. Band 140, Nr. 5, 2003, S. 790–801, doi:10.1038/sj.bjp.0705467, PMID 14517174.
- Osama M. H. Habayeb, Anthony H. Taylor, Mark Finney, Mark D. Evans, Justin C. Konje: Plasma Anandamide Concentration and Pregnancy Outcome in Women With Threatened Miscarriage. In: Journal of the American Medical Association. Band 299, Nr. 10, 2008, S. 1135–1136.
- J. Barnett-Norris, D. P. Hurst, D. L. Lynch, F. Guarnieri, A. Makriyannis, P. H. Reggio: Conformational memories and the endocannabinoid binding site at the cannabinoid CB1 receptor. In: J. Med. Chem. Band 45, Nr. 17, 2002, S. 3649–3659, PMID 12166938.
- R Ni, S Bhandari, PR Mitchell Jr, G Suarez, NB Patel, K Lamb, KS Bisht, DJ Merkler: Synthesis, Quantification, and Characterization of Fatty Acid Amides from In Vitro and In Vivo Sources. In: Molecules, 2021 Apr 27, 26(9), S. 2543, PMID 33925418
- C Lanz, J Mattsson, F Stickel, JF Dufour, R Brenneisen: Determination of the Endocannabinoids Anandamide and 2-Arachidonoyl Glycerol with Gas Chromatography-Mass Spectrometry: Analytical and Preanalytical Challenges and Pitfalls., Med Cannabis Cannabinoids. 2018 Jun 12;1(1):9-18, PMID 34676317
- CD Voegel, MR Baumgartner, T Kraemer, S Wüst, TM Binz: Simultaneous quantification of steroid hormones and endocannabinoids (ECs) in human hair using an automated supported liquid extraction (SLE) and LC-MS/MS - Insights into EC baseline values and correlation to steroid concentrations., Talanta. 2021 Jan 15;222:121499, PMID 33167212
- E. di Tomaso, M. Beltramo, D. Piomelli: Brain cannabinoids in chocolate. In: Nature. Band 382, Nr. 6593, 1996, S. 677–678, doi:10.1038/382677a0, PMID 8751435.
- W. A. Devane, L. Hanus, A. Breuer u. a.: Isolation and structure of a brain constituent that binds to the cannabinoid receptor. In: Science. Band 258, Nr. 5090, 1992, S. 1946–1949, PMID 1470919.