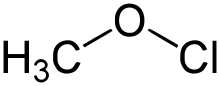
Alkylhypochlorite
Alkylhypochlorite sind Ester der hypochlorigen Säure und Alkoholen. Sie sind instabil und können spontan, unter Freisetzung hochgradig toxischer Dämpfe, explodieren. Die Instabilität der Alkylhypochlorite wird durch die Oxidationskraft der Hypochlorit-Gruppe hervorgerufen. Die Stabilität erhöht sich, je höher das nächstliegende C-Atom substituiert ist. So ist tert-Butylhypochlorit relativ stabil und kann als Reagenz verwendet werden. Alkylhypochlorite sind effiziente Chlorierungs- und Oxidationsmittel.[1]
Herstellung
Die Herstellung erfolgt durch Veresterung von Alkoholen mit hypochloriger Säure oder Chlor[2]:
Sicherheitshinweise
Alkylhypochlorite zersetzen sich unter Freisetzung von Chlorwasserstoff explosionsartig zu Aldehyden, daher ist auf entsprechende Sicherheitsmaßnahmen zu achten.[3]
Es werden verschiedene Zersetzungsmechanismen postuliert:
(nach Frederick Chattaway)
(nach J.F. Durand)
Einzelnachweise
- Science of Synthesis: Houben-Weyl Methods of Molecular Transformations Vol. 26 Ketones. Georg Thieme Verlag, 2014, ISBN 3-13-172011-5, S. 1228 (eingeschränkte Vorschau in der Google-Buchsuche).
- Steven V. Ley: Synthesis Carbon with One Heteroatom Attached by a Single Bond. Elsevier, 1995, ISBN 978-0-08-042323-4, S. 94 (eingeschränkte Vorschau in der Google-Buchsuche).
- THE THERMAL STABILITY OF ALKYL HYPOCHLORITES. (Nicht mehr online verfügbar.) In: SYMPOSIUM SERIES NO. 156. IChemE, 2011, archiviert vom Original am 20. Mai 2016; abgerufen am 20. Mai 2016 (englisch). Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.