Alkalische Phosphatase
Alkalische Phosphatase (AP, ALP, knochenspez. auch Ostase) ist der Name für Enzyme, die Phosphorsäureester hydrolysieren. Alkalische Phosphatasen entfernen Phosphat-Gruppen (Dephosphorylierung) von vielen Arten von Molekülen wie Proteinen, Nukleotiden und Alkaloiden. Sie arbeiten am effektivsten bei einem alkalischen pH-Wert.
| Alkalische Phosphatase E. coli K12 | ||
|---|---|---|
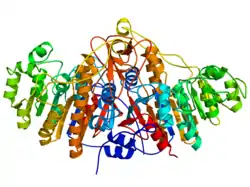 | ||
| Bändermodell des Dimer der alkalischen Phosphatase von E. coli, nach PDB 1ALK | ||
| Andere Namen |
AP, ALP, basische Phosphatase | |
|
Vorhandene Strukturdaten: 1aja, 1ajb, 1ajc, 1ajd, 1alh, 1ali, 1alj, 1alk, ,1anj 1ani ,1anj, 1b8j, 1ed8, 1ed9, 1elx, 1ely, 1elz, ,1ew8 1ew2 ,1ew8, 1ew9, 1hjk, 1hqa, 1k7h, 1kh4, 1kh5, ,1kh9 1kh7 ,1kh9, 1khj, 1khk, 1khl, 1khn, 1shn, 1shq, ,1urb 1ura ,1urb, 1y6v, 1y7a, 1zeb, 1zed, 1zef, 2anh, ,2ga3 2g9y ,2ga3, 2glq | ||
| Bezeichner | ||
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 3.1.3.1, Hydrolase | |
| Substrat | Phosphatmonoester + H2O | |
| Produkte | Alkohol + Phosphat | |
Alkalische Phosphatasen kommen in fast allen Lebewesen vor, ausgenommen wenige Pflanzen. Ein erhöhter Laborwert beim Menschen kann auf ein Krankheitsgeschehen, wie eine Gallenstauung, innere Organschäden, Knochenbrüche, einen Tumor oder Osteoporose/Osteomalazie (bei Kindern Rachitis) hindeuten.
Reaktion
Die alkalische Phosphatase hydrolysiert Phosphorsäureester zu Phosphat und Alkoholen, wobei Protonen entstehen.
Dieses Enzym arbeitet nur in schwach alkalischer Lösung mit einem pH-Optimum von 9,8. Gäbe man das Enzym zu einer ungepufferten Lösung, so käme die Reaktion wegen der Protonenfreisetzung zum Stillstand. In vitro kann sie also nur in Gegenwart eines Puffers von geeignetem pH-Wert verfolgt werden.
Alkalische Phosphatase ist ein in fast allen Geweben vorkommendes cytoplasmatisches Enzym, das eine wichtige Rolle bei Dephosphorylierungsreaktionen im Stoffwechsel spielt. Bisher wurden fünf gewebespezifische Isoenzyme gefunden, deren Aktivitätsoptimum bei einem pH-Wert von 9,8 liegt. Bei Leber- und Gallenfunktionsstörungen, Skeletterkrankungen, einigen Tumoren und bei Hyperthyreose steigt die Aktivität der AP im Serum. Die Bestimmung der enzymatischen Aktivität erfolgt durch den optischen Test.
Bei der DNA-Rekombinationstechnik findet die AP Anwendung zur Entfernung terminaler Phosphatgruppen vom 5'- oder 3'-Ende bzw. von beiden Positionen.
Selbst Mikroorganismen besitzen die ALP oder ALP-ähnliche Enzyme.
Die ALP besteht aus mindestens 500 Aminosäuren oder auch mehr, wobei die Anzahl schwanken kann. Die reaktive ALP ist kürzer, da sie bei der posttranslationalen Modifizierung[1] (PTM) gekürzt wird und entsprechend noch Zuckermoleküle angehängt werden. Dieser Vorgang wird Glykosylierung[2] genannt, weil so das organspezifische ALP-Isoenzym entsteht.
Inhibition
Humane gewebeunspezifische ALP sind besonders sensitiv gegenüber den Inhibitoren Levamisol und L-Homoarginin und werden bei Temperaturen unter 60 °C inaktiviert. Levamisol ist ein nicht-kompetitiver Inhibitor der alkalischen Phosphatase. Es hemmt zudem die Keimzellen-ALP sowie die gewebeunspezifische ALP. Die Inhibition wird durch höhere Konzentrationen von N-Ethylaminoethanol und Substrat verstärkt. L-Phenylalanin ist ein nicht-kompetitiver Inhibitor, der spezifisch an das Phosphoserylintermediat von Plazenta-[3] und Dünndarm-ALP bindet. 5‘-AMP hemmt Plazenta-ALP. Leucin ist ein nicht-kompetitiver Inhibitor von Plazenta-ALP,[3] Keimzellen-ALP, GAP. Imidazol ist ein Inhibitor der Plazenta-, Dünndarm-AP. Verschiedene organische Phosphate sind Inhibitoren, wie auch manche Reaktionsprodukte.
| Hemmung | Leber-AP | Knochen-AP | Darm-AP | Plazenta-AP |
|---|---|---|---|---|
| Hemmung durch Phenylalanin (%)[4] | 0-10 | 0-10 | 75 | 75 |
| Hemmung durch Homoarginin (%)[4] | 78 | 78 | 5 | 5 |
| Hemmung durch Hitzeinaktivierung (%)[4] | 50-70 | 90-100 | 50-60 | 0 |
Das bakterielle Enzym
In Gram-negativen Bakterien sitzen die alkalischen Phosphatasen im periplasmatischen Raum. Sie sind vergleichsweise thermostabil.[5]
Das humane Enzym
Im Menschen werden 15 verschiedene Isoenzyme unterschieden. Vier dieser Isoenzyme stammen von unterschiedlichen Genen (Dünndarm-AP, Plazenta-AP, Keimzell-AP und Gewebe-unspezifische AP). Die Gewebe-unspezifischen AP werden je nach Gewebe unterschiedlich glykosyliert, d. h., sie erhalten unterschiedliche Zuckerketten. Dadurch entstehen weitere Isoenzyme (Leber-AP, Knochen-AP, Nieren-AP).
Die höchste Konzentration an AP ist im Menschen in absteigender Reihenfolge in der Darmschleimhaut, Plazenta, Nieren- und Knochenzellen und der Leber vorhanden.
Bevor das Glycerin-3-Phosphat in den Zitronensäurezyklus eingeschleust wird, wird hier an dem dritten 3-C-Atom der Phosphatrest abgespalten. Hier wirkt die ALP.
Die plazentale und plazentaähnliche alkalische Phosphatase besteht aus 513 Aminosäuren, mit einer Übereinstimmung von 98 %. Dagegen bestehen die ALP in Leber, Nieren und Knochen aus 507 Aminosäuren. Es sind jedoch in den Aminosäuresequenzen Lücken enthalten, was einen Grad der Übereinstimmung von 50 bis 60 % ausmacht.[6]
Die ALP-Entwicklung entstand aus den nichtgewebespezifischen (TNAP, tissue nonspecific AP) und den drei gewebespezifischen ALPs.[7] Aus denen entstanden die drei gewebespezifischen Isoenzyme, IAP, GCAP und PLAP. Ein erhöhter ALP-Spiegel im Blutserum deutet auf eine krankhafte Störung im Organismus. Dagegen nimmt der ALP-Spiegel im menschlichen Organismus durch die natürliche Alterung ab. Grundsätzlich weisen sowohl Kinder im Wachstum als auch Frauen im letzten Schwangerschaftsdrittel höhere ALP-Werte auf. Dies ist jedoch normal und liefert keinen grundsätzlichen Hinweis auf eine Erkrankung.
Schwangere und Kinder haben einen höheren Wert, da bei ihnen der Knochenaufbau, insbesondere beim Fötus, noch nicht abgeschlossen ist; ebenso bei den Kindern bis zur Beendigung der Pubertät. Hier werden die freigesetzten Phosphorsäure als Phosphate an die Knochenmatrix angelagert, was als Hydroxylapatit die Festigkeit bewirkt.[8]
Labordiagnostik
Die Gesamtheit dieser Enzyme wird als „alkalische Phosphatase“ bei Standard-Blutuntersuchungen gemessen und kann Hinweise auf vorliegende Krankheiten der Leber und des Skeletts liefern.
Die plazentare Isoform (PLAP) wird normalerweise durch plazentare Syncytiotrophoblasten produziert. Ihre Bestimmung wird bei Seminomen empfohlen. Die Halbwertszeit im Blutserum beträgt weniger als drei Tage.
Referenzbereich
Für Messungen bei 37 °C nach IFCC:
- Säuglinge 110–590 IU/l
- Kleinkinder 110–550 IU/l
- Schulkinder 130–700 IU/l
- Frauen 55–147 IU/l
- Männer 62–176 IU/l
Interpretation
Alkalische Phosphatasen sind in großer Menge im Skelettsystem, im Leberparenchym und in den Gallengangsepithelien vorhanden. Zu hohe Werte können ihre Ursache z. B. in Erkrankungen der Leber, der Gallenblase, der Schilddrüse oder der Bauchspeicheldrüse haben. Auch bei Knochenerkrankungen wie Osteomalazie, Morbus Paget, Rachitis, Knochenmetastasen, Hyperparathyreoidismus oder auch bei Knochenbrüchen ist der Wert der AP in der Regel erhöht. Eine der häufigsten Ursachen für eine AP-Erhöhung sind maligne Tumoren, die in den Knochen metastasiert sind (Knochenmetastasen).
Grundsätzlich weisen sowohl Kinder im Wachstum als auch Frauen im letzten Schwangerschaftsdrittel höhere AP-Werte auf; dies ist jedoch normal und liefert keinen grundsätzlichen Hinweis auf eine Erkrankung.
Ein zu niedriger Gehalt an alkalischer Phosphatase findet sich z. B. bei der seltenen Erbkrankheit Hypophosphatasie; darüber hinaus als Begleiterscheinung eines Vitamin-C-Mangels (Skorbut), als Folge einer Bypass-Operation, bei Schilddrüsen-Unterfunktion (Hypothyreose), Morbus Wilson, Zinkmangel, schwerer Blutarmut, Magnesiummangel und bei Einnahme von Kontrazeptiva.
Bei der CML finden sich erniedrigte alkalische Phosphatase-Werte in den Granulozyten.
Anwendungsgebiete
Anwendung in der Biologie
In der Biochemie wird die Alkalische Phosphatase in Verbindung mit einem chromogenen Substrat für verschiedene Nachweismethoden (Färbungen) eingesetzt:
- Antikörperfärbung beim Western Blot zum Nachweis von Proteinen
- beim Northern Blot und Southern Blot zum Nachweis von RNA bzw. DNA
- bei der In-situ-Hybridisierung zum Nachweis von RNA
Als chromogenes Substrat wird hierbei häufig BCIP in Verbindung mit NBT verwendet, das von der Alkalischen Phosphatase zu einem blauen Indigo-Farbstoff umgesetzt wird.
In der Molekularbiologie wird die Alkalische Phosphatase zur Dephosphorylierung von linearer DNA eingesetzt.
Die gebräuchlichsten Alkalischen Phosphatasen sind:
- Bacterial Alkaline Phosphatase (BAP), aus Escherichia coli
- Calf Intestine Alkaline Phosphatase (CIAP), aus Kälberdarm
- Shrimp Alkaline Phosphatase (SAP), aus Eismeergarnelen (Pandalus borealis)
Alkalische Phosphatasen wurden früher in Bodansky-Einheiten gemessen.
Anwendung in der Milchindustrie
Die alkalische Phosphatase wird oft in der Milchindustrie als Nachweismethode für eine erfolgreiche Pasteurisierung verwendet. Der hitzeresistenteste Mikroorganismus in der Milch, Mycobacterium paratuberculosis, denaturiert bei Temperaturen unterhalb von denen der AP. Wird in der Probe keine AP-Aktivität nachgewiesen, so ist das Produkt erfolgreich pasteurisiert worden. Die Messung erfolgt im alkalischen Medium bei 37 °C mit Dinatriumphenylphosphat als Substrat. Ist aktive AP in der Probe vorhanden, wird Phenol frei, welches nach Umsetzung mit 2,6-Dibromchinin-1,4-chlorimid (Gibb’s Reagenz) photometrisch bestimmt und auf die AP-Aktivität umgerechnet wird.[9]
Literatur
- B. Neumeister, I. Besenthal, H. Liebrich: Klinikleitfaden Labordiagnostik. Urban & Fischer, München/ Jena 2003, ISBN 3-437-22231-7.
- L. Thomas: Labor und Diagnose. TH-Books, Frankfurt am Main 2005, ISBN 3-9805215-5-9.
- J. Sambrook, T. Maniatis, D. W. Russel: Molecular cloning: a laboratory manual. 3. Auflage. Cold Spring Harbor Laboratory Press, 2001, ISBN 0-87969-577-3.
Siehe auch
Weblinks
- Alkalische Phosphatase auf ExPASy.org
- Alkalische Phosphatase auf med4you.at
- Stabilität in Blutproben publiziert durch die WHO (PDF-Datei; 292 kB)
- H. N. Fernley, P. G. Walker: Studies on alkaline Phosphatase. In: Biochem J. 104(3), Sep 1967, S. 1011–1018. PMC 1271245 (freier Volltext)
- Stephen P. Coburn, J. Dennis Mahuren, Manas Jain, Yvonne Zubovic, Jacobo Wortsman: Alkaline Phosphatase (EC 3.1.3.1) in Serum Is Inhibited by Physiological Concentrations of Inorganic Phosphate. In: The Journal of Clinical Endocrinology & Metabolism. 83, 1998, S. 3951, doi:10.1210/jcem.83.11.5288.
- K. McDougall, C. Plumb, W. A. King, A. Hahnel: Inhibitor Profiles of Alkaline Phosphatases in Bovine Preattachment Embryos and Adult Tissues. In: Journal of Histochemistry & Cytochemistry. 50, 2002, S. 415, doi:10.1177/002215540205000312.
Einzelnachweise
- Uniprot: http://www.uniprot.org/
- S. Iino, L. Fishman: The effect of sucrose and other carbohydrates on human alkaline phosphatase isoenzyme activity. In: Clinica Chimica Acta. Volume 92, Issue 2, 1. März 1979, S. 197–207.
- A. Kozlenkov, T. Manes, M. F. Hoylaerts, J. L. Millán: Function assignment to conserved residues in mammalian alkaline phosphatases. In: The Journal of biological chemistry. Band 277, Nummer 25, Juni 2002, S. 22992–22999, doi:10.1074/jbc.M202298200. PMID 11937510.
- W. H. Fishman: Perspectives on alkaline phosphatase isoenzymes. In: The American journal of medicine. Band 56, Nummer 5, Mai 1974, S. 617–650. PMID 4596648.
- Robert B. McComb: Alkaline Phosphatase. Springer Science & Business Media, 2013, ISBN 978-1-4613-2970-1, S. 419.
- H. Harris: The human alkaline phosphatases: what we know and what we don't know. In: Clinica Chimica Acta. Band 186, Nummer 2, Januar 1990, S. 133–150. PMID 2178806 (Review).
- M. H. Le Du, J. L. Millan: Structural evidence of functional divergence in human alkaline phosphatases. In: The Journal of biological chemistry. Band 277, Nummer 51, Dezember 2002, S. 49808–49814, doi:10.1074/jbc.M207394200. PMID 12372831.
- W. H. Lee, C. Y. Loo u. a.: Osteoblast response to the surface of amino acid-functionalized hydroxyapatite. In: Journal of biomedical materials research. Part A. Band 103, Nummer 6, Juni 2015, S. 2150–2160, doi:10.1002/jbm.a.35353. PMID 25346517.
- Reinhard Matissek, Gabriele Steiner, Markus Fischer: Lebensmittelanalytik. 5. Auflage. Springer Verlag, 2013, ISBN 978-3-642-34828-0, S. 418.