Afrikanische Trypanosomiasis
Die Afrikanische Trypanosomiasis ist eine durch Unterarten von Trypanosoma brucei ausgelöste Tropenerkrankung, die auch als (Afrikanische) Schlafkrankheit bezeichnet wird. Sie kommt in den tropischen Gebieten Afrikas vor und wird von der Tsetsefliege übertragen. Die Erkrankung, eine chronisch verlaufende Protozoenerkrankung, verläuft in drei Stadien: Einige Wochen nach der Infektion kommt es zu Fieber, Schüttelfrost, Ödemen, Lymphknotenschwellung sowie Hautausschlag und Juckreiz. Im zweiten Stadium nach einigen Monaten stehen Symptome des Nervensystems im Vordergrund: Verwirrtheit, Koordinations- und Schlafstörungen sowie Krampfanfälle. Im Endstadium fällt der Patient in einen schläfrigen Dämmerzustand (Schlafsucht), der der Krankheit ihren Namen gegeben hat. Der Nachweis der Erreger erfolgt mikroskopisch im Blut oder dem Liquor cerebrospinalis sowie mit immunologischen Methoden. Zur Behandlung stehen mehrere Wirkstoffe zur Verfügung.
| Klassifikation nach ICD-10 | |
|---|---|
| B56.0 | Trypanosomiasis gambiensis |
| B56.1 | Trypanosomiasis rhodesiensis |
| B56.9 | Afrikanische Trypanosomiasis, nicht näher bezeichnet |
| ICD-10 online (WHO-Version 2019) | |
Erreger
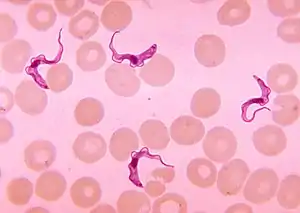
Die Schlafkrankheit wird durch humanpathogene Einzeller (Protozoen) aus der Gruppe der Trypanosomen hervorgerufen. Man unterscheidet zwei Erregertypen:
- Trypanosoma brucei gambiense (Erreger der Westafrikanischen Schlafkrankheit)
- Trypanosoma brucei rhodesiense (Erreger der Ostafrikanischen Schlafkrankheit)
Das Erbgut von Trypanosoma brucei wurde 2005 sequenziert.[1]
Übertragung

Als Erregerreservoir der Trypanosomen dienen Menschen, Rinder und Antilopen. Anders als bei Malaria sind die Überträger der Schlafkrankheit tagaktive, stechende und blutsaugende Tsetsefliegen. Man trifft sie im tropischen Afrika vorwiegend in Feuchtgebieten (Flussläufe, Sümpfe), aber auch in trockenen Savannenlandschaften (z. B. Kalahari) an. Der Stich ist sehr schmerzhaft und kann auch durch Bekleidung hindurch erfolgen. Die Erreger gelangen mit dem Fliegenspeichel in den Stichkanal. Er wird von der Fliege abgesondert, um Gerinnungsprozesse zu verhindern. Durch einen Stich werden mehrere tausend Erreger übertragen. Ein einziges übertragenes Trypanosom kann genügen, um die Krankheit auszulösen. Bremsen und Stechfliegen könnten (in besonderen Fällen) möglicherweise eine Rolle durch mechanische Übertragung spielen.[2]
Infektionsrisiko
Nicht alle Tsetsefliegen sind Trypanosomen-Überträger, so dass nicht jeder Stich zwangsläufig zu einer Infektion führt. Das Infektionsrisiko bei einem Stich ist regional sehr unterschiedlich und liegt durchschnittlich in der Größenordnung 1 %, denn auch die Durchseuchungsrate der Tsetse variiert stark. Das Risiko steigt also mit der Zahl der Stiche. Die Infektion trifft überwiegend die einheimische Bevölkerung, seltener Touristen.
Epidemiologie
Die Schlafkrankheit kommt mit einem schwer erfassbaren regionalen Verteilungsmuster im gesamten Tropengürtel Afrikas vor. Insgesamt sind nach Schätzungen der WHO mehr als 500.000 Menschen von der Schlafkrankheit betroffen. Durch die instabile politische Situation in vielen Regionen und daraus resultierende Flüchtlingsbewegungen hat die Erkrankungsrate in den letzten Jahren zugenommen.
Das Parasitenreservoir von T. b. gambiense besteht nach Dönges (1988)[3] hauptsächlich aus den infizierten, eventuell auch nur latent infizierten Menschen, einigen Haustieren, besonders dem Hausschwein (auch bei Desowitz (1981)) und der Riesenhamsterratte Cricetomys gambianus (Langschwanzmäuse). Piekarski (1962) nennt die Antilope unter den Wildtieren. Oft wird T. b. gambiense während des 1. Stadiums im Menschen nicht diagnostiziert und es folgt (oft erst nach Jahren) das schwerer zu behandelnde 2. Stadium.
T. b. rhodesiense fand sich weiterhin am häufigsten bei der Schirrantilope, gefolgt von dem Hausrind, der Kuhantilope, dem Afrikanischen Büffel, der Fleckenhyäne und dem Löwen (Dönges). In begrenzterem Umfang als bei T. b. gambiense ist auch hier der erkrankte Mensch ein Erregerreservoir. Piekarski nennt für beide Trypanosomenunterarten noch Ziegen und Schafe.
Welche Tierarten bei der Übertragung auf den Menschen die bedeutendste Rolle spielen, ist nicht abschließend geklärt, da ein kompliziertes Geflecht von anderen epidemiologischen Parametern beachtet werden muss (z. B. 31 Tsetse-Arten mit Vorlieben für bestimmte Wirtstiere, sowie Regenzeiten, soziale Faktoren, unterschiedliche Erregerstämme etc.). Das Infektionsrisiko ist deswegen lokal und regional sehr unterschiedlich. Die Parasitenreservoire sind zum großen Teil auch für jene Trypanosomen relevant, die bei afrikanischen Haus- und Nutztieren die sog. Nagana verursachen.
Neu berichtete Fälle (1990 bis 2020)
| Trypanosoma brucei gambiense[4] | 1990 | 1991 | 1992 | 1993 | 1994 | 1995 | 1996 | 1997 | 1998 | 1999 | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 | 2020 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Angola | 1498 | 2094 | 2406 | 1796 | 1274 | 2441 | 6726 | 8275 | 6610 | 5351 | 4546 | 4577 | 3621 | 3115 | 2280 | 1727 | 1105 | 648 | 517 | 247 | 211 | 154 | 70 | 69 | 36 | 35 | 19 | 18 | 79 | 30 | 33 |
| Benin | 0 | 0 | 2 | 1 | 0 | 0 | 0 | 0 | 0 | 20 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Burkina Faso | 27 | 27 | 20 | 17 | 18 | 13 | 12 | 1 | 15 | 15 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 0 |
| Kamerun | 86 | 69 | 21 | 3 | 20 | 21 | 17 | 10 | 54 | 32 | 27 | 14 | 32 | 33 | 17 | 3 | 15 | 7 | 13 | 24 | 16 | 15 | 7 | 6 | 7 | 6 | 6 | 5 | 7 | 17 | 2 |
| Zentralafrikanische Republik | 308 | 197 | 362 | 262 | 368 | 676 | 492 | 730 | 1068 | 869 | 988 | 718 | 572 | 539 | 738 | 666 | 460 | 654 | 1194 | 1054 | 395 | 132 | 381 | 59 | 194 | 147 | 124 | 76 | 57 | 86 | 39 |
| Tschad | 20 | 221 | 149 | 65 | 214 | 315 | 178 | 122 | 134 | 187 | 153 | 138 | 715 | 222 | 483 | 190 | 276 | 97 | 196 | 510 | 232 | 276 | 197 | 195 | 95 | 67 | 53 | 28 | 12 | 16 | 17 |
| Kongo | 580 | 703 | 727 | 829 | 418 | 475 | 474 | 142 | 201 | 91 | 111 | 894 | 1005 | 717 | 873 | 398 | 300 | 189 | 182 | 87 | 87 | 61 | 39 | 20 | 21 | 36 | 18 | 15 | 24 | 17 | 15 |
| Elfenbeinküste | 365 | 349 | 456 | 260 | 206 | 326 | 240 | 185 | 121 | 104 | 188 | 92 | 97 | 68 | 74 | 42 | 29 | 13 | 14 | 8 | 8 | 10 | 9 | 7 | 6 | 3 | 0 | 3 | 2 | 1 | 0 |
| Demokratische Republik Kongo | 7515 | 5825 | 7757 | 11384 | 19021 | 18182 | 19342 | 25094 | 26318 | 18684 | 16951 | 17300 | 13816 | 11459 | 10339 | 10249 | 8013 | 8155 | 7318 | 7178 | 5624 | 5590 | 5968 | 5647 | 3205 | 2351 | 1769 | 1110 | 660 | 604 | 395 |
| Äquatorialguinea | 63 | 36 | 45 | 30 | 85 | 37 | 46 | 67 | 62 | 28 | 16 | 17 | 32 | 23 | 22 | 17 | 13 | 15 | 11 | 7 | 8 | 1 | 2 | 3 | 0 | 0 | 3 | 4 | 4 | 3 | 1 |
| Gabun | 80 | 45 | 33 | 80 | 61 | 20 | 32 | 11 | 6 | 38 | 45 | 30 | 26 | 26 | 49 | 53 | 31 | 30 | 24 | 14 | 22 | 17 | 9 | 17 | 10 | 9 | 10 | 9 | 16 | 8 | 11 |
| Ghana | 3 | 6 | 16 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Guinea | 52 | 29 | 24 | 27 | 26 | 33 | 38 | 88 | 99 | 68 | 52 | 72 | 132 | 130 | 95 | 94 | 48 | 69 | 90 | 79 | 68 | 57 | 70 | 78 | 33 | 29 | 107 | 140 | 74 | 69 | 36 |
| Mali | 0 | 0 | 0 | 27 | 17 | 11 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Nigeria | 24 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 27 | 14 | 14 | 26 | 31 | 10 | 21 | 3 | 0 | 0 | 0 | 2 | 3 | 2 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 |
| Südsudan | 67 | 58 | 28 | 62 | 69 | 56 | 157 | 737 | 1726 | 1312 | 1801 | 1919 | 3121 | 3061 | 1742 | 1853 | 789 | 469 | 623 | 373 | 199 | 272 | 317 | 117 | 63 | 45 | 17 | 12 | 17 | 11 | 15 |
| Togo | 2 | 0 | 0 | 0 | 0 | 3 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Uganda | 2066 | 1328 | 2042 | 1764 | 1469 | 1062 | 981 | 1123 | 971 | 1036 | 948 | 310 | 604 | 517 | 378 | 311 | 290 | 120 | 198 | 99 | 101 | 44 | 20 | 9 | 9 | 4 | 4 | 0 | 1 | 2 | 1 |
| Total | 12756 | 10987 | 14088 | 16607 | 23266 | 23671 | 28736 | 36585 | 37385 | 27862 | 25841 | 26095 | 23799 | 19941 | 17100 | 15624 | 11372 | 10466 | 10380 | 9680 | 6973 | 6632 | 7091 | 6228 | 3679 | 2733 | 2131 | 1420 | 953 | 864 | 565 |
| Trypanosoma brucei rhodesiense [5] | 1990 | 1991 | 1992 | 1993 | 1994 | 1995 | 1996 | 1997 | 1998 | 1999 | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 | 2020 |
| Kenya | 91 | 8 | 4 | 2 | 1 | 0 | 2 | 5 | 14 | 22 | 15 | 10 | 11 | 0 | 0 | 0 | 1 | 0 | 0 | 1 | 0 | 0 | 2 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Malawi | 228 | 195 | 143 | 53 | 31 | 15 | 8 | 7 | 10 | 11 | 35 | 38 | 43 | 70 | 48 | 41 | 58 | 50 | 49 | 39 | 29 | 23 | 18 | 35 | 32 | 30 | 37 | 7 | 15 | 91 | 89 |
| Mosambik | 3 | 7 | 24 | 10 | 16 | No data | No data | No data | No data | No data | No data | No data | 1 | No data | 1 | No data | No data | No data | No data | No data | No data | No data | No data | No data | No data | No data | No data | No data | No data | No data | No data |
| Uganda | 1417 | 832 | 606 | 503 | 342 | 497 | 178 | 217 | 283 | 283 | 300 | 426 | 329 | 338 | 335 | 473 | 261 | 119 | 138 | 129 | 112 | 84 | 71 | 43 | 70 | 28 | 10 | 13 | 4 | 5 | 2 |
| United Republic of Tanzania | 187 | 177 | 366 | 262 | 319 | 422 | 400 | 354 | 299 | 288 | 350 | 277 | 228 | 113 | 159 | 186 | 127 | 126 | 59 | 14 | 5 | 1 | 4 | 1 | 1 | 2 | 3 | 3 | 0 | 3 | 1 |
| Sambia | 7 | No data | 4 | 1 | 1 | 1 | 3 | No data | No data | 15 | 9 | 4 | 5 | 15 | 9 | 7 | 6 | 10 | 13 | 4 | 8 | 3 | 6 | 6 | 12 | 8 | 2 | 3 | 5 | 15 | 6 |
| Simbabwe | No data | No data | No data | No data | 1 | No data | No data | 9 | No data | No data | No data | No data | No data | No data | No data | 3 | No data | No data | 0 | 3 | 2 | 4 | 9 | 1 | 3 | 3 | 1 | 1 | 0 | 2 | 0 |
| Total | 1933 | 1219 | 1147 | 831 | 710 | 935 | 591 | 583 | 606 | 619 | 709 | 755 | 617 | 536 | 552 | 707 | 453 | 305 | 259 | 187 | 154 | 111 | 101 | 85 | 115 | 68 | 52 | 27 | 24 | 116 | 98 |
Symptomatik
Der Krankheitsverlauf ist abhängig vom auslösenden Erreger. Bei Infektion mit Trypanosoma brucei gambiense ist der Krankheitsverlauf langsamer, bei Infektion mit Trypanosoma brucei rhodesiense in der Regel schneller und ausgeprägter.
Stadium I (Hämolymphatische Phase): Völlig symptomlos dringen die Trypanosomen bereits nach wenigen Stunden vom Blut in Parenchymzellen des Gehirns ein.[6] In der ersten Woche nach der Infektion kann es an der Einstichstelle zu einer schmerzhaften Schwellung mit zentralem Bläschen, dem sog. Trypanosomenschanker kommen. Dieses Symptom tritt jedoch nur bei einem Teil der Infizierten (5–20 %) auf. 1–3 Wochen nach der Infektion beginnt die eigentliche Parasitämie, die von Fieber, Schüttelfrost, Kopf- und Gliederschmerzen, Ödemen, Juckreiz, Exanthem und Lymphknotenschwellung begleitet wird. Häufig tritt diese Lymphknotenschwellung an den hinteren Halslymphknoten oder am Nacken auf und wird dann als Winterbottom-Zeichen bezeichnet. Hinzu treten Anämie und Thrombozytopenie, sowie erhöhte Immunglobulin-Spiegel.
Stadium II (Meningoenzephalitische Phase): Ca. 4–6 Monate nach Infektion (bei T. b. rhodesiense oft schon nach wenigen Wochen) zeigen sich die ersten Symptome des Eindringens in das Zentralnervensystem. Die Patienten leiden unter zunehmenden Verwirrungszuständen, Koordinations- und Schlafstörungen, Krampfanfällen, Apathie und Gewichtsverlust. Es können extrapyramidale Störungen oder ein Parkinson-Krankheit-ähnliches Krankheitsbild auftreten.
Im Endstadium fallen die Patienten in einen kontinuierlichen Dämmerzustand, der der Krankheit ihren Namen gegeben hat. Im Liquor cerebrospinalis ist eine Zellvermehrung (Pleozytose) nachweisbar. Nach einem Verlauf von Monaten bis Jahren endet die Krankheit tödlich.
Immunantwort
Die Trypanosomen sind von Glykoproteinen, den so genannten „variable surface glycoproteins“ (VSGs) umgeben. Die VSGs werden von den Einzellern im Rahmen der Vermehrung ständig variiert, wodurch sie der Immunantwort des Wirts entgehen (Antigenvariation). Im Trypanosomen-Genom sind über 1000 verschiedene VSG-Gene codiert, die abwechselnd exprimiert werden. Das menschliche Immunsystem kann zwar Antikörper gegen die vorherrschenden Antigene produzieren, aber immer nur einen Teil der Erreger eliminieren, da bereits neue Varianten im Blutkreislauf zirkulieren.
Eine andere, von Wissenschaftlern der TU Darmstadt und des Max-Planck-Instituts für Dynamik und Selbstorganisation entdeckte Abwehrmethode ist die Aufnahme der Antikörper durch den Erreger mittels einer strömungsdynamischen Besonderheit. Die Trypanosomen bewegen sich im Blutkreislauf mit hoher Geschwindigkeit voran und lenken die Antikörper dabei an den hinteren Zellpol, wo diese durch Endozytose aufgenommen, abgebaut und somit ihrer Wirksamkeit beraubt werden.[7]
Diagnostik
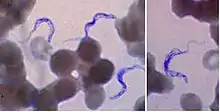
Im Stadium I werden die Erreger mikroskopisch im Blut („dicker Tropfen“), im Punktat des Schankers, im Knochenmarkaspirat oder mittels Lymphknotenbiopsie nachgewiesen. Zum Ausschluss des Stadium II erfolgt bei Parasitennachweis zusätzlich eine Untersuchung des Liquor cerebrospinalis. Als immundiagnostische Verfahren werden ELISA, IFT und PHA/IHA eingesetzt. Besonders bei der T. b. gambiense im späten Stadium kann der Erregernachweis im Blut misslingen.
Vorbeugung
Zurzeit ist weder eine medikamentöse Prophylaxe der Schlafkrankheit noch eine vorbeugende Impfung verfügbar. In der Mitte des letzten Jahrhunderts wurde Pentamidin, intramuskulär injiziert, erfolgreich als Prophylaxe eingesetzt. Diese war für mindestens sechs Monate effektiv (T. b. gambiense). Die heute einzig mögliche Vorbeugung besteht in der Vermeidung von Insektenstichen. Touristen sollten sich mit Repellents, Moskitonetzen und langärmeliger Kleidung schützen. Wichtig könnte auch das Tragen von heller Kleidung sein, da die Tsetsefliege besonders von blau und schwarz angezogen wird. Diese Maßnahmen sind jedoch nur bedingt erfolgreich, da Tsetsefliegen aggressiv vorgehen und schnell eine ungeschützte Stelle am Körper finden.
Therapie
Aufgrund der Toxizität der verfügbaren Medikamente wird die Schlafkrankheit in den meisten Fällen stationär behandelt. Im Stadium II werden Arsenverbindungen eingesetzt, die ausgeprägte Nebenwirkungen auslösen. Die Letalität kann hier bis zu 10 % betragen.
- Stadium I: Gabe von Suramin (T. b. rhodesiense/gambiense) oder Pentamidin (T. b. gambiense). Beide Medikamente wirken nicht auf Erreger im Zentralnervensystem, da sie die Blut-Hirn-Schranke nicht überwinden.
- Stadium II: Gabe von Melarsoprol oder Eflornithin, früher auch Tryparsamid (T. b. gambiense). Beide Medikamente wirken gegen Erreger im zentralen Nervensystem, sind jedoch neurotoxisch.
Im November 2018 wurde in Europa ein Medikament mit dem Wirkstoff Fexinidazol zur Zulassung empfohlen,[8] das als Tablette eingenommen werden kann und die Patienten in beiden Stadien innerhalb von zehn Tagen heilt.[9] Der Wirkstoff wurde zuvor in Afrika an 750 Patienten erfolgreich getestet.[10]
Geschichte
David Bruce erforschte als einer der Ersten die Epidemiologie der Krankheit in Afrika.
Den Erreger (Trypanosoma gambiense) entdeckten 1901 R. M. Forde und J. E. Dutton.[11]
Auf Grundlage der Arbeiten von Harold Wolferstan Thomas und Anton Breinl erforschte Robert Koch die Wirkung von Atoxyl gegen die Erkrankung. Paul Ehrlich entwickelte daraus das Arsphenamin, das zuerst von Werner von Raven in Togo erprobt wurde. Als vorbeugendes Chemotherapeutikum wurde vor der Entdeckung der Antibiotika das arsenhaltige Medikament Stovarsolan[12] verwendet.
Das erste effektiv wirksame Medikament gegen Schlafkrankheit ist das um 1920er bei Bayer entwickelte Suramin (Germanin, Bayer 205), dessen Entdeckung in Deutschland zur Zeit des Nationalsozialismus zu Propagandazwecken[13] genutzt wurde.
Literatur
- Sarah Ehlers: Europa und die Schlafkrankheit. Koloniale Seuchenbekämpfung, europäische Identitäten und moderne Medizin 1890–1950. Göttingen 2019, ISBN 978-3-525-31068-7.
- Peter GE Kennedy: Clinical features, diagnosis, and treatment of human African trypanosomiasis (sleeping sickness). In: The Lancet Neurology. 12, 2013, S. 186–194. doi:10.1016/S1474-4422(12)70296-X
- Stefan Winkle: Geißeln der Menschheit – Kulturgeschichte der Seuchen. 3. Auflage. Artemis & Winkler Verlag, 2005, ISBN 3-538-07159-4.
Weblinks
- Afrikanische Trypanosomiasis. In: Orphanet (Datenbank für seltene Krankheiten).
- Factsheet der WHO (englisch)
- Informationen zur Schlafkrankheit der Ärzte ohne Grenzen
- Information der CDC (englisch)
Einzelnachweise
- M. Berriman u. a.: The genome of the African trypanosome Trypanosoma brucei. In: Science. 2005 Jul 15;309(5733), S. 416–422. PMID 16020726
- T. Cherenet u. a.: Seasonal prevalence of bovine trypanosomosis in a tsetse-infested zone and a tsetse-free zone of the Amhara Region, north-west Ethiopia. In: Onderstepoort J Vet Res. 2004 Dec;71(4), S. 307–312. PMID 15732457.
- C. Moll-Merks, H. Werner, J. Donges: Suitability of in-vitro xenodiagnosis: development of Trypanosoma cruzi in Triatoma infestans depending on larval stage of bugs and number of trypomastigotes taken during in-vitro blood meal. In: Zentralbl Bakteriol Mikrobiol Hyg [A]. 1988 Mar;268(1), S. 74–82. PMID 3134769
- Number of new reported cases (T.b. gambiense). World Health Organization. 22. Juli 2021. Abgerufen am 26. November 2021.
- Number of new reported cases (T.b. rhodesiense). World Health Organization. 22. Juli 2021. Abgerufen am 26. November 2021.
- U. Frevert, A. Movila u. a.: Early invasion of brain parenchyma by african trypanosomes. In: PloS one. Band 7, Nummer 8, 2012, S. e43913. doi:10.1371/journal.pone.0043913. PMID 22952808. PMC 3432051 (freier Volltext).
- M. Engstler, T. Pfohl, S. Herminghaus, M. Boshart, G. Wiegertjes, N. Heddergott, P. Overath: Hydrodynamic flow-mediated protein sorting on the cell surface of trypanosomes. In: Cell. Band 131, Nummer 3, November 2007, S. 505–515, doi:10.1016/j.cell.2007.08.046, PMID 17981118.
- CHMP recommends first oral-only treatment for sleeping sickness | European Medicines Agency. Abgerufen am 23. November 2018 (englisch).
- Celine Müller: Erste orale Therapie der Schlafkrankheit. In: Deutsche Apotheker Zeitung. 19. November 2018, abgerufen am 20. November 2018.
- Donald G. McNeil Jr.: Rapid Cure Approved for Sleeping Sickness, a Horrific Illness. In: New York Times. 16. November 2018, abgerufen am 20. November 2018 (englisch).
- Werner Köhler: Infektionskrankheiten. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 667–671; hier: S. 671.
- J. L. Kritschewsky, K. A. Friede: Die Chemoprophylaxis des Rückfallfiebers und der Trypanosomenerkrankungen durch das Stovarsolan. Leipzig 1925.
- Eva Anne Jacobi: Das Schlafkrankheitsmedikament Germanin als Propagandainstrument: Rezeption in Literatur und Film zur Zeit des Nationalsozialismus. In: Würzburger medizinhistorische Mitteilungen. Band 29, 2010, S. 43–72.