4-Methylaminorex
4-Methylaminorex (syn. Euphoria) ist eine psychotrope Substanz aus der 2-amino-5-aryloxazolin Gruppe mit Stimulanter Wirkung, die der von Amphetamin ähnelt.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
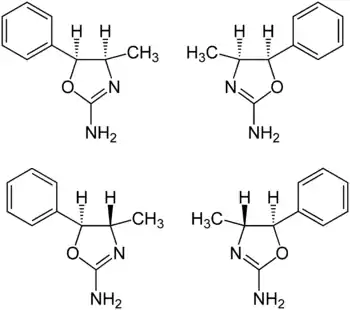 | ||||||||||||||||
| (4R,5S)-Form (links oben), (4S,5R)-Form (rechts oben),
(4S,5S)-Form (links unten) und (4R,5R)-Form (rechts unten) | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | 4-Methylaminorex | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C10H12N2O | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 176,21 g·mol−1 | |||||||||||||||
| Schmelzpunkt |
Racemat aus (4R,5S)-Form und (4S,5R)-Form: 154,5–156 °C sowie 139–142 °C[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Geschichte
Die Substanz[4] wurde in den frühen 1960er Jahren als Appetithemmer entwickelt[5] und 1964 patentiert.[6] 1963 wurde eine stark euphorisierende Nebenwirkung nachgewiesen.[7] Deshalb wurde die Substanz nicht vermarktet. Illegal wird sie unter den Bezeichnungen Euphoria, U4Euh, Intellex, Verbosamin, Aminorex oder Ice gehandelt. Die Bezeichnung Ice rührt vom Aussehen der milchigen bis klaren Kristalle her, die als Rocks oder Steine zum Teil in großen Stücken verkauft werden. Auch Methamphetamin wird als Ice illegal vermarktet; daher kann es zu Verwechslungen kommen.
Besucher einer Musikveranstaltung berichteten 1986 über unangenehme Empfindungen und Aggressionen, nachdem sie Euphoria zusammen mit LSD eingenommen hatten. Daher hatte die Droge eine Zeitlang einen schlechten Ruf. Inzwischen ist die Substanz wieder relativ begehrt, aber nicht allzu verbreitet. 1987 wurde 4-Methylaminorex in den USA als illegal erklärt. Einige größere Untergrundlabore hatten hauptsächlich diese Droge hergestellt. 4-Methylaminorex ist auch in Deutschland dem Betäubungsmittelgesetz (BtMG) unterstellt und als nicht verkehrsfähiges Betäubungsmittel[8] illegal.
Stereoisomere
4-Methylaminorex enthält zwei stereogene Zentren, es existieren also folgende vier Stereoisomere:
- (4R,5S)-Form
- (4S,5R)-Form
- (4S,5S)-Form
- (4R,5R)-Form
Es ist bekannt, dass die Stereoisomere unterschiedliche pharmakologische Wirkungen haben.[9]
Das Racemat (1:1-Gemisch) aus der (4R,5S)-Form und der enantiomeren (4S,5R)-Form wird auch cis-(±)-4-Methylaminorex genannt.
Anwendungsweise
Aufgrund des niedrigen Schmelzpunktes können die Kristalle auf Aluminiumfolie erhitzt und die Dämpfe mit einem Röhrchen inhaliert werden.[4] Die orale Einnahme ist weniger verbreitet, da die geringen benötigten Mengen ohne Laborwaage schwer abzuschätzen sind. Die Bioverfügbarkeit der einzelnen Applikationswege beträgt wie folgt: 62 % oral; 79 % intranasal; 91–93,5 % verdampft; 100 % intravenös. Bedingt durch den niedrigen Schmelzpunkt ist es schwer, die Substanz unauffällig mit anderen Substanzen zu strecken, wie es bei Kokain und Heroin üblich ist.
Wirkung
Psychische Wirkung
Rauchen von rund 10 mg erzeugt Wohlbefinden und für rund 4–6 Stunden eine stimulierende und aufputschende Wirkung.[4] Viele Konsumenten fühlen sich intelligenter und glauben, Probleme unter Einfluss der Substanz besser lösen zu können. Monotone Arbeitsabläufe sollen leichter fallen und als weniger belastend empfunden werden. Als Leistungsdroge soll 4-Methylaminorex effektiver als Amphetamin sein, weil Fehlhandlungen und Verwirrtheit, abhängig von der Dosis, seltener auftreten. Höhere Dosen ab ca. 50 mg führen zu Euphorie zu Lasten der Konzentrationsfähigkeit. Die körperliche Müdigkeit wird ausgeschaltet; Schlaf wird unmöglich. Die Konsumenten haben das Bedürfnis, immer neue Unternehmungen anzufangen oder ununterbrochen zu reden.
Dieser Zustand kann durch weitere Einnahme mehrere Tage lang aufrechterhalten werden. Mitunter werden Schlafmittel eingenommen, um der quälenden Schlaflosigkeit zu begegnen.
Körperliche Wirkung
Häufige Nebenwirkungen sind Durchfall, Mundtrockenheit und übler Mund- und Körpergeruch.[4] Körperliche Gewöhnung tritt schnell ein. Bei fortwährendem Gebrauch benötigt der Konsument immer höhere Dosen. Durch Abstinenz wird dies nach einiger Zeit wieder abgebaut.
Aufgrund der strukturellen Verwandtschaft mit dem Appetitzügler Aminorex könnte, bei anfälligen Personen, eine Pulmonale Hypertonie als Folge des chronischen Konsums auftreten. Im Zusammenhang mit 4-Methylaminorex steht ein Fall bei dem drei Familienmitglieder mit einer Pulmonalen Hypertonie diagnostiziert wurden. Der Zusammenhang wurde allerdings erst nach einer unabhängigen, von der DEA durchgeführten, Durchsuchung des Grundstücks und einem darauffolgenden Fund von rund 10 Kilogramm 4-Methylaminorex gezogen.[10]
Trivia
Die in dem Film Interstate 60 als Euphoria bezeichnete Droge wird dort als Machtmittel genutzt, um Arbeitskräfte in einer Stadt zu halten. Ob es sich bei der fiktiven Droge tatsächlich auch um 4-Methylaminorex handelt, ist fraglich.
Die Droge wird in der Folge Aktion Eiertausch (2x15) der Serie Beverly Hills, 90210 thematisiert. Brandon Walsh lehnt Drogen generell ab. Seine Freundin Emily Valentine mixt ihm heimlich Euphoria in einen Drink, was letztlich zum Aus der Beziehung führt.
Literatur
- Ralph Parnefjord: Das Drogentaschenbuch. 3. Auflage. Thieme, Stuttgart 2005, ISBN 978-3-13-118033-9, S. 56–58.
Weblinks
- 4-Methylaminorex. In: Erowid. (englisch)
Einzelnachweise
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1039, ISBN 978-0-911910-00-1.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Eintrag zu 4-Methylaminorex in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Dieser Abschnitt folgt, soweit nicht ausdrücklich andere Quellen angegeben sind, der Darstellung in Parnefjord, Das Drogentaschenbuch, 3. Auflage, Thieme Verlag 2005, S. 56–58
- G. I. Poos, J. Carson, J. Rosenau, A. Roszkowski, N. Kelly, J. McGowir: 2-Amino-5-Aryl-2-Oxazolines: New Anorectic Agents. In: Journal of Medicinal Chemistry. Band 6, 1963, S. 266–272.
- Patent US3161650: 2-Amino-5-Aryloxazoline Products. Veröffentlicht am 1964, Erfinder: G. Poos.
- J. Yelnasky, R. Katz: Sympathomimetic Actions of cis-2-Amino-4-Methyl-5-Phenyl-2-Oxazoline. In: Journal of Pharmacology and Experimental Therapeutics. Band 140, 1963, S. 180.
- Anlage I (zu § 1 Abs. 1), nicht verkehrsfähige Betäubungsmittel).
- R. A. Glennon und B. Misenheimer, Pharmacology and Biochemical Behaviour 35 (1990) 517.
- Seán P. Gaine, Lewis J. Rubin, James J. Kmetzo, Harold I. Palevsky, Thomas A. Traill: Recreational Use of Aminorex and Pulmonary Hypertension. In: Chest. 23. März 1963, doi:10.1378/chest.118.5.1496.