Wanzenpflanzen
Die Wanzenpflanzen (Roridula), auch Taupflanzen genannt, sind die einzige und nur aus zwei Arten bestehende Gattung der Familie der Wanzenpflanzengewächse (Roridulaceae) in der Kapensis. Die in Südafrika heimischen Halbsträucher fangen mit ihren klebrigen Blättern Insekten, die von auf der Pflanze lebenden Wanzen und Spinnen gefressen werden. Deren Ausscheidungen wiederum werden von den Blättern der Pflanze als Dünger absorbiert.
| Wanzenpflanzen | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|

Roridula gorgonias | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name der Familie | ||||||||||||
| Roridulaceae | ||||||||||||
| Engl. & Gilg | ||||||||||||
| Wissenschaftlicher Name der Gattung | ||||||||||||
| Roridula | ||||||||||||
| Burm.f. ex L. |
Beschreibung
Beide Arten sind bis zu 2 Meter hohe, immergrüne Halbsträucher. Ihr Wurzelwerk besteht aus einer stark ausgebildeten Pfahlwurzel mit nur schwach ausgeprägten, feinen Seitenwurzeln. Die ausdauernde Sprossachse ist aufrecht, verholzend und nur schwach verzweigt.
Bei beiden Arten konnte ein deutliches sekundäres Dickenwachstum nachgewiesen werden, bei Roridula dentata auch Jahresringe. Einzelne, spiralig verdickte Tracheen finden sich verstreut in Wurzeln und Stängeln. Im primären Stamm sind die einzelnen Leitbündel durch einen Ring aus Faserzellen miteinander verbunden. Die Holzstrahlen sind einreihig, einzigartig sind die aufrecht angeordneten Speicherzellen. Die Siebröhren-Plastiden gehören dem Ss-Typ an (= S-Typ mit Stärke).
Stängel und Blätter reflektieren gleichermaßen UV-Strahlen und locken so Insekten an.[1]
Blätter
Die gelblich-grünen, linealischen bis sich verjüngenden Laubblätter sind wechselständig, nebenblattlos, entweder ganzrandig oder zur Seite hin kurz linealisch gelappt. Sie stehen unterhalb der Sprossenden lichter. Die Blätter sind an den Blatträndern mit gestielten Drüsen von unterschiedlicher Länge besetzt, die dem Insektenfang dienen. Der von diesen Drüsen abgesonderte Fangschleim der Wanzenpflanzen basiert im Gegensatz zu dem der meisten anderen karnivoren Gattungen mit Klebefallen nicht auf Wasser, sondern auf Kautschuk, und ist extrem klebrig. Er hält auch größere Insekten wie Schmetterlinge oder Libellen fest. Bemerkenswert ist die, bei höheren Pflanzen äußerst seltene, sogenannte circinate Vernation, bei der die jungen Blätter während des Wachstums wie bei einem Bischofsstab schneckenartig eingerollt sind und sich von der Blattbasis her entrollen.

Blüten
Die zwittrigen, mittelgroßen und attraktiven Blüten stehen in traubenförmigen, wenigblütigen, endständigen Blütenständen. Die doppelte Blütenhülle ist unverwachsen und radiärsymmetrisch. Die Kronblätter sind blassviolett, rosa oder weiß, breit umgekehrt-eiförmig und kahl. In der Knospe sind die Kronblätter dachziegelartig übereinandergelegt (imbricat).
Die fünf Staubblätter stehen den Kelchblättern gegenüber, die fadenförmigen Staubfäden sind unverwachsen. Die Staubfäden setzen (annähernd) an der Basis der Staubbeutel an (basifix) und haben zwei Theken. Diese öffnen sich zum Zentrum der Blüte hin und stehen unterhalb des Fruchtknotens. Am Ansatz der Staubbeutel findet sich eine Ausbeulung des Konnektivs, die Nektar enthält. Das Tapetum ist drüsig. Die Pollenkörner entstehen sämtlich zu gleicher Zeit und sind bei der Freisetzung zweikernig. Die Staubfäden sind während der Blüte reizbar; wenn sie berührt werden, springen die Staubbeutel an der Spitze auf und schleudern den Pollen durch die Öffnungen heraus.
Das Gynoeceum besteht aus drei verwachsenen Fruchtblättern, der daraus gebildete Fruchtknoten ist oberständig mit zentralwinkelständiger Plazentation. Die Samenanlagen sind anatrop und haben nur ein Integument (Unitegmie). Der Embryosack entwickelt sich nach dem Polygonum-Typ. Die Polkerne verschmelzen noch vor der Befruchtung, das Endosperm bildet sich zellulär und der Embryo entwickelt sich nach dem Solanaceen-Typus. Der Griffel ist endständig, papillös und aufrechtstehend.
Frucht und Samen
Die Frucht ist eine glatte, knorpelige, dreifächrige Kapsel, die Fruchtwände reißen mittig auf. Sie enthält zahlreiche, elliptische, dunkel rotbraune Samen. Die Samen haben einen Durchmesser von 5 Millimetern und besitzen eine harte Samenschale mit stark verdickten Zellwänden. Im Inneren befinden sich reichlich fleischiges Endosperm und ein länglicher Embryo.
Cytologie und Inhaltsstoffe
Die Chromosomenzahl beträgt 2n = 12. In den Epidermiszellen nahe den Seiten- und Mittelrippen finden sich Kristallsand-Ablagerungen, im Endosperm sowie den Integumenten Tannine. Naphthochinone fehlen, Iridoide konnten nachgewiesen werden.
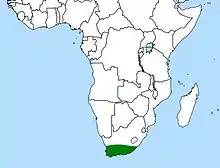
Verbreitung
Wanzenpflanzen sind Florenelemente der Capensis und endemisch im Areal der früheren Kapprovinz Südafrikas in den Zederbergen und dem Raum um Hermanus. Sie wachsen dort in Höhenlagen zwischen 100 und 1200 Meter in bergigen, teils nebelfeuchten Regionen. Die Standorte liegen im Fynbos, einer heideartigen Vegetation, auf sumpfigem Terrain mit schwarzen Böden, oder an Hängen mit Sickerwasser bzw. nahe Wasserläufen auf sauren und extrem nährstoffarmen Sandböden zwischen Quarzitfelsen. Dort sind die Pflanzen vergesellschaftet mit Torfmoosen (Sphagnum) oder Grubbia rosmarinifolia[2].
Alle Vorkommen sind voneinander isoliert und umfassen von wenigen bis zu 2000 Pflanzen. Beide Arten sind selten, Roridula gorgonias ist gefährdet.[3]
Ökologie
Präkarnivorie

Die Wanzenpflanzen verwerten ihren Fang indirekt in einer mutualistischen Symbiose mit zwei spezialisierten Wanzenarten der Gattung Pameridea (Pameridea marlothii sowie Pameridea roridulae, letztere nur bei Roridula gorgonias). Diese leben ausschließlich auf den Wanzenpflanzen, finden die Beutetiere innerhalb von wenigen Minuten nach dem Fang[4] und ernähren sich von den gefangenen Tieren, im Falle von mangelnder Beute saugen sie jedoch auch Pflanzensäfte[5]. Wie genau die Wanzen selbst sich vor dem Kleben-Bleiben schützen, war lange Zeit unklar[6], vermutet wurde, dass die Tiere über die spezielle Gestalt ihrer Tarsi befähigt sind, sich an den unteren Partien der Stieldrüsen der Pflanzen festzuhalten und dabei weitgehend nicht in Kontakt mit der klebrigen Spitze zu kommen[7]. 2008 konnte dann nachgewiesen werden, dass die Tiere am ganzen Körper mit einer dicken Sekretschicht bedeckt sind, die als „Anti-Haft-Schicht“ wirkt[8].
Die Ausscheidungen der Wanzen nimmt die Pflanze als Blattdünger durch die Kutikula auf und nutzt so indirekt die Nährstoffe ihres Fangs[9]. Bis zu 70 % ihres Stickstoffbedarfs können die Pflanzen auf diesem Wege decken, ein im Vergleich mit anderen fleischfressenden Pflanzen sehr hoher Wert[10]. Hauptsächlich gefangen werden fliegende Insekten wie Fliegen, Wespen und andere Hautflügler, bis hin zu großen Beutetieren wie Schmetterlingen und Libellen. Die Untersuchung eines Fanges einer Roridula gorgonias ergab, dass sie innerhalb von acht Wochen 109 Insekten größer als 2 Millimeter (10,1 % Käfer, 80,6 % Zweiflügler) und 112 kleinere (52 % Fransenflügler, 35 % Zweiflügler) erbeutete[4].
Ebenfalls von den Fängen der Pflanze, aber auch von den Wanzen selbst, ernährt sich wiederum die Krabbenspinne Synema marlothii. Ihre Anwesenheit schadet den Pflanzen jedoch durch die Minderung der Wanzenbestände und – als Folge davon – durch eine Reduktion des aus der Verwertung von Beute stammenden Stickstoffs von 70 % auf bis zu 30 %.[10]

Charles Darwin untersuchte 1875 erstmals Wanzenpflanzen auf eine mögliche Karnivorie, kam aber zu keinem Ergebnis[11]. Aufgrund der Symbiose und dem Fehlen von absorptionsfähigen Gefäßen in den Drüsen wurden sie anhand von Untersuchungen von Rudolf Marloth 1910 als sogenannte präkarnivore Pflanze eingestuft. Man ging also davon aus, dass sie zwar Vorrichtungen zum Fang von Insekten haben, diese aber nicht selbstständig verdauen könnten und sie daher nicht als fleischfressend im eigentlichen Sinne anzusehen seien. 2006 konnte dann in der Epidermis eine hohe Phosphatase-Aktivität belegt werden, ein Hinweis darauf, dass die Blattoberflächen der Pflanzen ebenfalls Enzyme produzieren und so zur Verdauung zumindest beitragen, wenngleich nicht ausgeschlossen werden kann, dass diese Werte allein aus der hohen Stoffwechselaktivität der Pflanze resultieren. Unzweifelhaft ist jedoch, dass die Insekten den größten Anteil an der Verdauung haben.[12]
Bestäubung
Roridula-Arten sind hauptsächlich selbstbestäubend, Fremdbestäubung ist selten. Als Bestäuber dienen zumeist die Wanzen.[13] Die Tiere durchbohren mit ihren Saugrüsseln die Konnektive der Staubbeutel, um so an den dort enthaltenen Nektar zu gelangen. Dadurch drehen sich die Staubbeutel schlagartig um 180 Grad, setzen durch die Öffnungen an der Spitze des Staubbeutels den Pollen frei und stäuben die Wanzen damit ein.
Selten dienen auch andere Tierarten als Bestäuber, festgestellt wurden Allodape punctata und Xylocopa albifrons (beide aus der Familie Echte Bienen) und Ceroctis capensis, ein Ölkäfer. Die Bienen sind sogenannte Buzz-Pollinators, das Summen der Tiere also löst die Staubbeutel aus. Der Besuch insbesondere von Bienen ist wichtig für den genetischen Austausch der Populationen, da Bienen auch größere Strecken zurücklegen können, allerdings ist der Besuch der nur kurzgestielten und sich somit nahe der Blätter befindlichen Blüte für diese Tiere mit der Gefahr verbunden, gefangen zu werden.[13]
Feuerökologie
Beide Arten sind pyrophil, also in mehrfacher Hinsicht an die regelmäßig alle paar Jahre auftretenden Buschbrände angepasst und teils auch darauf angewiesen. Die Feuer lichten zum einen die Vegetation und verhindern so, dass die Wanzenpflanzen überwuchert werden, zum anderen erlauben sie den Samen, unter offenen Bedingungen zu keimen und zu wachsen.
Niedergebrannte ältere Pflanzen treiben nach dem Feuer aus dem feuerfesten Wurzelstock wieder aus. Dies kann jedoch durch die saisonalen Bedingungen verzögert werden, so dass Pflanzen nach dem Niederbrennen erst durch die Ruhephase gehen und danach wieder ausschlagen. So können zwischen Brand und Neuaustrieb bis zu sechs Monate vergehen.

Systematik
Gattung wie Arten sind deutlich voneinander abgegrenzt und unumstritten, zwei Arten werden anerkannt:
- Roridula dentata L.
- Roridula gorgonias Planch.
Die Typusart ist Roridula dentata. Vier weitere beschriebene Taxa (Roridula crinita, Roridula verticilliata, Roridula muscicarpa, Roridula × brachysepala ) werden durchweg verworfen und als Synonyme eingestuft. Nicht zur Gattung gehören weitere zwischen 1775 und 1818 als Roridula beschriebene Arten, bei denen es sich um Taxa der – nicht näher verwandten – Gattung Cleome in der Familie der Kaperngewächse (Capparaceae) handelt.[14]
Deutlich weniger klar jedoch war lange die Position der Gattung. Historisch wurde sie unter anderem den Sonnentaugewächsen (Droseraceae, bei Bentham und Hooker 1865), den Grätenblattgewächsen (Ochnaceae, bei Planchon 1848) und den Scheinellergewächsen (Clethraceae, bei Hallier 1912) zugeordnet. 1924 dann beschrieben Adolf Engler und Ernst Friedrich Gilg die Gattung als eigenständige Familie, dem folgten Marloth (1925) und Diels (1930). Zwar wurde diese Einstufung im Laufe des 20. Jahrhunderts mehrfach in Frage gestellt, unter anderem durch Platzierungen bei den Regenbogenpflanzengewächsen (Byblidaceae), mittlerweile aber hat sich die Behandlung als eigene Familie durchgesetzt, auch molekulargenetische Untersuchungen bestätigten dies. Diesen zufolge ist die Gattung verwandt mit den amerikanischen Schlauchpflanzengewächsen (Sarraceniaceae) und den Strahlengriffelgewächsen (Actinidiaceae).[15]
| |||||||||||||||||||
Paläobotanik
2014 wurden zwei 35 bis 47 Mio. Jahre alte (eozäne) Blätter einer Roridulaceae in einer Probe des russischen Bernsteintagebaus bei Jantarny beschrieben. Sie stellen den ersten dokumentierten fossilen Nachweis von Fallen einer fleischfressenden Pflanze dar. Der Fund bestätigte zum einen die zuvor bereits durch molekulare Untersuchungen aufgestellte Annahme, dass sich die Familie der Roridulaceae vor rund 38 Millionen Jahren von den Actinidiaceae trennte. Darüber hinaus allerdings wies der Fund in Nordeuropa auch nach, dass die Familie im Eozän eine weit größere Verbreitung hatte als heute, was die bisherigen Theorien vom paläoendemitischen Ursprung der Familie in Gondwana unwahrscheinlich erscheinen lässt. Auch im Hinblick auf die Verbreitungsgebiete der verwandten Familien Actinidiaceae (tropisches Asien und Amerika) und Sarraceniaceae (Nord- und Südamerika) gilt im Licht des Fundes ein großes Verbreitungsgebiet der Familie als wahrscheinlich. Wohl erst durch Aussterbevorgänge nach dem Eozän wurde es dann kleiner, die heutigen Arten in ihren Verbreitungsgebieten wären dann Relikte dieses Prozesses.[16]
Verwendung
Die Wanzenpflanzen sind für den Menschen als Nutzpflanze ohne Bedeutung. Marloth berichtet allerdings davon, dass abgeschnittene Äste der Pflanzen in Häusern als Fliegenfänger aufgehängt wurden.[17]
Literatur
- John G. Conran: Roridulaceae. In: Klaus Kubitzki (Hrsg.): The Families and Genera of Vascular Plants. Band 6: Flowering plants – Dicotyledons, Celastrales, Oxalidales, Rosales, Cornales, Ericales. Springer, Berlin u. a. 2004, ISBN 3-540-06512-1, S. 339–343.
- Wilhelm Barthlott, Stefan Porembski, Rüdiger Seine, Inge Theisen: Karnivoren. Biologie und Kultur fleischfressender Pflanzen. Ulmer, Stuttgart 2004, ISBN 3-8001-4144-2, S. 163–165.
Einzelnachweise
Die Informationen dieses Artikels entstammen zum größten Teil den unter Nachweise angegebenen Quellen, darüber hinaus werden folgende Quellen zitiert:
- Jeremy J. Midgley, William D. Stock: Natural Abundance of δ ¹⁵N Confirms Insectivorous Habit of Roridula gorgonias, Despite it Having No Proteolytic Enzymes. In: Annals of Botany. Bd. 82, Nr. 3, 1998, ISSN 0305-7364, S. 387–388, JSTOR 42765801.
- Sherwin Carlquist: Wood Anatomy of Roridulaceae: Ecological and Phylogenetic Implications. In: American Journal of Botany. Bd. 63, Nr. 7, 1976, ISSN 0002-9122, S. 1003–1008, JSTOR 2441759.
- Fauna and Flora of Hermanus. Website des Fernkloof Nature Reserve, (Online (Memento vom 22. April 2008 im Internet Archive)).
- Alan G. Ellis, Jeremy J. Midgley: A new plant-animal mutualism involving a plant with sticky leaves and a resident hemipteran insect. In: Oecologia. Bd. 106, Nr. 4, 1996, S. 478–481, JSTOR 4221288.
- Bruce Anderson, Jeremy J. Midgley: Density-dependent outcomes in a digestive mutualism between carnivorous Roridula plants and their associated hemipterans. In: Oecologia. Bd. 152, Nr. 1, 2007, S. 115–120, JSTOR 40210657.
- Paul Simons: When a carnivore is not a carnivore. In: New Scientist. 2045, 31. August 1996, S. 16, (Online).
- William R. Dolling, J. M. Palmer: Pameridea (Hemiptera: Miridae): predaceous bugs specific to the highly viscid plant genus Roridula. In: Systematic Entomology. Bd. 16, Nr. 3, 1991, ISSN 0307-6970, S. 319–328, doi:10.1111/j.1365-3113.1991.tb00692.x.
- Dagmar Voigt, Stanislav Gorb: An insect trap as habitat: cohesion-failure mechanism prevents adhesion of Pameridea roridulae bugs to the sticky surface of the plant Roridula gorgonias. In: Journal of Experimental Biology. Bd. 211, Nr. 16, 2008, S. 2647–2657, doi:10.1242/jeb.019273.
- Bruce Anderson: Adaptations to Foliar Absorption of Faeces: a Pathway in Plant Carnivory. In: Annals of Botany. Bd. 95, Nr. 5, 2005, S. 757–761, JSTOR 42796161.
- Bruce Anderson, Jeremy J. Midgley: It takes two to tango but three is a tangle: mutualists and cheaters on the carnivorous plant Roridula. In: Oecologia. Bd. 132, Nr. 3, 2002, S. 369–373, JSTOR 4223351.
- Charles Darwin: Insectenfressende Pflanzen (= Ch. Darwin's gesammelte Werke. Bd. 8). E. Schweizerbart'sche Verlagshandlung (E. Koch), Stuttgart 1876, S. 309–310.
- Bartosz J. Płachno, Lubomír Adamec, Irene K. Lichtscheidl, Marianne Peroutka, Wolfram Adlassnig, Jaroslav Vrba: Fluorescence Labelling of Phosphatase Activity in Digestive Glands of Carnivorous Plants. In: Plant Biology. Bd. 8, Nr. 6, 2006, ISSN 1438-8677, S. 813–820, doi:10.1055/s-2006-924177.
- Bruce Anderson, Jeremy J. Midgley, Barbara A. Stewart: Facilitated selfing offers reproductive assurance: a mutualism between a hemipteran and carnivorous plant. In: American Journal of Botany. Bd. 90, Nr. 7, 2003, S. 1009–1015, JSTOR 4124120.
- Carnivorous Plant Database. Abgerufen am 7. September 2018.
- Randall J. Bayer, Larry Hufford, Douglas E. Soltis: Phylogenetic Relationships in Sarraceniaceae Based on rbcL and ITS Sequences. In: Systematic Botany. Bd. 21, Nr. 2, 1996, ISSN 0363-6445, S. 121–134, JSTOR 2419743.
- Eva-Maria Sadowski, Leyla J. Seyfullah, Friederike Sadowski, Andreas Fleischmann, Hermann Behling, Alexander R. Schmidt: Carnivorous leaves from Baltic amber. In: Proceedings of the National Academy of Sciences. Bd. 112, Nr. 1, 2015, S. 190–195, doi:10.1073/pnas.1414777111.
- Rudolf Marloth: Some recent Observations on the Biology of Roridula. In: Annals of Botany. Bd. 17, Nr. 65, 1903, S. 151–157, JSTOR 43235665.