Tebuconazol
Tebuconazol ist ein Gemisch von zwei enantiomeren chemischen Verbindungen aus der Gruppe der Triazole.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| 1:1-Gemisch (Racemat) aus (R)-Form (oben) und (S)-Form (unten) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tebuconazol | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C16H22ClN3O | ||||||||||||||||||
| Kurzbeschreibung |
farb- und geruchloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 307,82 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
1,25 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
165 °C (Zersetzung)[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
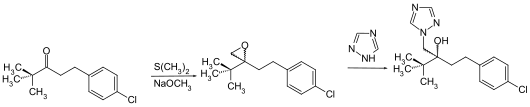
Tebuconazol kann durch Ringöffnung von 2-tert-Butyl-2-(4-chlorphenethyl)-oxiran mit 1,2,4-Triazol in Gegenwart einer Base gewonnen werden.[6][7]
Stereochemie
Da Tebuconazol ein Stereozentrum enthält gibt es zwei Enantiomere dieses Wirkstoffs. Das technische Tebuconazol wird als 1:1-Gemisch (Racemat) der (R)- und der (S)-Form eingesetzt.
Eigenschaften
Tebuconazol ist ein brennbarer, farb- und geruchloser Feststoff, der praktisch unlöslich in Wasser ist.[1] Es ist stabil gegenüber Hydrolyse bei pH-Werten von 5, 7 und 9.[2] Die oxidative Zersetzung unter Luft startet beim Erhitzen bei Temperaturen oberhalb von 200 °C. Hauptprodukte der Zersetzung sind 1-Chlor-4-ethenylbenzol, 4-Chlorbenzaldehyd und 1-(4-Chlorphenyl)ethanon.[8]
Verwendung
Tebuconazol wird als Fungizid verwendet.[1] Die Wirkung beruht auf einem Eingreifen des Stoffes in den Metabolismus der Pilzzellen.[2] Die Verbindung wurde 1988 auf den Markt gebracht.[9]
Tebuconazol wird auch Holzschutzmitteln als fungizider Wirkstoff zugesetzt.[2]
Zulassung
In der Europäischen Union dürfen seit September 2009 Pflanzenschutzmittel mit Tebuconazol für Anwendungen als Fungizid zugelassen werden.[10]
In vielen Staaten der EU, unter anderem in Deutschland und Österreich, sowie in der Schweiz sind Pflanzenschutzmittel (z. B. Folicur) mit diesem Wirkstoff zugelassen.[11]
Einzelnachweise
- Eintrag zu Tebuconazol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- BAUA:[https://de.wikipedia.org/w/index.php?title=Wikipedia:Defekte_Weblinks&dwl=http://circa.europa.eu/Public/irc/env/bio_reports/library?l=/assessement_directive/tebuconazolepdf/_EN_1.0_&a=d Seite nicht mehr abrufbar], Suche in Webarchiven: [http://timetravel.mementoweb.org/list/2010/http://circa.europa.eu/Public/irc/env/bio_reports/library?l=/assessement_directive/tebuconazolepdf/_EN_1.0_&a=d Directive 98/8/EC concerning the placing of biocidal products on the market – Tebuconazol], 29. November 2007.
- Müller, F.; Ackermann, P.; Margot, P.: Fungicides, Agricultural, 2. Individual Fungicides in Ullmanns Enzyklopädie der Technischen Chemie, 2012 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, doi:10.1002/14356007.o12_o06.
- Eintrag zu Tebuconazole (ISO); 1-(4-Chlorphenyl)-4,4-dimethyl-3-(1,2,4-triazol-1-ylmethyl)pentan-3-ol im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 24. Januar 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Datenblatt Tebuconazole bei Sigma-Aldrich, abgerufen am 10. November 2021 (PDF).
- Eintrag zu Tebuconazole in der Hazardous Substances Data Bank, abgerufen am 8. April 2013 (online auf PubChem).
- Thomas A. Unger: Pesticide synthesis handbook. 1996, ISBN 978-0-8155-1401-5, S. 720 (eingeschränkte Vorschau in der Google-Buchsuche).
- Monika Borucka, Maciej Celiński: Thermal Degradation and Combustion Behavior of Antifungal Pesticides: Triadimenol and Tebuconazole in Chem. Eng. Trans. 77 (2019) 139–144, doi:10.3303/CET1977024, Open Access.
- Horst Börner, Klaus Schlüter: Pflanzenkrankheiten und Pflanzenschutz. Springer, 2009, ISBN 3-540-49068-X, S. 496 (eingeschränkte Vorschau in der Google-Buchsuche).
- Richtlinie 2008/125/EG der Kommission vom 19. Dezember 2008 zur Änderung der Richtlinie 91/414/EWG des Rates zwecks Aufnahme von Aluminiumphosphid, Calciumphosphid, Magnesiumphosphid, Cymoxanil, Dodemorph, 2,5-Dichlorbenzoesäuremethylester, Metamitron, Sulcotrion, Tebuconazol und Triadimenol als Wirkstoffe (PDF).
- Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Tebuconazole in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs und Deutschlands, abgerufen am 23. Februar 2016.


