Sesquiterpenlactone
Sesquiterpenlactone sind natürlich vorkommende Terpenderivate, genauer gesagt Sesquiterpenderivate, die eine Lacton-Funktion aufweisen, an der sie häufig eine exocyclische Methylengruppe besitzen.[1] Es sind fast 5000 Vertreter dieser Stoffgruppe bekannt, die sich als Sekundärmetaboliten in vielen Pflanzen, vor allem in Vertretern der Familie der Korbblütler (Asteraceae), finden lassen. Sie können unter anderem als taxonomisches Merkmal für Asteraceae verwendet werden.[2] Sesquiterpenlactone spielen eine wichtige Rolle in der Abwehr von Fraßfeinden der Pflanzen, sie wirken hormonartig und sind als bioaktive Substanzen von medizinischem Interesse.
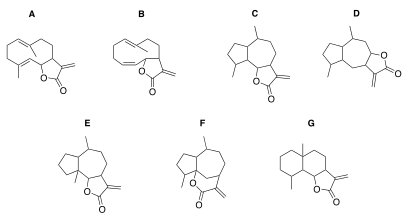
A: Germacranolide, B: Heliangolide, C+D: Guaianolide,
E: Pseudoguaianolide, F: Hypocretenolide, G: Eudesmanolide
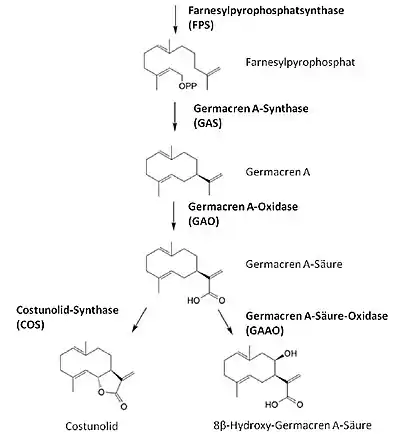
Aufbau und Biosynthese
Der grundlegende Aufbau von Terpenen besteht aus Isopren-Einheiten. Das sind C5-Körper (5 Kohlenstoff Atome) deren Anzahl und Anordnung je nach Terpentyp variiert.[3] Sesquiterpene bestehen aus drei Isopren-Einheiten und besitzen demnach ein C15-Gundgerüst. Man nimmt an, dass der Biosyntheseweg über den cytosolischen Mevalonatweg verläuft und Farnesylpyrophosphat eine Sesquiterpen-Vorstufe darstellt.[4] Dabei werden zunächst drei Acetyl-CoA-Moleküle in mehreren Schritten zu Mevalonsäure zusammengefügt. Durch Pyrophosphorylierung, Decarboxylierung und Dehydration entsteht Isopentenylpyrophosphat. Ausgehend von Isopentenylpyrophosphat und seinem Isomer Dimethylallylpyrophosphat wird dann in mehreren Schritten Farnesylpyrophosphat synthetisiert.[5] Die Biosynthese des einfachsten Sesquiterpenlactons Costunolid erfordert weitere enzymatisch katalysierte Schritte. Zunächst katalysiert das Enzym Germacren A-Synthase (GAS) die Bildung von Germacren A aus Farnesylpyrophosphat.[6] Dann folgt eine dreistufige Oxidation, katalysiert von der Germacren A-Oxidase (GAO), wodurch Germacren A-Säure entsteht. Als Zwischenprodukt entsteht dabei zunächst Germacren A-Alkohol, der dann über das Germacren A-Aldehyd zu Germacren A-Säure oxidiert wird.[7] Die Germacren A-Säure-Oxidase (GAAO) katalysierte daraufhin die Hydroxylierung am C8-Atom der Germacren A-Säure, sodass als Produkt 8β-Hydroxy-Germacren A-Säure gebildet wird.[8] Mithilfe der Costunolid-Synthase (COS) kann aus der Germacren A-Säure 6α-Hydroxy-Germacren A-Säure synthetisiert werden. Die Hydroxylierung am C6-Atom der Germacren A-Säure kann dabei zur spontanen Ausbildung des für Sesquiterpenlactone charakteristischen γ-Lactonringes führen. Während es sich bei GAO, GAAO und COS um P450-Monooxygenasen handelt, gehört GAS zu den Terpensynthasen.[9] Costunolid dient als Grundgerüst für die Biosynthese weiterer Sesquiterpenlactone.[10]
Sesquiterpenlactone unterliegen einer Klassifizierung aufgrund der Anordnung ihres Kohlenstoffgrundgerüstes. So gibt es z. B. die Klasse der Xanthanolide, zu der unter anderem Tomentosin und 8-Epixanthatin gehören, die Klasse der Guaianolide, vertreten z. B. durch Dehydrocostuslacton, und die Klasse der Germacranolide mit Costunolid als Exempel. Weiterhin gibt es die Klassen der Heliangolide, Pseudoguaianolide, Hypocretenolide und Eudesmanolide.[11]
Funktionen
Die exocyclische Methylengruppe am γ-Lactonring der Sesquiterpenlactone führt durch ihre hohe elektrophile Reaktivität zu einer starken biologischen Aktivität der Verbindungen. Aufgrund dessen kommt es unter anderem zu Reaktionen mit Thiolgruppen, so z. B. der Thiolgruppe der Aminosäure Cystein, was einen Einfluss der Verbindungen auf Proteine ermöglicht.[12] Das Funktions- und Wirkungsspektrum der Sesquiterpenlactone ist sehr breit. Sie besitzen z. B. antimykotische, antibakterielle, zytotoxische, antitumorale, antiinflammatorische und allelopathische Eigenschaften. Auch für Säugetiere wie den Menschen können diese Substanzen toxisch sein, da sie zu Kontaktdermatitis führen können.[13] Für Pflanzen fungieren sie vor allem als Abwehrstoffe gegen Herbivore und Mikroorganismen. Diese Funktion wird einerseits durch ihren bitteren Geschmack und andererseits durch die Zytotoxizität, z. B. durch Eingriffe in den Stoffwechsel der Pathogene, erfüllt. Zur Abwehrzwecken werden sie in spezialisierten Zellen, den köpfchentragenden Drüsenhaaren, auf den Oberflächen der Pflanzen gebildet und in Kutikularblasen sezerniert.[14] Sesquiterpenlactone wurden nicht nur in Asteraceae, sondern auch in anderen Pflanzenfamilien entdeckt. So z. B. in Apiaceae[15], Cupressaceae[16], Magnoliaceae[17] und sogar in Pilzen[18].
Sesquiterpenlactone als Pflanzenhormone
Neben der Verteidigung der Pflanzen gegen Pathogene und Herbivore haben Sesquiterpenlactone offensichtlich auch hormonelle Wirkungen. Die vier Sesquiterpenlactone Tomentosin, 8-Epixanthatin, Dehydrocostuslacton und Costunolid wurden innerhalb der Pflanzengewebe nachgewiesen. Sie kommen nicht in den Trichomen auf der Pflanzenoberfläche vor und sind um ein Vielfaches geringer konzentriert als die in den Trichomen lokalisierten Verbindungen.[19] Innerhalb der Pflanzengewebe wird eine physiologische Funktion der Sesquiterpenlactone als Inhibitoren des Auxin-abhängigen Streckungswachstums angenommen.[20][21] Gestützt wird diese These durch Versuche, bei denen gezeigt wurde, dass während einer einseitigen Belichtung von Sonnenblumen Hypokotylen keine differenzierte Verteilung von Auxin stattfindet.[22] Daraus wurde geschlossen, dass Auxininhibitoren auf der belichteten Seite für die Krümmungsreaktion der Pflanzen verantwortlich sein müssten.[23][24] Zudem wurde eine abwärts gerichtete Diffusionsrichtung der Verbindungen nachgewiesen.[25] Daher kann nicht ausgeschlossen werden, dass Sesquiterpenlactone, aufgrund ihrer Eigenschaft an Thiolgruppen binden zu können, mit Proteinen der AUXIN RESISTANT1- und/oder der PIN-Familie interagieren können, und so den polaren Auxin-Transport beeinflussen könnten, der treibende Kraft hinter Phototropismus und Gravitropismus ist. Die Hemmung des abwärts gerichteten Auxintransports wurde experimentell durch Applikation von Dehydrocostuslacton an Hypokotylen von Raphanus gezeigt.[26] Die erwähnten Proteine sind wesentlich am polaren Auxin Transport der Zellen beteiligt und spielen damit auch eine große Rolle im lichtinduzierten Auxin-abhängigen Streckungswachstum.[27] Bei Versuchen wurden zudem erstmals Thiolgruppen-Addukte der Sesquiterpenlactone in den Pflanzengeweben nachgewiesen und daraufhin ein bisher ungeklärter Inaktivierungsmechanismus für die mutmaßlichen Auxininhibitoren postuliert. Die Bindung von Thiolgruppen könnte demnach auch Teil der Negativ-Regulation der Verbindungen sein. Sesquiterpenlactone werden in sehr geringen Konzentrationen auch in die Rhizosphäre exsudiert, was die Annahme des abwärts gerichteten Transports stützt. Zudem konnte nachgewiesen werden, dass geringste Konzentrationen (im nano- milimolaren Bereich) von Dehydrocostuslacton im Boden in der Lage sind, die Keimung der parasitischen Sommerwurz Samen (Orobanche cumana) zu stimulieren.[28] Wenige Jahre später wurden auch Tomentosin, Costunolid und 8-Epixanthatin in Wurzelexsudaten als Keimungsstimulatoren für die Samen von Orobanche cumana identifiziert.[29]
Möglicher Nutzen im Agrarsektor
Ein möglicher kommerzieller Einsatz von Sesquiterpenlactonen im Agrarsektor wird diskutiert. Dort könnten sie zum Schutz von Nutzpflanzen vor den parasitischen Sommerwurzen (Orobanche, Striga und Phelipanche Arten) dienen. Betroffen von diesen parasitischen Blütenpflanzen sind in erster Linie Sonnenblumen, Tomaten, Linsen, Raps, Ackerbohnen und Melonen bei denen ein Befall zu großen Ernteausfällen führen kann. Die Sommerwurzen produzieren winzige Samen (200–400 µm) die jahrelang im Boden überdauern können. Das Auskeimen dieser Samen wird durch chemische Signalstoffe der Wirtspflanzen induziert. Diese chemischen Signalstoffe sind beispielsweise Strigolactone oder Sesquiterpenlactone. Nach der Keimung des Samens muss die Keimwurzel binnen kurzer Zeit eine geeignete Wirtswurzel finden, um dort ein Haustorium zu etablieren und die Parasitose zu beginnen. Man könnte der Theorie nach einen brachliegenden, befallenen Bereich mit einer definierten Konzentration von bestimmten Sesquiterpenlactonen behandeln um die Keimung der im Boden ruhenden Sommerwurz-Samen zu induzieren. Wenn die Keimwurzel nicht binnen kurzer Zeit eine geeignete Wirtspflanzen-Wurzel erreicht, stirbt der Keimling ab.[30][31]
Medizinischer Nutzen

Einige Vertreter der Sesquiterpenlactone sind von pharmakologischem Interesse, da ihnen antitumorale, migräne- und entzündungshemmende sowie antimikrobielle Eigenschaften zugeschrieben werden und sie toxisch für einige wichtige humanpathogene Erreger wie z. B. Trypanosomen sind.[32][33][34] Viele der Wirkungen dieser Substanzen macht man sich in der traditionellen Medizin bereits seit Jahrhunderten zu Nutze. So ist etwa die entzündungshemmende Wirkung der Arnica montana, die in Europa seit dem Mittelalter als Heilpflanze bekannt ist, auf Sesquiterpenlactone zurückzuführen. Ebenso die Wirkungen der Mikania micrantha, die in Mittel- und Südamerika beheimatet ist, und der Saussurea lappa, der in Asien vorkommt. Der entzündungshemmende Effekt der Sesquiterpenlactone ist auf eine Hemmung von Transkriptionsfaktoren wie z. B. NF-κB und AP-1 zurückzuführen.[35] NF-κB ist ein Schlüssel-Regulator der zellulären Entzündungs- und Immunantwort. Anhand des Sesquiterpenlactons Parthenolid konnte gezeigt werden, dass durch diese Verbindungen ein wichtiger Schritt in der Aktivierung des Transkriptionsfaktors gehemmt wird. Zusätzlich verhindert Pathenolid die Aktivierung der DNA-Bindung von NF-κB.[36]
Siehe auch
- Artemisinin
- Lactucopicrin
- Tomentosin
- 8-Epixanthatin
- Dehydrocostuslacton
- Costunolid
Einzelnachweise
- Nikolaus H. Fischer: Sesquiterpene Lactones: Biogenesis and Biomimetic Transformations. In: Biochemistry of the Mevalonic Acid Pathway to Terpenoids. Springer US, Boston, MA 1990, ISBN 978-1-4684-8791-6, S. 161–201, doi:10.1007/978-1-4684-8789-3_4.
- Thomas J. Schmidt: Toxic Activities of Sesquiterpene Lactones – Structural and Biochemical Aspects. In: Current Organic Chemistry 3, 1999, S. 577–605; Abstract.
- L. Ruzicka: The isoprene rule and the biogenesis of terpenic compounds. In: Experientia. Band 9, Nr. 10, Oktober 1953, ISSN 0014-4754, S. 357–367, doi:10.1007/bf02167631.
- Helga D. Fischer, N. H. Fischer, R. W. Franck, E. J. Olivier: Fortschritte der Chemie organischer Naturstoffe / Progress in the Chemistry of Organic Natural Products. In: Fortschritte der Chemie organischer Naturstoffe / Progress in the Chemistry of Organic Natural Products. 1979, ISSN 0071-7886, doi:10.1007/978-3-7091-8548-3.
- T. LAZAR: Taiz, L. and Zeiger, E. Plant physiology. 3rd edn. In: Annals of Botany. Band 91, Nr. 6, 1. Mai 2003, ISSN 0305-7364, S. 750–751, doi:10.1093/aob/mcg079, PMC 4242361 (freier Volltext) – (oup.com [abgerufen am 24. September 2018]).
- Jens C Göpfert, Gillian MacNevin, Dae-Kyun Ro, Otmar Spring: Identification, functional characterization and developmental regulation of sesquiterpene synthases from sunflower capitate glandular trichomes. In: BMC Plant Biology. Band 9, Nr. 1, 2009, ISSN 1471-2229, S. 86, doi:10.1186/1471-2229-9-86, PMID 19580670, PMC 2715020 (freier Volltext).
- Don Trinh Nguyen, Jens Christian Göpfert, Nobuhiro Ikezawa, Gillian MacNevin, Meena Kathiresan: Biochemical Conservation and Evolution of Germacrene A Oxidase in Asteraceae. In: Journal of Biological Chemistry. Band 285, Nr. 22, 28. Mai 2010, ISSN 0021-9258, S. 16588–16598, doi:10.1074/jbc.M110.111757, PMID 20351109, PMC 2878029 (freier Volltext).
- Nobuhiro Ikezawa, Jens Christian Göpfert, Don Trinh Nguyen, Soo-Un Kim, Paul E. O'Maille: Lettuce Costunolide Synthase (CYP71BL2) and Its Homolog (CYP71BL1) from Sunflower Catalyze Distinct Regio- and Stereoselective Hydroxylations in Sesquiterpene Lactone Metabolism. In: Journal of Biological Chemistry. Band 286, Nr. 24, 17. Juni 2011, ISSN 0021-9258, S. 21601–21611, doi:10.1074/jbc.M110.216804, PMID 21515683, PMC 3122218 (freier Volltext).
- Jan-Willem de Kraker, Maurice C. R. Franssen, Maaike Joerink, Aede de Groot, Harro J. Bouwmeester: Biosynthesis of Costunolide, Dihydrocostunolide, and Leucodin. Demonstration of Cytochrome P450-Catalyzed Formation of the Lactone Ring Present in Sesquiterpene Lactones of Chicory. In: Plant Physiology. Band 129, Nr. 1, 1. Mai 2002, ISSN 0032-0889, S. 257–268, doi:10.1104/pp.010957, PMID 12011356, PMC 155889 (freier Volltext).
- N. H. Fischer, E. J. Olivier, H. D. Fischer: The Biogenesis and Chemistry of Sesquiterpene Lactones. In: Fortschritte der Chemie organischer Naturstoffe / Progress in the Chemistry of Organic Natural Products. Springer Vienna, Vienna 1979, ISBN 978-3-7091-8550-6, S. 47–320, doi:10.1007/978-3-7091-8548-3_2.
- Frederick C. Seaman: Sesquiterpene lactones as taxonomic characters in the asteraceae. In: The Botanical Review. Band 48, Nr. 2, April 1982, ISSN 0006-8101, S. 121–594, doi:10.1007/bf02919190.
- Otmar Spring, Achim Hager: Inhibition of elongation growth by two sesquiterpene lactones isolated from Helianthus annuus L. In: Planta. Band 156, Nr. 5, Dezember 1982, ISSN 0032-0935, S. 433–440, doi:10.1007/bf00393314.
- Anna K. Picman: Biological activities of sesquiterpene lactones. In: Biochemical Systematics and Ecology. Band 14, Nr. 3, Mai 1986, ISSN 0305-1978, S. 255–281, doi:10.1016/0305-1978(86)90101-8.
- Otmar Spring, Uta Bienert, Volker Klemt: Sesquiterpene Lactones in Glandular Trichomes of Sunflower Leaves. In: Journal of Plant Physiology. Band 130, Nr. 4-5, Oktober 1987, ISSN 0176-1617, S. 433–439, doi:10.1016/s0176-1617(87)80208-0.
- Damian Paul Drew, Nadja Krichau, Kirsten Reichwald, Henrik Toft Simonsen: Guaianolides in apiaceae: perspectives on pharmacology and biosynthesis. In: Phytochemistry Reviews. Band 8, Nr. 3, 19. Mai 2009, ISSN 1568-7767, S. 581–599, doi:10.1007/s11101-009-9130-z.
- Anna K. Picman: Biological activities of sesquiterpene lactones. In: Biochemical Systematics and Ecology. Band 14, Nr. 3, Mai 1986, ISSN 0305-1978, S. 255–281, doi:10.1016/0305-1978(86)90101-8.
- Sung-Hee Park, Sang-Un Choi, Chong Ock Lee, Sung-eun Yoo, Seok Keun Yoon: Costunolide, a Sesquiterpene from the Stem Bark of Magnolia sieboldii, Inhibits the RAS-Farnesyl-Proteintransferase. In: Planta Medica. Band 67, Nr. 4, 2001, ISSN 0032-0943, S. 358–359, doi:10.1055/s-2001-14315.
- Pattama Pittayakhajonwut, Atit Usuwan, Chakapong Intaraudom, Sukitaya Veeranondha, Prasert Srikitikulchai: Sesquiterpene Lactone 12,8-Eudesmanolides from the FungusXylaria ianthinovelutina. In: Planta Medica. Band 75, Nr. 13, 18. Mai 2009, ISSN 0032-0943, S. 1431–1435, doi:10.1055/s-0029-1185698.
- Frank M. Raupp, Otmar Spring: New Sesquiterpene Lactones from Sunflower Root Exudate as Germination Stimulants for Orobanche cumana. In: Journal of Agricultural and Food Chemistry. Band 61, Nr. 44, 24. Oktober 2013, ISSN 0021-8561, S. 10481–10487, doi:10.1021/jf402392e.
- Otmar Spring, Achim Hager: Inhibition of elongation growth by two sesquiterpene lactones isolated from Helianthus annuus L. In: Planta. Band 156, Nr. 5, Dezember 1982, ISSN 0032-0935, S. 433–440, doi:10.1007/bf00393314.
- Kaori Yokotani-Tomita, Jun Kato, Seiji Kosemura, Shosuke Yamamura, Midori Kushima: Light-induced auxin-inhibiting substance from sunflower seedlings. In: Phytochemistry. Band 46, Nr. 3, Oktober 1997, ISSN 0031-9422, S. 503–506, doi:10.1016/s0031-9422(97)00307-5.
- J. BRUINSMA, C.M. KARSSEN, M. BENSCHOP, J.B. VAN DORT: Hormonal Regulation of Phototropism in the Light-grown Sunflower Seedling,Helianthus annuusL.: Immobility of Endogenous Indoleacetic Acid and Inhibition of Hypocotyl Growth by Illuminated Cotyledons. In: Journal of Experimental Botany. Band 26, Nr. 3, 1975, ISSN 0022-0957, S. 411–418, doi:10.1093/jxb/26.3.411.
- Martin Feyerabend, Elmar W. Weiler: Immunological estimation of growth regulator distribution in phototropically reacting sunflower seedlings. In: Physiologia Plantarum. Band 74, Nr. 1, September 1988, ISSN 0031-9317, S. 185–193, doi:10.1111/j.1399-3054.1988.tb04962.x.
- Johan Bruinsma, Koji Hasegawa: A new theory of phototropism - its regulation by a light-induced gradient of auxin-inhibiting substances. In: Physiologia Plantarum. Band 79, Nr. 4, August 1990, ISSN 0031-9317, S. 700–704, doi:10.1111/j.1399-3054.1990.tb00047.x.
- SHIBAOKA, HIROH: STUDIES ON THE MECHANISM OF GROWTH INHIBITING EFFECT OF LIGHT. In: Plant and Cell Physiology. Band 2, Nr. 2, Mai 1961, ISSN 1471-9053, doi:10.1093/oxfordjournals.pcp.a077675 (oup.com [abgerufen am 21. September 2018]).
- Junichi Ueda, Yuta Toda, Kiyotaka Kato, Yuichi Kuroda, Tsukasa Arai: Identification of dehydrocostus lactone and 4-hydroxy-β-thujone as auxin polar transport inhibitors. In: Acta Physiologiae Plantarum. Band 35, Nr. 7, 29. März 2013, ISSN 0137-5881, S. 2251–2258, doi:10.1007/s11738-013-1261-6.
- Jürgen Kleine-Vehn, Pankaj Dhonukshe, Ranjan Swarup, Malcolm Bennett, Jiří Friml: Subcellular Trafficking of the Arabidopsis Auxin Influx Carrier AUX1 Uses a Novel Pathway Distinct from PIN1. In: The Plant Cell. Band 18, Nr. 11, 1. November 2006, ISSN 1040-4651, S. 3171–3181, doi:10.1105/tpc.106.042770, PMID 17114355, PMC 1693951 (freier Volltext).
- Daniel M. Joel, Swapan K. Chaudhuri, Dina Plakhine, Hammam Ziadna, John C. Steffens: Dehydrocostus lactone is exuded from sunflower roots and stimulates germination of the root parasite Orobanche cumana. In: Phytochemistry. Band 72, Nr. 7, Mai 2011, ISSN 0031-9422, S. 624–634, doi:10.1016/j.phytochem.2011.01.037.
- Frank M. Raupp, Otmar Spring: New Sesquiterpene Lactones from Sunflower Root Exudate as Germination Stimulants for Orobanche cumana. In: Journal of Agricultural and Food Chemistry. Band 61, Nr. 44, 24. Oktober 2013, ISSN 0021-8561, S. 10481–10487, doi:10.1021/jf402392e.
- Daniel M. Joel, Swapan K. Chaudhuri, Dina Plakhine, Hammam Ziadna, John C. Steffens: Dehydrocostus lactone is exuded from sunflower roots and stimulates germination of the root parasite Orobanche cumana. In: Phytochemistry. Band 72, Nr. 7, Mai 2011, ISSN 0031-9422, S. 624–634, doi:10.1016/j.phytochem.2011.01.037.
- Frank M. Raupp, Otmar Spring: New Sesquiterpene Lactones from Sunflower Root Exudate as Germination Stimulants for Orobanche cumana. In: Journal of Agricultural and Food Chemistry. Band 61, Nr. 44, 24. Oktober 2013, ISSN 0021-8561, S. 10481–10487, doi:10.1021/jf402392e.
- S. P. Hehner, T. G. Hofmann, W. Dröge, M. L. Schmitz: The antiinflammatory sesquiterpene lactone parthenolide inhibits NF-kappa B by targeting the I kappa B kinase complex. In: Journal of Immunology (Baltimore, Md.: 1950). Band 163, Nr. 10, 15. November 1999, ISSN 0022-1767, S. 5617–5623, PMID 10553091.
- Anna K. Picman: Biological activities of sesquiterpene lactones. In: Biochemical Systematics and Ecology. Band 14, Nr. 3, Mai 1986, ISSN 0305-1978, S. 255–281, doi:10.1016/0305-1978(86)90101-8.
- Thomas J. Schmidt, Fernando B. Da Costa, Norberto P. Lopes, Marcel Kaiser, Reto Brun: In Silico Prediction and Experimental Evaluation of Furanoheliangolide Sesquiterpene Lactones as Potent Agents against Trypanosoma brucei rhodesiense. In: Antimicrobial Agents and Chemotherapy. Band 58, Nr. 1, 1. Januar 2014, ISSN 0066-4804, S. 325–332, doi:10.1128/AAC.01263-13, PMID 24165182, PMC 3910805 (freier Volltext).
- Steffen Wagner: Sesquiterpenlactone: Neuronale Netze als QSAR-Modell sowie pharmakokinetische Untersuchungen am Beispiel von Arnica montana. Dissertation, 2006. PDF; 6,03 MB.
- S. P. Hehner, T. G. Hofmann, W. Dröge, M. L. Schmitz: The Antiinflammatory Sesquiterpene Lactone Parthenolide Inhibits NF-kappa B by Targeting the I kappa B Kinase Complex. In: Journal of Immunology (Baltimore, Md.: 1950). Band 163, Nr. 10, 15. November 1999, ISSN 0022-1767, S. 5617–5623.