Prisman
Prisman oder Ladenburg-Benzol, Summenformel C6H6, ist ein anderer Name für die Verbindung Tetracyclo[2.2.0.02,6.03,5]hexan. Den Namen hat die Verbindung durch ihre Prisma-Struktur.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
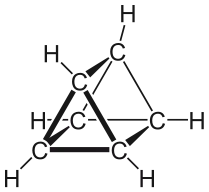 | ||||||||||
| Allgemeines | ||||||||||
| Name | Prisman | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C6H6 | |||||||||
| Kurzbeschreibung |
farblose, hochexplosive Flüssigkeit[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 78,11 g·mol−1 | |||||||||
| Aggregatzustand |
flüssig | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Die Struktur wurde ursprünglich von Albert Ladenburg für das Benzol-Molekül vorgeschlagen, stellte sich jedoch als falsch heraus. Der Kohlenwasserstoff Prisman, der der damals vorgeschlagenen Struktur entspricht, wurde 1973 zum ersten Mal synthetisch hergestellt.
Prisman steht unter starker Ringspannung und ist um 377 kJ/mol energiereicher als Benzol. Dessen ungeachtet ist Prisman sogar bei Raumtemperatur metastabil. Robert B. Woodward und Roald Hoffmann entdeckten, was der Umlagerung von Prisman zu Benzol entgegensteht: die Erhaltung der Orbitalsymmetrie (Woodward-Hoffmann-Regeln). Hoffmann erhielt zusammen mit Fukui Ken’ichi für diese Theorie 1981 den Chemie-Nobelpreis. Zu diesem Zeitpunkt war Woodward (Nobelpreis 1965) bereits verstorben. Woodward und Hoffmann bezeichneten Prisman als einen „wütenden Tiger, dem es unmöglich ist, aus seinem Papierkäfig auszubrechen.“
Prisman ist eine farblose, leicht flüchtige und explosive Flüssigkeit.[1]
Synthese
Prisman als Valenzisomeres von Benzol kann über photochemische Umwandlungen aus Benzol hergestellt werden:[3]
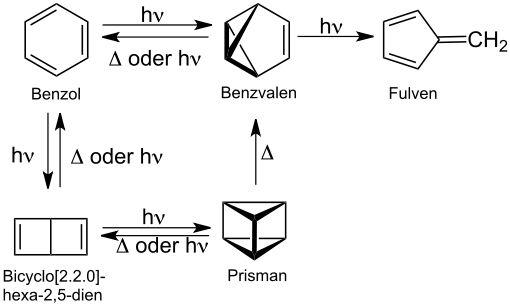
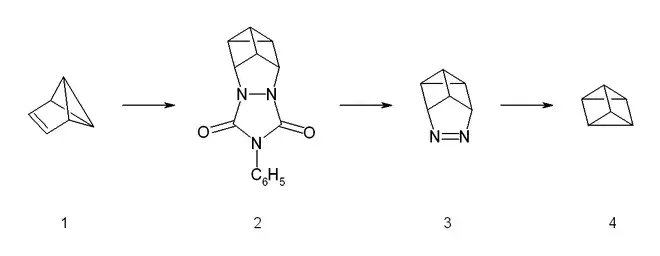
Eine alternative Synthese von Prisman geht ebenfalls von Benzvalen (1) aus.[1] Dazu wird Benzvalen mit der Verbindung 4-Phenyl-1,2,4-triazolin-3,5-dion (PTAD) umgesetzt, welche das bisher reaktivste bekannteste Dienophil darstellt. Die Reaktion ist eine schrittweise Diels-Alder-artige Umsetzung, mit einem Carbeniumion als reaktiver Zwischenstufe. Das Addukt 2 wird im basischen Medium hydrolysiert und dann mit Kupfer(II)-chlorid umgesetzt. Die Neutralisation mit einer starken Base liefert die kristalline Azoverbindung 3 in 65 % Ausbeute. Die Photolyse von 3 ergibt unter Stickstoffabspaltung ein Diradikal, das dann zu Prisman (4) cyclisiert.
Einzelnachweise
- Eintrag zu Prisman. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. September 2014.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 266–267, ISBN 3-342-00280-8.