Molekulare Maschine
Eine molekulare Maschine oder Nanomaschine ist ein aus Makromolekülen zusammengesetztes Gebilde, das bestimmte Funktionen ausführen kann. Dabei handelt es sich um eine Klasse von supramolekularen Verbindungen, die mechanische Bewegungen ausführen können. Dabei kopiert man – wie in der Bionik – in Tier- oder Pflanzenzellen vorkommende Systeme und versucht, sie synthetisch zu konstruieren. Andererseits versucht man, die Grundprinzipien der klassischen Mechanik auf Maschinen im molekularen Bereich anzuwenden. Molekulare Maschinen sind dem Forschungsgebiet Nanotechnologie zuzuordnen, wo eine Reihe von komplexen molekularen Maschinen vorgeschlagen wurde. Da bewiesen ist, dass ein Perpetuum mobile nach den Grundgesetzen der Physik unmöglich ist, muss man auch einer molekularen Maschine, genauso wie einer klassischen Maschine, von außen Energie zuführen.
Molekulare Systeme, die in der Lage sind, einen chemischen oder mechanischen Prozess ins Gleichgewicht zu verschieben, stellen einen potenziell wichtigen Zweig der Chemie und der Nanotechnologie dar. Für diesen Prozess ist ein vorher von außen erzeugter Gradient (z. B. Konzentrationsgefälle, Temperaturdifferenz, Potentialdifferenz o. ä.) erforderlich, damit die Maschine in der Lage ist, nützliche Arbeit durchzuführen. Da ein System immer ein Gleichgewicht anstrebt, werden Substanzen in Zellen immer in Richtung eines Konzentrationsgefälles wandern, oder Moleküle unterschiedlicher Temperatur werden sich so vermischen, dass es zum Temperaturausgleich kommt.
Der Nobelpreis für Chemie wurde 2016 an Jean-Pierre Sauvage, Sir J. Fraser Stoddart and Bernard L. Feringa für das Design und die Synthese molekularer Maschinen verliehen.
Geschichtlicher Hintergrund
Es gibt zwei Gedankenexperimente zum historischen Hintergrund molekularer Maschinen: Maxwells Dämon und Feynmans "Ratsche" (oder molekulare Ratsche): Maxwells Dämon ist woanders beschrieben, und eine unterschiedliche Interpretation von Feynmans Gesetz findet sich im Folgenden:
Man stelle sich ein sehr kleines System (siehe Bild unten) von zwei Schaufel- bzw. Zahnrädern vor, durch eine starre Achse verbunden, und dass es möglich ist, diese beiden Räder bei zwei verschiedenen Temperaturen zu halten. Das Zahnrad bei Temperatur 2 (T2) wird durch eine Sperrklinke daran gehindert, gegen den Uhrzeigersinn zu rotieren, was für eine gleichgerichtete Bewegung des Systems sorgt. Daher kann sich die Achse nur in einer Drehung im Uhrzeigersinn bewegen, und dabei könnte die Maschine ein Gewicht (m) nach oben heben. Wenn das Schaufelrad im Kasten mit der Temperatur 1 (T1) in einer viel heißeren Umgebung wäre als das Zahnrad im Kasten T2, würde man erwarten, dass die kinetische Energie, mit der die Gasmoleküle (rote Kreise) die Schaufeln treffen, bei T1 viel höher wäre, als die Energie der Gasmoleküle, die bei T2 gegen die Zähne des Zahnrad treffen werden. Daher gäbe es bei der Temperatur T2, also bei geringerer kinetischer Energie der gasförmigen Teilchen, eine sehr viel geringere Wahrscheinlichkeit, dass die Moleküle mit dem Zahnrad in der statistisch entgegengesetzten Richtung zusammenstoßen. Ferner würde die Klinke es mit einer gerichteten Bewegung ermöglichen, langsam über einen gewissen Zeitraum die Achse zu drehen und das Gewicht (m) hochzuheben.
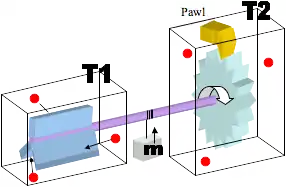
Wie beschrieben, kann das System wie ein Perpetuum mobile scheinen; jedoch ist der Hauptbestandteil des Systems das Wärmegefälle innerhalb des Systems. Der zweite Hauptsatz der Thermodynamik gilt auch hier, denn das Temperaturgefälle muss durch einige äußere Bedingungen erzeugt werden. Die Brownsche Molekularbewegung der gasförmigen Teilchen liefert die Energieversorgung der Maschine, und das Temperaturgefälle bewirkt, dass das Gerät das System mit einer Kreisbewegung aus dem Gleichgewicht bringt. In Feynmans Ratsche wird der zufälligen Brownschen Bewegung nicht entgegengewirkt, sondern diese wird nutzbar gemacht und gelenkt. Es kommt darauf an, ob der Temperaturgradient auch im molekularen Maßstab beibehalten werden kann, oder ob eine Umverteilung der Energie durch molekulare Schwingungen innerhalb des Moleküls erfolgt. Darüber hinaus ist anzumerken, dass Feynmans Maschine wertvolle Arbeit bei dem Hochheben einer Masse leistet, um unter Nutzung der Brownschen Molekularbewegung einer molekularen Maschine Energie zu liefern. Diese Energie (potentielle Energie des aufgehobenen Gewichtes (m)) kann eventuell verwendet werden, um nanoskalige Aufgaben auszuführen.
Funktion molekularer Maschinen
Aus synthetischer Sicht gibt es zwei wichtige Arten von molekularen Maschinen: molekulare Schalter (oder Pendel) und molekulare Motoren. Der Hauptunterschied zwischen den beiden Systemen besteht darin, dass ein Schalter auf ein System als eine Funktion des Zustandes wirkt, wohingegen ein Motor ein System als Funktion der Bewegung beeinflusst. Einen Schalter (oder ein Pendel) bedient man durch eine Translationsbewegung, aber die Rückkehr des Schalters in seine ursprüngliche Position zeigt eine mechanische Wirkung und setzt Energie frei, die dem System zugeführt wird. Darüber hinaus können Schalter nicht verwendet werden, um unter Energiezufuhr ein chemisches System wiederholt aus dem Gleichgewicht zu bringen, was ein Motor wiederum kann.
Synthese und Typen molekularer Maschinen
Eine Vielfalt einfacher molekularer Maschinen wurde von Chemikern synthetisiert. Sie können nicht aus einem einzelnen Molekül bestehen, sind aber konstruiert für mechanische molekulare Architekturen, wie Rotaxane und Catenane. Kohlenstoff-Nanomotoren wurden auch schon hergestellt.[1]
- Ein synthetischer molekularer Motor ist ein Molekül, das in der Lage ist, eine gerichtete Drehbewegung auszuführen, angetrieben durch Fremdenergie. Eine Reihe von molekularen Maschinen wurden synthetisiert, angetrieben durch Licht oder eine Reaktion mit anderen Molekülen. Ein Beispiel ist ein molekularer Bohrer, der – angetrieben durch UV-Licht – Zellwände soweit perforiert, dass kleine Moleküle – insbesondere Wasser (H2O) – austreten können. Das UV-Licht kann punktuell eingesetzt werden, um gewünschtes Gewebe zu behandeln.[2][3]
- Molekularer Propeller ist ein Molekül, das bei einer Drehbewegung Flüssigkeiten antreiben kann, aufgrund seiner speziellen Form, die in Analogie zum makroskopischen Propeller ausgebildet ist. Er hat mehrere Flügel, die im molekularen Maßstab in einem bestimmten Neigungswinkel um den Stiel einer nanoskaligen Welle befestigt sind.
- Molekularer Schalter ist ein Molekül, das reversibel zwischen zwei oder mehreren stabilen Zuständen geschaltet werden kann. Die Moleküle reagieren auf Änderungen von pH-Wert, Licht, Temperatur, elektrischem Strom, Mikroumgebung oder die Gegenwart eines Liganden und werden dadurch zwischen verschiedenen Zuständen verschoben.
- Ein molekulares Pendel (Shuttle) ist ein Molekül, das Moleküle oder Ionen von einem Ort zu einem anderen bewegt. Ein molekulares Pendel besteht aus einem Rotaxan, einem Makrozyklus, der sich zwischen zwei Standorten oder Stationen entlang einer Hantel-Stange bewegen kann.
- Molekulare Pinzetten sind Wirtsmoleküle, die in der Lage sind, Gegenstände zu umschließen. Der offene Hohlraum der Moleküls bindet (wie eine Pinzette) Elemente mit nicht-kovalenter Bindung, (einschließlich Wasserstoffbindung, Metallkoordination, hydrophoben Kräften, Van-der-Waals-Kräften, π-π-Wechselwirkungen und/oder elektrostatischen Effekten). Beispiele für molekulare Pinzetten sind beschrieben worden, die aus DNA aufgebaut sind und als DNA-Maschinen bezeichnet werden.
- Molekularer Sensor ist ein Molekül, das dazu dient, die Konzentrationsänderung einer zu analysierenden Substanz nachzuweisen. Molekulare Sensoren kombinieren, wie Detektoren, die molekulare Erkennung mit Signalaufzeichnung oder -weiterleitung, so dass die Anwesenheit einer bestimmten Substanz beobachtet werden kann.[4]
- Ein molekulares Logikgatter ist ein Molekül, das eine logische Operation bei einem oder mehreren logischen Eingaben (input) durchführt und eine einzige logische Ausgabe (output) erzeugt. Im Gegensatz zu einem molekularen Sensor gibt es bei dem Molekularlogikgatter nur dann eine Ausgabe, wenn eine bestimmte Kombination von Eingaben vorhanden ist.
Vorbilder aus der Biologie
Die komplexesten molekularen Maschinen sind die in den Zellen vorkommenden Proteine. Diese umfassen die Motorproteine wie Myosin, das verantwortlich ist für die Muskelkontraktion, Kinesin, das die Organellen in den Zellen mit Mikrotubuli vom Zellkern wegtransportiert, Dynein, das die Bewegung der Geißeln hervorruft und membranständige ATPasen wie die ATP-Synthase. Diese Proteine und ihre auf der Nanometerskala befindliche Dynamik sind komplexer als alle molekularen Maschinen, die je konstruiert wurden. Die wahrscheinlich bedeutendsten biologischen Maschinen sind die Ribosomen. In der Tat sind Mikrotubuli Nanomaschinen, die aus über 600 Proteinen in Molekülkomplexen bestehen.[5] Die ersten sinnvollen Anwendungen dieser biologischen Maschinen mag es in der Nanomedizin geben. Zum Beispiel[6] könnten sie verwendet werden, um Krebszellen zu erkennen und zu zerstören.[7][8] Molekulare Nanotechnologie ist ein Unterkapitel der Nanotechnologie, betrachtet man die gesamten Möglichkeiten der molekularen Mechanik, könnten biologische Maschinen eine Therapie auf molekularer oder atomarer Ebene betreffen. Nanomedizin könnte diese Nanoroboter verwenden, um Schäden oder Infektionen festzustellen und zu reparieren. Molekulare Nanotechnologie ist hoch theoretisch, um vorwegzunehmen, dass Erfindungen auf dem Gebiet der Nanotechnologie erfolgversprechend sind und ein zukunftsweisendes Forschungsgebiet. Der gegenwärtige Stand der Forschung der Nanotechnologie mit den vorgeschlagenen Elementen ist noch weit entfernt von Nanorobotern.[9][10]
Verwendung
Die Synthese komplexer molekularer Maschinen ist ein vielversprechendes Gebiet theoretischer Forschung. Eine Vielzahl von Molekülen, wie beispielsweise ein molekularer Propeller, wurde entworfen, wobei die Schwierigkeit darin liegt, diese Synthesepläne umzusetzen. Sie bilden die Basis eines großen Gebietes der Nanotechnologie.
Siehe auch
Literatur
- Ballardini R, Balzani V, Credi A, Gandolfi MT, Venturi M.: Artificial Molecular-Level Machines: Which Energy To Make Them Work?. In: Acc. Chem. Res.. 34, Nr. 6, 2001, S. 445–455. doi:10.1021/ar000170g.
- Peter Satir, Søren T. Christensen: Structure and function of mammalian cilia. In: Springer Berlin / Heidelberg (Hrsg.): Histochemistry and Cell Biology. 129, Nr. 6, 26. März 2008, S. 688. doi:10.1007/s00418-008-0416-9. PMID 18365235. PMC 2386530 (freier Volltext).
- V. Balzani, M. Venturi, A. Credi: Molecular Devices and Machines, A Journey into the Nanoworld, Wiley, VCH 2003, ISBN 3-527-30506-8
- David A. Leigh: Genesis of the Nanomachines: The 2016 Nobel Prize in Chemistry, Angew Chem Int Ed, 55, 14506–14508 (2016).
- B. Lewandowski, G. De Bo, J. W. Ward, M. Papmeyer, S. Kuschel, M. J. Aldegunde, P. M. E. Gramlich, D. Heckmann, S. M. Goldup, D. M. D’Souza, A. E. Fernandes and D. A. Leigh: Sequence-Specific Peptide Synthesis by an Artificial Small-Molecule Machine, Science, 339, 189–193 (2013).
Einzelnachweise
- A. M. Fennimore, T.D. Yuzvinsky, Wei-Qiang Han, M. S. Fuhrer, J. Cumings and A. Zettl: Rotational actuators based on carbon nanotubes. In: Nature. 424, Nr. 6947, 2003, S. 408–410. bibcode:2003Natur.424..408F. doi:10.1038/nature01823. PMID 12879064.
- Lars Fischer: Der kleinste Bohrer der Welt, auf Spektrum online vom 31. August 2017
- Victor García López, Fang Chen, Lizanne G. Nilewski, Guillaume Duret, Amir Aliyan, Anatoly B. Kolomeisky, Jacob T. Robinson, Gufeng Wang, Robert Pal, James M. Tour: Molecular machines open cell membranes, in: Nature 548, S. 567–572, vom 31. August 2017, doi: 10.1038/nature23657
- Cavalcanti A, Shirinzadeh B, Freitas Jr RA, Hogg T.: Nanorobot architecture for medical target identification. In: Nanotechnology. 19, Nr. 1, 2008, S. 015103(15pp). bibcode:2008Nanot..19a5103C. doi:10.1088/0957-4484/19/01/015103.
- Bu Z, Callaway DJ: Proteins MOVE! Protein dynamics and long-range allostery in cell signaling. In: Adv in Protein Chemistry and Structural Biology. 83, 2011, S. 163–221. doi:10.1016/B978-0-12-381262-9.00005-7. PMID 21570668.
- M. Amrute-Nayak, R. P. Diensthuber, W. Steffen, D. Kathmann, F. K. Hartmann, R. Fedorov, C. Urbanke, D. J. Manstein, B. Brenner, G. Tsiavaliaris: Targeted Optimization of a Protein Nanomachine for Operation in Biohybrid Devices. In: Angewandte Chemie. 122, Nr. 2, 2010, S. 322. doi:10.1002/ange.200905200.
- G. M. Patel, G. C. Patel, R. B. Patel, J. K. Patel, M. Patel: Nanorobot: A versatile tool in nanomedicine. In: Journal of Drug Targeting. 14, Nr. 2, 2006, S. 63. doi:10.1080/10611860600612862.
- S. Balasubramanian, D. Kagan, C. M. Jack Hu, S. Campuzano, M. J. Lobo-Castañon, N. Lim, D. Y. Kang, M. Zimmerman, L. Zhang, J. Wang: Micromachine-Enabled Capture and Isolation of Cancer Cells in Complex Media. In: Angewandte Chemie International Edition. 50, Nr. 18, 2011, S. 4161. doi:10.1002/anie.201100115.
- Robert A., Jr. Freitas, Ilkka Havukkala: Current Status of Nanomedicine and Medical Nanorobotics. In: Journal of Computational and Theoretical Nanoscience. 2, Nr. 4, 2005, S. 1–25. doi:10.1166/jctn.2005.001.
- Robert A. Freitas Jr., Ralph C. Merkle: Nanofactory Collaboration