Rotaxane
Rotaxane (lateinisch rota ‚Rad‘; axis, Achse) sind Stoffe, die aus mindestens einem Molekül mit einer linearen Einheit bestehen, welche von mindestens einem Makrocyclus (ein cyclisches Molekül mit einem Ring mit ausreichendem Durchmesser) umschlossen wird. Der Makrocyclus wird nicht kovalent auf seiner Position im Molekül gehalten, beispielsweise durch sperrige endständige Gruppen auf der linearen Einheit, und/oder durch van der Waals-, London-, Coulomb- und dipolare Wechselwirkungen zwischen Schaft und Ring. Es treten komplexe Isomerieformen auf.

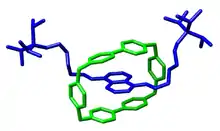
Die Existenz von Rotaxanen wurde 1967 bewiesen als kleiner statistischer Anteil bei gleichzeitiger Synthese eines hantelförmigen und ringförmigen Moleküls.[1] Die erste gezielte Synthese erfolgte durch Gottfried Schill 1967, der auch den Namen vorschlug.[2] Unter anderem für die Synthese von Rotaxanen erhielt Fraser Stoddart 2016 den Nobelpreis für Chemie. Stoddart entwickelte einen effizienten Templat-geführten Syntheseweg.[3]
Synthesen
Es gibt prinzipiell drei Möglichkeiten, Rotaxane darzustellen.
- Threading
- Die Strategie des Threading (engl.: Einfädeln) beruht darauf, dass die lineare Komponente (oft als Faden bezeichnet) in den fertigen Makrocyclus hineingleitet und anschließend durch Anbringen von voluminösen Endgruppen an beiden Seiten des so entstandenen Pseudorotaxanes daran gehindert wird, sich wieder auszufädeln.
- Slipping
- Beim Slipping (engl.: Schlüpfen) werden beide fertigen Komponenten zusammen erhitzt. Dadurch wird genügend Aktivierungsenergie aufgebracht, so dass sich der Ring über die Endgruppen stülpt. Beim Abkühlen bleibt der Makrocyclus wegen der stabilisierenden nicht-kovalenten Wechselwirkungen auf dem Faden.
- Clipping
- Die dritte Möglichkeit ist das sogenannte Clipping (engl.: Klammern). Dabei wird der Makrocyclus in mehreren Teilen erst um den Faden herum koordiniert (wieder getrieben von nicht-kovalenten Wechselwirkungen) und dann durch eine chemische Reaktion geschlossen.
Pseudorotaxane und Semirotaxane
Als „Pseudorotaxane“ werden solche Rotaxane bezeichnet, bei denen der aufgefädelte Makrocyclus nicht durch endständige Gruppen des Moleküls am Verlassen seiner Position gehindert wird, sondern durch Wechselwirkungen mit dem Schaft auf dem der Makrocyclus aufgefädelt ist.
Als „Semirotaxane“ werden solche Rotaxane bezeichnet, bei denen der Makrocyclus nur durch eine der endständigen Gruppen des Moleküls, auf dem er aufgefädelt ist, am Verlassen seiner Position gehindert wird.
Nomenklatur
Gottfried Schill machte 1971 einen Vorschlag[4] zur Nomenklatur der Rotaxane, 2000 schlugen Fritz Vögtle und andere eine erweiterte Form dieser Nomenklatur vor, beide Vorschläge regeln die Nomenklatur aber nicht völlig eindeutig. Eine IUPAC-Empfehlung zur eindeutigen Nomenklatur der Rotaxane wurde 2009 publiziert.[5]
Anwendung
Rotaxane sind als mögliche Schalter und Motoren für die Nanotechnologie von Interesse.
Siehe auch
Weblinks
Einzelnachweise
- Ian Thomas Harrison, Shuyen Harrison: Synthesis of a stable complex of a macrocycle and a threaded chain. J. Am. Chem. Soc., Band 89, 1967, S. 5723–5724.
- Schill, Hubertus Zollenkopf: Rotaxan-Verbindungen (1). Liebigs Ann. Chemie, Band 721, 1969, S. 53–74. Im Aufsatz S. 53 wird darauf hingewiesen, dass der Inhalt auszugsweise auf der Westdeutschen Chemiedozententagung am 13. April 1967 in Saarbrücken vorgetragen wurde (siehe auch Nachr. Chemie Technik, Band 15, 1967, S. 149).
- José A. Bravo, Francisco M. Raymo, J. Fraser Stoddart, Andrew J. White, David J. Williams: High Yielding Template-Directed Syntheses of [2]Rotaxanes. Eur. J. Org. Chem. 1998 (11): 2565–2571.
- Gottfried Schill: Nomenclature of Catenanes and Rotaxanes. In: Gottfried Schill, Catenanes, Rotaxanes, and Knots, Academic Press, 1971, ISBN 9781483275666.
- Ida Schomburg: Nomenklatur der Rotaxane und Pseudorotaxane. In: Angewandte Chemie, 2009, 121, 4719–4738. doi:10.1002/ange.200900665.