Merlin (Protein)
Merlin, auch Neurofibromin 2 oder Schwannomin genannt, ist ein Protein des Zytoskelett. Beim Menschen ist es ein Tumorsuppressorprotein, das an der Entstehung der Neurofibromatose Typ 2 beteiligt ist.[1][2] Sequenzanalysen haben die Ähnlichkeit des Proteins mit der Ezrin-Radexin-Moesin-Proteinfamilie aufgezeigt. Der Name Merlin ist ein Akronym für Moesin-Ezrin-Radixin-Like Protein und hat nichts mit der gleichnamigen literarischen Figur des Zauberers Merlin zu tun.
| Merlin | ||
|---|---|---|
| ||
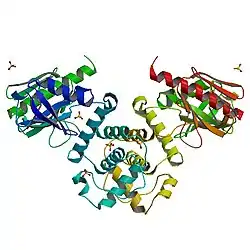
| Neurofibromin 2 nach PDB 1H4R | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 595 Aminosäuren; 69,7 kDa | |
| Isoformen | 10 | |
| Bezeichner | ||
| Gen-Name | NF2 | |
| Externe IDs | ||
| Vorkommen | ||
| Übergeordnetes Taxon | Bilateria (Zweiseitentiere) | |
| Orthologe | ||
| Mensch | Maus | |
| Entrez | 4771 | 18016 |
| Ensembl | ENSG00000186575 | ENSMUSG00000009073 |
| UniProt | P35240 | Q3TIW4 |
| Refseq (mRNA) | NM_000268 | NM_010898 |
| Refseq (Protein) | NP_000259 | NP_035028 |
| Genlocus | Chr 22: 28.33 – 28.42 Mb | Chr 11: 4.67 – 4.75 Mb |
| PubMed-Suche | 4771 | 18016 |
Gen
Für das menschliche Merlin codiert das NF-2 Gen auf Chromosom 22. Das Hausmaus-Merlin-Gen ist auf dem Chromosom 11 der Maus lokalisiert[3] und das Merlin-Gen der Wanderratte auf dem Ratten-Chromosom 17. Das Drosophila-Merlin-Gen (Symbol Mer) findet sich auf dem Chromosom 1 und hat eine 58-prozentige Sequenzähnlichkeit mit seinem menschlichen Homolog. Andere merlinähnliche Gene kennt man von vielen Tieren, und die Entstehung des Merlin vermutet man für die Zeit der Entstehung der Metazoen. Merlin ist ein Mitglied der ERM-Proteinfamilie, zu der Ezrin, Moesin und Radixin gehören. Diese gehören zur Protein-4.1-Superfamilie der Proteine. Merlin wird auch Schwannomin genannt. Dies ist ein Name für den häufigsten Tumor bei NF2-Patienten, dem Schwannom.
Struktur
Das Merlin der Vertebraten ist ein 70-kDa-Protein. Es gibt zehn bekannte Isoformen des menschlichen Merlinmoleküls. Das komplette Molekül hat eine Länge von 595 Aminosäuren. Die beiden am häufigsten vorkommenden Isoformen finden sich auch bei der Maus, werden Typ 1 und Typ 2 genannt und unterscheiden sich durch die Ab- oder Anwesenheit der jeweiligen Exons 16 oder 17. Alle bekannten Varianten haben einen hochkonservierten N-terminalen Teil, der eine sogenannte FERM-Domaine enthält, die sich bei vielen Proteinen findet, die das Zytoskelett mit der Zellmembran verbinden. Der FERM-Domäne folgt eine α-Helix mit einem hydrophilen Anteil.[4] Merlin kann Dimere mit sich selbst und Heterodimere mit anderen Mitgliedern der ERM-Familie bilden.
Funktion
Merlin ist ein Membran-Zytoskelett-Faltungsprotein. Das heißt, es verbindet Aktin-Filamente mit der Zellmembran oder mit Membran-Glykoproteinen.[5] Das menschliche Merlin kommt vor allem in Nervengewebe und einigen fetalen Geweben vor, und findet sich hauptsächlich im Bereich der Adherens Junctions.[6] Seine Tumorsuppressor-Eigenschaften sind möglicherweise mit der kontaktvermittelten Wachstumsinhibierung verbunden. Das Merlin von Drosophila wird hauptsächlich in embryonalen Hinterdarm, Speicheldrüsen und Imaginalscheiben exprimiert und hat offensichtlich eine etwas andere Funktion als das Merlin der Vertebraten.[7]
Eine Phosphorylierung des Serin Nummer 518 ändert die Funktion des Merlin.[8] Zum merlinabhängigen Signalpfad gehören vermutlich einige Mechanismen, die die Zellteilung regeln, so eIF3c, CD44, Proteinkinase A und die p21-aktivierten Kinasen.
Mutationen des NF2-Gens verursachen beim Menschen eine autosomal dominante Erkrankung, die Neurofibromatose Typ 2. Diese Erkrankung ist durch die Entwicklung von Tumoren des Nervensystems, in erster Linie bilaterale vestibuläre Schwannome (auch Akustikusneurom genannt) gekennzeichnet. NF2 gehört zu den Tumorsuppressorgenen.[9]
Einzelnachweise
- Rouleau GA, Merel P, Lutchman M, Sanson M, Zucman J, Marineau C, Hoang-Xuan K, Demczuk S, Desmaze C, Plougastel B: Alteration in a new gene encoding a putative membrane-organizing protein causes neuro-fibromatosis type 2. In: Nature. 363, Nr. 6429, 1993, S. 515–21. doi:10.1038/363515a0. PMID 8379998.
- Golovnina K, Blinov A, Akhmametyeva EM, Omelyanchuk LV, Chang LS: Evolution and origin of merlin, the product of the Neurofibromatosis type 2 (NF2) tumor-suppressor gene. In: BMC Evol. Biol.. 5, 2005, S. 69. doi:10.1186/1471-2148-5-69. PMID 16324214.
- Haase VH, Trofatter JA, MacCollin M, Tarttelin E, Gusella JF, Ramesh V: The murine NF2 homologue encodes a highly conserved merlin protein with alternative forms. In: Hum. Mol. Genet.. 3, Nr. 3, 1994, S. 407–11. doi:10.1093/hmg/3.3.407. PMID 8012352.
- Shimizu T, Seto A, Maita N, Hamada K, Tsukita S, Tsukita S, Hakoshima T: Structural basis for neurofibromatosis type 2. Crystal structure of the merlin FERM domain. In: J. Biol. Chem.. 277, Nr. 12, 2002, S. 10332–6. doi:10.1074/jbc.M109979200. PMID 11756419.
- McClatchey AI, Giovannini M: Membrane organization and tumorigenesis--the NF2 tumor suppressor, Merlin. In: Genes Dev.. 19, Nr. 19, 2005, S. 2265–77. doi:10.1101/gad.1335605. PMID 16204178.
- den Bakker MA, Vissers KJ, Molijn AC, Kros JM, Zwarthoff EC, van der Kwast TH: Expression of the neurofibromatosis type 2 gene in human tissues Archiviert vom Original am 18. Mai 2008. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. In: J. Histochem. Cytochem.. 47, Nr. 11, 1999, S. 1471–80. PMID 10544220. Abgerufen am 24. Februar 2008.
- LaJeunesse DR, McCartney BM, Fehon RG: Structural analysis of Drosophila merlin reveals functional domains important for growth control and subcellular localization. In: J. Cell Biol.. 141, Nr. 7, 1998, S. 1589–99. doi:10.1083/jcb.141.7.1589. PMID 9647651.
- Alfthan K, Heiska L, Grönholm M, Renkema GH, Carpén O: Cyclic AMP-dependent protein kinase phosphorylates merlin at serine 518 independently of p21-activated kinase and promotes merlin-ezrin heterodimerization. In: J. Biol. Chem.. 279, Nr. 18, 2004, S. 18559–66. doi:10.1074/jbc.M313916200. PMID 14981079.
- Scoles DR, Yong WH, Qin Y, Wawrowsky K, Pulst SM: Schwannomin inhibits tumorigenesis through direct interaction with the eukaryotic initiation factor subunit c (eIF3c). In: Hum. Mol. Genet.. 15, Nr. 7, 2006, S. 1059–70. doi:10.1093/hmg/ddl021. PMID 16497727.
Weblinks
- FlyBase synopsis of gene Mer (englisch)