Kaliumformiat
Kaliumformiat ist das Kaliumsalz der Ameisensäure mit der Formel K(HCOO). Es ist eine farblose, zerfließliche Substanz in kristalliner, rhombischer Form. Die Dichte beträgt 1,91 g/cm3, der Schmelzpunkt liegt bei 167,5 °C. Kaliumformiat tritt als Zwischenprodukt im inzwischen technisch unbedeutenden Formiat-Pottasche-Verfahren zur Herstellung von Kaliumcarbonat auf. Der Namensbestandteil -formiat geht auf das lateinische Wort formica (Ameise) zurück.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
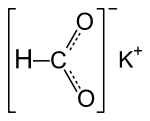 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Kaliumformiat | ||||||||||||||||||
| Summenformel | CHKO2 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 84,12 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,91 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
sehr leicht in Wasser[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−679,7 kJ/mol[3] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Kaliumformiat wird als Flächenenteisungsmittel, beispielsweise auf Straßen und Flughäfen, eingesetzt und hat sich in einer Untersuchung des Finnish Environment Institute (SYKE) im Vergleich zu kochsalzhaltigen Auftaumitteln als verhältnismäßig umweltschonend erwiesen.[4]
Gewinnung und Darstellung
Kaliumformiat kann durch Salzbildungsreaktion aus Kaliumhydroxid und Ameisensäure hergestellt werden.
Ebenso ist die Synthese aus Kaliumcarbonat und Ameisensäure unter Entwicklung von Kohlendioxid möglich.[5]
Einzelnachweise
- Datenblatt Kaliumformiat bei AlfaAesar, abgerufen am 26. März 2010 (PDF) (JavaScript erforderlich).
- Eintrag zu Kaliumformiat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Mai 2017. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-19.
- Alternative de-icer found (Memento vom 27. September 2007 im Internet Archive), Pressemitteilung des Finnischen Umweltministeriums vom 2. Oktober 2004.
- T. Meisel, Z. Halmos, K. Seybold, E. Pungor: "The thermal decomposition of alkali metal formates", in: Journal of Thermal Analysis and Calorimetry, 1975, 7 (1), S. 73–80 doi:10.1007/BF01911627