Hofmannscher Wasserzersetzungsapparat
Der Hofmannsche Wasserzersetzungsapparat, Hofmannsche Zersetzungsapparat oder Wasserzersetzungsapparat nach Hofmann ist ein Gerät zur elektrolytischen Zerlegung von wässrigen Lösungen und wurde nach August Wilhelm Hofmann (1818–1892) benannt, der diesen Versuchsaufbau z. B. in seinem 1866 erschienenen Buch beschrieben hat.[1] Der Versuchsaufbau wurde auch als ein Voltameter benutzt.
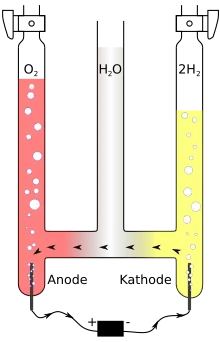
Funktion
Er dient zur Demonstration der elektrolytischen Zersetzung beispielsweise von Wasser. In diesem Fall wird die komplette Apparatur meistens mit verdünnter Schwefelsäure gefüllt, da reines Wasser keine ausreichende elektrische Leitfähigkeit besitzt.[2] Nach dem Anlegen einer Gleichspannung an den Platinelektroden oder Kohleelektroden findet eine Gasentwicklung an Kathode und Anode statt.
Dabei wird das Wasser in seine beiden Bestandteile Sauerstoff und Wasserstoff zerlegt. Die entstehenden Gase sammeln sich in den beiden Messrohren und können mit Hilfe eines Hahns entnommen werden. An der Kathode werden die Oxoniumionen, welche durch Protolyse der zugesetzten Säure entstanden sind, zu Wasserstoff reduziert und an der Anode das Wasser zu Sauerstoff und zu Oxoniumionen oxidiert.
Kathodenreaktion:
Anodenreaktion:
Gesamtreaktion:
Das Verhältnis der Gasvolumina in den Schenkeln wird dabei 1 : 2 (Sauerstoff : Wasserstoff) betragen. Dieses Verhältnis kann allerdings nicht genau zustande kommen, da sich der Sauerstoff am Anfang besser im Wasser löst als Wasserstoff. Um dieses Problem zu umgehen, sollte der Versuch ein paar Minuten zuvor bei geöffneten Hähnen laufen.
Funktionsweise
Die positiv geladenen Oxoniumionen, die sich in der Nähe der negativ geladenen Elektrode, der Kathode, befinden, werden durch die negative Ladung angezogen und dort unter Wasserstofffreisetzung entladen (kathodische Reduktion). Im Bereich der positiv geladenen Elektrode, der Anode, werden dem Wasser Elektronen entzogen (anodische Oxidation). Die oxidierten Wasserteilchen sind instabil und zerfallen unter Freisetzung von Sauerstoff und Bildung von Oxoniumionen. Die Oxoniumionen müssen nicht durch die Lösung zur Kathode wandern, sie geben vielmehr ihre positive Ladung über eine Umorientierung der Wasserstoffbrückenbindungen durch die Lösung bis zur Kathode weiter:

Diese Form der elektrischen Leitung wird Protonenleitung genannt und durch den Grotthus-Mechanismus beschrieben.[3]
Siehe auch
Literatur
- Eintrag zu Hofmannscher Zersetzungsapparat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 21. Juni 2014.
Weblinks
- Der Hofmannsche Zersetzungsapparat (Memento vom 12. November 2011 im Internet Archive) (PDF-Datei; 30 kB)
Einzelnachweise
- August Wilhelm Hofmann: Introduction to modern chemistry: experimental and theoretic; embodying… Walton and Maberly, 1866, S. 55 (eingeschränkte Vorschau in der Google-Buchsuche).
- Peter Kurzweil: Chemie. Springer Vieweg, Wiesbaden 2015, ISBN 978-3-658-08660-2, S. 198, doi:10.1007/978-3-658-08660-2.
- Skript des Schülerlabors Quantensprung der Helmholtz Gesellschaft: Wasserstoff und Brennstoffzelle (PDF; 7,9 MB).