Hexaphenyldistannan
Hexaphenyldistannan ist eine chemische Verbindung aus der Gruppe der zinnorganischen Verbindungen.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
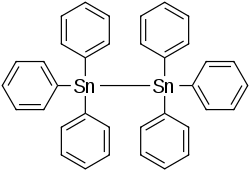 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Hexaphenyldistannan | |||||||||||||||
| Summenformel | C36H30Sn2 | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff mit charakteristischem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 700,05 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Hexaphenyldistannan kann durch Reaktion von Triphenyllithiumzinn mit Kohlendioxid gewonnen werden.[2]
Es entsteht auch bei der Reduktion von Mono-, Diphenylzinn oder Triphenylzinnchlorid (zum Beispiel mit Natrium).[3][4]
Ebenfalls möglich ist die Darstellung durch Reaktion von Phenylisocyanat mit Triphenylzinnhydrid.[5]
Eigenschaften
Hexaphenyldistannan ist ein brennbarer schwer entzündbarer weißer Feststoff mit charakteristischem Geruch, der praktisch unlöslich in Wasser ist. Er zersetzt sich bei Erhitzung über 280 °C.[1] Unter UV-Licht ist es instabil.[3][6] Beim Erhitzen über 250 °C färbt sich die Substanz gelblich. Mit Schwefel reagiert die Verbindung zu trimerem Diphenylsulfid.
Mit Lösungsmitteln bildet es Solvate.[7]
Hexaphenyldistannan besitzt eine monokline Kristallstruktur mit der Raumgruppe P21/c (Raumgruppen-Nr. 14).[8]
Einzelnachweise
- Eintrag zu Hexaphenyldistannan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- B. J. Aylett: Organometallic Compounds Volume One The Main Group Elements Part Two Groups IV and V. Springer Science & Business Media, 2012, ISBN 978-94-009-5729-9, S. 267 (eingeschränkte Vorschau in der Google-Buchsuche).
- Rudolf Bock: Triphenyltin Compounds and Their Degradation Products. Springer Science & Business Media, 2012, ISBN 978-1-4612-5877-3, S. 16 (eingeschränkte Vorschau in der Google-Buchsuche).
- Michel Pereyre, Jean-Paul Quintard, Alain Rahm: Tin in Organic Synthesis. Butterworth-Heinemann, 2013, ISBN 978-1-4831-6107-5, S. 335 (eingeschränkte Vorschau in der Google-Buchsuche).
- S. Coffey: Monocarbonyl Derivatives of Aliphatic Hydrocarbons, Their Analogues and Derivatives A Modern Comprehensive Treatise. Elsevier, 2016, ISBN 978-1-4832-2133-5, S. 359 (eingeschränkte Vorschau in der Google-Buchsuche).
- L. Wilputte-Steinert, J. Nasielski: The photochemistry of aromatic compounds IV. Photochemical behaviour of hexaphenylditin. In: Journal of Organometallic Chemistry. 24, 1970, S. 113, doi:10.1016/S0022-328X(00)91572-9.
- Karin Eckardt, Hartmut Fuess, Masakazu Hattori, Ryuichi Ikeda, Hiroshi Ohki, Alarich Weiss: Structure and Dynamics of Crystal Solvates Hexaphenylditin • 2X, X=Benzene, Toluene, Fluorobenzene, Chlorobenzene, and Aniline. An X-Ray, P(VAPOR)=ƒ(T)> and 2H NMR Study. In: Zeitschrift für Naturforschung A. 50, 1995, doi:10.1515/zna-1995-0808.
- J. Trotter: Structure Reports Organic Section. Springer Science & Business Media, 2013, ISBN 978-94-017-3121-8, S. 550 (eingeschränkte Vorschau in der Google-Buchsuche).

