Hayashi-Umlagerung
Die Hayashi-Umlagerung ist eine Namensreaktion aus der organischen Chemie. Sie wurde nach dem japanischen Chemiker Mosuke Hayashi (1895–1990) benannt, der 1927 erstmals davon berichtete. Bei der Reaktion findet durch Ansäuern mit Schwefelsäure eine Umlagerungsreaktion der o-Benzoylbenzoesäure statt.
Übersichtsreaktion
Die Hayashi-Umlagerung von ortho-Benzoylbenzoesäure im Überblick:
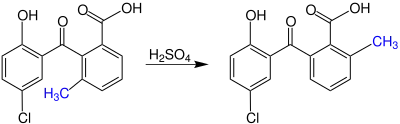
Allgemeines
Die Reaktion läuft bei 173–175 °C ab und benötigt konzentrierte Schwefelsäure als Katalysator. Andere Katalysatoren außer Phosphorpentoxid zeigen keine Wirkung in Bezug auf die Umlagerung.[1] Die Reaktion tritt nur in relativ seltenen Fällen ein, daher hat sie nur einen besonderen Nutzen für die Herstellung spezieller Derivate. Ähnliche Reaktionen laufen auch bei Naphthalinen und Diphenylmethanen ab.[2]
Vorgeschlagener Reaktionsmechanismus
Im nachfolgenden Reaktionsmechanismus[2] stehen die grauen Pfeile für eine Drehung um die Achse an der sie gesetzt sind und die roten für eine Elektronenwanderung. Zunächst muss eine Drehung an der gekennzeichneten Verbindung in 1 getätigt werden, damit der räumliche Zusammenhang in der Reaktion 3 schlüssig wird. In 2 erfolgt eine nukleophile Addition des Protons an die Carbonylgruppe des Ketons, wodurch die Abbildung 3 entsteht. Durch Elektronenmangel bedingt, klappt das Elektronenpaar der Carbonylgruppe zum Sauerstoff und es entsteht ein Carbokation, welches sterisch bedingt von der OH-Gruppe der Carbonsäure nucleophil angegriffen wird. Es entsteht die Verbindung 4. Die nun folgenden reaktiven Zwischenstufen sind explizit in eckige Klammern gesetzt, da sie instabil und nur von sehr kurzer Lebensdauer sind. Es spaltet sich aus 4 gleichzeitig das H+ und die linke Arylgruppe ab, wobei das Elektronenpaar der Arylgruppe eine Bindung zum H+ eingeht. Folglich entsteht der Übergangszustand 5, welcher ladungsbedingt eine Elektronenwanderung verursacht und zu der Konstitution 6 führt. In den Abbildungen 6 und 7 wird lediglich die Stellung des Moleküls korrigiert. Die nun elektrophile Addition in 8 erfolgt derigierend durch die OH-Gruppe am Benzolring in ortho-stellung. Durch den genauen Reaktionsmechanismus ist nun erkennbar, dass eine Abspaltung des rechten Benzolrings mit dem Keton erfolgt und eine neue Anbindung durch die Carboxygruppe vonstatten geht.

Literatur
- Zerong Wang:Comprehensive Organic Name Reactions and Reagents, Volume 2, Wiley, 2009, S. 1347–1349, ISBN 978-0-471-70450-8
- The Merck Index, 9. Auflage, Merck & Co. 1976, ONR-41, ISBN 0911910-26-3
Einzelnachweise
- M. G. Zolotukhin, F. J. Balta Calleja, D. R. Rueda, M. Bruix, Yu. L. Sorokina, E. A. Sedova: Macromolecules. Band 28, 1995, S. 7325–7330, doi:10.1021/ma00126a006.
- Zerong Wang: Comprehensive Organic Name Reactions and Reagents, Volume 2, Wiley, 2009, S. 1347 f., ISBN 978-0-471-70450-8.