Fluorperchlorat
Fluorperchlorat ist eine chemische Verbindung aus der Gruppe der Perchlorate.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
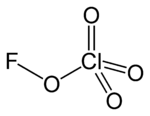 | ||||||||||
| Allgemeines | ||||||||||
| Name | Fluorperchlorat | |||||||||
| Andere Namen |
Chlortetroxidfluorid | |||||||||
| Summenformel | FClO4 | |||||||||
| Kurzbeschreibung |
farbloses, scharf sauer riechendes Gas[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 118,46 g·mol−1 | |||||||||
| Aggregatzustand |
gasförmig[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
−15,9 °C[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gewinnung und Darstellung
Fluorperchlorat kann durch Reaktion von Perchlorsäure mit Fluor bei tiefen Temperaturen gewonnen werden.[1]
Eigenschaften
Fluorperchlorat ist ein farbloses, scharf sauer riechendes, sehr explosives Gas. Es explodiert häufig schon beim Schmelzen, Kondensieren oder als Gas (ähnlich wie Nitroxyfluorid NO3F) schon bei Berührung mit Staub, Fett oder Gummi. Im offenen Reagenzglas explodiert das Gas bei Berührung mit einer Flamme oder einer Funkenstrecke.[1]
Sicherheitshinweise
Fluorperchlorat reizt den Rachen und die Lungen. Es erzeugt lang anhaltende Atemnot.[1]
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 180.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.