Etravirin
Etravirin (ETV, Handelsname: Intelence®; Hersteller: Tibotec) ist ein Arzneistoff zur Behandlung HIV-infizierter Patienten im Rahmen einer HIV-Kombinationstherapie.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
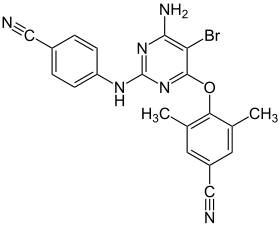 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Etravirin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C20H15BrN6O | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
J05AG04 | |||||||||||||||||||||
| Wirkstoffklasse |
Virustatikum, nichtnukleosidische Reverse-Transkriptase-Inhibitoren | |||||||||||||||||||||
| Wirkmechanismus |
nicht-kompetitive Hemmung der reversen Transkriptase | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 435,28 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Etravirin gehört zur Substanzklasse der nichtnukleosidischen Reverse-Transkriptase-Inhibitoren (NNRTI).
Geschichte
Intelence in Kombination mit anderen antiretroviralen Arzneimitteln wurde für die Therapie von Infektionen mit HIV-1 bei bereits vergeblich behandelten Patienten in den USA im Januar 2008 und in der Europäischen Union im August 2008 zugelassen.
Pharmakologie
Etravirin gehört zur Substanzklasse der nichtnukleosidischen Reverse-Transkriptase-Inhibitoren (NNRTI). Der Wirkstoff bindet nicht-kompetitiv an die Reverse Transkriptase von HIV-I, nahe der Substratbindungsstelle für Nukleoside. Dadurch wird die katalytisch aktive Bindungsstelle blockiert. Es können nur wenige Nukleoside binden und die Polymerisation wird deutlich verlangsamt.
Nebenwirkungen
Im Allgemeinen wird Etravirin gut vertragen, allerdings traten in einigen Studien die für NNRTIs typischen Nebenwirkungen Schwindel und Hautausschlag auf.[2] Die Nebenwirkungen führten aber selten zum Therapieabbruch.
Mitte 2009 gab der Hersteller bekannt, dass es zu einem Todesfall infolge eines Lyell-Syndroms sowie zu Überempfindlichkeitsreaktionen kombiniert mit Leberversagen kam.[3]
Resistenzen
Gegenüber anderen NNRTIs hat Etravirin den Vorteil, dass es, neben einer sehr guten Wirkung gegen den Wildtyp, auch noch gegen die meisten NNRTI-resistenten Stämme gut wirksam ist. In Phase I/II Studien zeigte Etravirin seine hohe Potenz bei der Absenkung der Viruslast.[4]
Weblinks
Einzelnachweise
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von 4-(6-Amino-5-bromo-2-(4-cyanoanilino)pyrimidin-4-yloxy)-3,5-dimethylbenzonitrile im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 10. Februar 2020.
- Kakuda 2006.
- Tibotec Therapeutics: Intelence: Important Drug Warning. (PDF; 74 kB) FDA, August 2009; abgerufen am 27. August 2009.
- B. Gruzdev, A. Rakhmanova, E. Doubovskaya u. a.: A randomized, double-blind, placebo-controlled trial of TMC125 as 7-day monotherapy in antiretroviral naive, HIV-1 infected subjects. In: AIDS, 17, 2003, S. 2487–2494. PMID 14600520.