Dihydrolipoyl-Dehydrogenase
Die Dihydrolipoyl-Dehydrogenase (DLDH, E3, Protein L) ist das Enzym in allen Lebewesen, das die Dehydrierung von Dihydroliponamid katalysiert. Als Untereinheit E3 des Pyruvat-Dehydrogenase-Komplexes (PDC) und des α-Ketoglutarat-Dehydrogenase-Komplexes ist sie unentbehrlich für die Aufrechterhaltung der Glykolyse und des Citratzyklus. Als Untereinheit E3 des Verzweigtkettige-α-Ketosäuren-Dehydrogenase-Komplexes (BCKD) ist sie notwendig zum Abbau der Aminosäuren Valin, Leucin und Isoleucin. Außerdem ist DLDH Bestandteil des Glycin-spaltenden Systems, eines Enzymkomplexes in einem Abbauweg von Glycin. Mutationen im DLD-Gen können zu DLDH-Mangel und dieser zur Ahornsirupkrankheit Typ III und zum Leigh-Syndrom führen.[2]
| Dihydrolipoyl-Dehydrogenase | ||
|---|---|---|
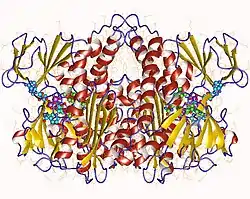 | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 474 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Kofaktor | FAD | |
| Bezeichner | ||
| Gen-Name | DLD | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 1.8.1.4, Oxidoreduktase | |
| Reaktionsart | Dehydrierung | |
| Substrat | Protein N(6)-(dihydrolipoyl)lysin + NAD+ | |
| Produkte | Protein N(6)-(lipoyl)lysin + NADH/H+ | |
| Vorkommen | ||
| Übergeordnetes Taxon | Lebewesen[1] | |
DLDH und Dihydroliponamid sind zusammen in der Lage, S-Nitrosogruppen an Proteinen zu denitrosieren, eine Aufgabe, die normalerweise von Thioredoxin übernommen wird. DLDH kann außerdem Nitrogruppen an DNA und Proteinen zum Amin reduzieren und ist so Teil des Metabolismus reaktiver Stickstoffspezies.[3][4]
Einzelnachweise
- Homologe bei eggNOG
- UniProt P09622
- Sengupta R, Billiar TR, Atkins JL, Kagan VE, Stoyanovsky DA: Nitric oxide and dihydrolipoic acid modulate the activity of caspase 3 in HepG2 cells. In: FEBS Lett.. 583, Nr. 21, November 2009, S. 3525–30. doi:10.1016/j.febslet.2009.10.016. PMID 19822150.
- Chen HJ, Chen YM, Chang CM: Lipoyl dehydrogenase catalyzes reduction of nitrated DNA and protein adducts using dihydrolipoic acid or ubiquinol as the cofactor. In: Chem. Biol. Interact.. 140, Nr. 3, August 2002, S. 199–213. PMID 12204577.
Weblinks
- OrphaNet: Lipoamid-Dehydrogenase-Mangel
- OrphaNet: Pyruvat-Dehydrogenase-Mangel